Clear Sky Science · ru
Последовательное применение платиновой химиотерапии и ингибирования PARP усиливает эффективность иммунотерапии PD1 в мышиной модели панкреатического рака с мутацией Brca2
Почему это исследование важно для пациентов
Рак поджелудочной железы — один из самых смертельных видов рака, и даже при наличии у опухоли очевидной уязвимости — например, мутации в гене BRCA2 — современные методы лечения редко обеспечивают длительный контроль болезни. В этом исследовании на реалистичной мышиной модели задают практический вопрос, с которым сейчас сталкиваются многие пациенты и онкологи: может ли добавление современной иммунотерапии после интенсивной химиотерапии и ингибитора PARP существенно продлить выживание, и почему опухоли так часто рецидивируют?
Упрямый рак с генетической слабой стороной
Аденокарцинома протоков поджелудочной железы крайне трудно поддаётся лечению, и пятилетняя выживаемость остаётся в однозначных процентах. Небольшая часть пациентов несёт наследственные или опухолево-специфические дефекты в BRCA2 — гене, необходимом для ремонта разрывов ДНК. Такие опухоли особенно чувствительны к препаратам, повреждающим ДНК, например к платиновым схемам химиотерапии, а также к ингибиторам PARP, которые ещё сильнее нарушают способность раковых клеток восстанавливать ДНК. Современная стандартная практика при распространённом BRCA-мутационном раке поджелудочной железы — месяцы платиновой химиотерапии с последующим поддерживающим лечением ингибитором PARP. Однако в ключевом клиническом исследовании POLO эта стратегия не увеличила общую выживаемость, что подчёркивает необходимость понимания механизмов резистентности и разработки лучших поддерживающих подходов.
Создание более правдоподобной мышиной модели
Многие существующие лабораторные модели лишают опухоль иммунных и стромальных компонентов, которые окружают реальные опухоли у пациентов. Чтобы преодолеть это, авторы создали мышей, у которых развиваются опухоли поджелудочной железы с дефицитом BRCA2 на фоне полностью функционирующей иммунной системы. Из этих спонтанных опухолей они вывели клональные клеточные линии, которые можно было имлантировать в генетически совместимых мышей. Эти опухоли с мутацией Brca2 выглядели и вели себя похоже на человеческие панкреатические раки: они были плотно фиброзными, в значительной степени исключали T-клетки и демонстрировали высокий уровень спонтанного повреждения ДНК. Что важно, опухоли были очень чувствительны к обычной платиновой комбинации (гемцитабин плюс цисплатин), тогда как монотерапия ингибитором PARP давала лишь умеренный и кратковременный эффект у животных, несмотря на сильную активность против тех же клеток в культуре. 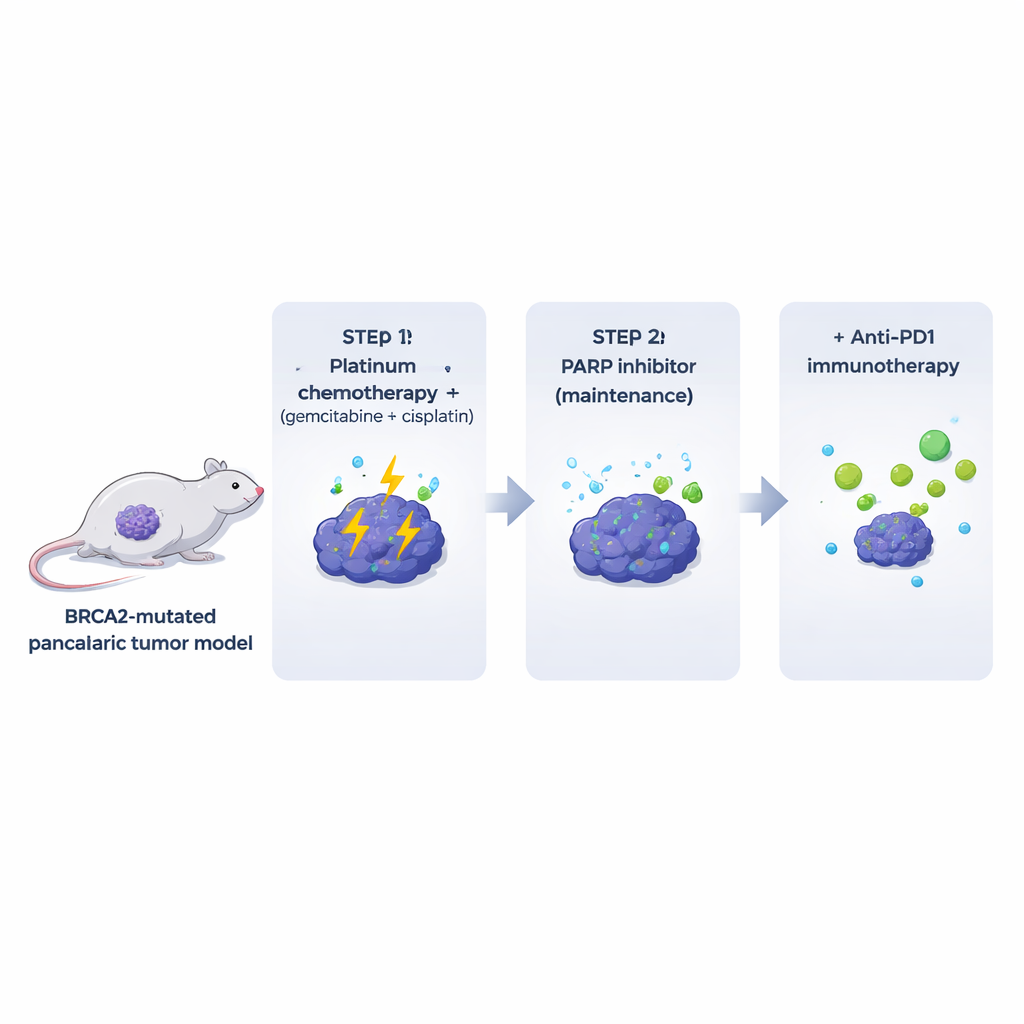
Химиотерапия перестраивает опухолевое окружение
Команда далее исследовала, что происходит внутри опухоли после платиновой химиотерапии. Через десять дней после лечения опухоли уменьшились, но не были полностью уничтожены. Анализы экспрессии генов показали заметный сдвиг в сторону иммунной активности: включились пути, связанные с активацией T-клеток и адаптивным иммунитетом. В обработанных опухолях обнаружилось больше T-клеток, и многие из них несли маркеры истощения — признаки того, что они были активированы, но теряли эффективность. Схожие закономерности увеличения присутствия T-клеток наблюдали в образцах человеческих панкреатических опухолей с мутациями BRCA или связанными PALB2 после того, как пациенты получили платиновую химиотерапию до операции. Одновременно опухолевые клетки усиливали экспрессию PD-L1 — белка на поверхности, который может выключать T-клетки, взаимодействуя с рецептором PD-1, — что указывает на то, что опухоли защищаются от нового иммунного давления.
Почему PARP в одиночку недостаточен и где возникает резистентность
Воспроизводя клиническую практику, исследователи провели мышам начальный курс гемцитабина и цисплатина, а затем поддерживающее лечение ингибитором PARP олапарибом. Такая последовательность улучшила контроль опухоли и выживаемость по сравнению с одной химиотерапией, подтвердив, что предшествующая химиотерапия может сделать опухоли более чувствительными к ингибированию PARP. Однако ни одна мышь не была излечена: опухоли в конце концов возобновляли рост под поддерживающей терапией PARP. Резистентные опухоли приобрели более дифференцированный вид и значительно увеличили уровни регулятора развития CDX2. Это говорит о том, что, по крайней мере в этой модели, резистентность не обязательно возникает из восстановления исходного дефекта репарации ДНК, а может сопровождаться изменением клеточной идентичности опухоли. CDX2 потенциально может служить биомаркером развивающейся резистентности у пациентов.
Открывая иммунотерапию подходящей последовательностью
Ингибиторы иммунных контрольных точек, такие как антитела против PD-1, преобразили лечение ряда опухолей, но рак поджелудочной железы остаётся в основном нечувствительным. В соответствии с этим антитела против PD-1 (с дополнительным анти-CTLA4 или без) не помогли при первично необработанных опухолях с мутацией BRCA2 и почти не дали эффекта, когда их просто добавляли к терапии ингибитором PARP. Картина изменилась, когда применили полную последовательность: сперва платиновая химиотерапия, затем поддержание ингибитором PARP с добавлением анти-PD1. В этом случае опухоли сократились глубже, и мыши жили дольше, чем при химиотерапии плюс PARP-ингиботор или анти-PD1 по отдельности. Добавление анти-CTLA4 к поддерживающему PARP не давало аналогичных преимуществ, что позволяет предположить: окружение опухоли, подготовленное химиотерапией, особенно восприимчиво к блокаде PD-1. 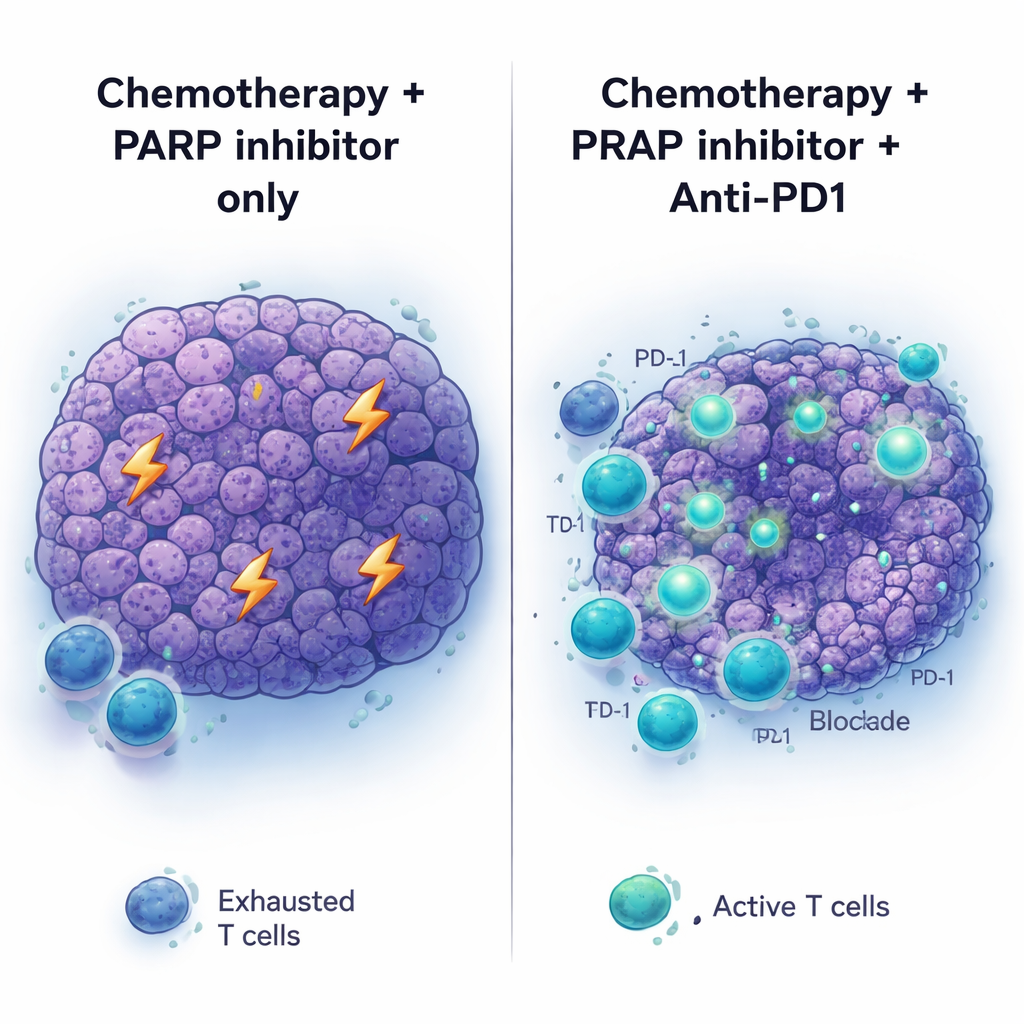
Что это может значить для будущего лечения
В сумме исследование показывает, что для BRCA-мутационного рака поджелудочной железы порядок и сочетание терапий имеют большое значение. Интенсивная ДНК-повреждающая химиотерапия не только напрямую поражает опухолевые клетки, но и активизирует иммунный ответ, даже если он изначально ослаблен состоянием истощения и защитой через PD-L1. Ингибиторы PARP могут продлить пользу, но в одиночку вряд ли приведут к излечению и могут способствовать сдвигу опухолей в резистентное состояние с высоким уровнем CDX2. Наложение анти-PD1 иммунотерапии на поддерживающую PARP-терапию после платиновой химиотерапии может преобразовать кратковременно воспалённую, истощённую иммунную среду в более эффективную и долговременную противоопухолевую реакцию. Текущие клинические исследования, комбинирующие ингибиторы PARP с иммунотерапией при BRCA‑связанном раке поджелудочной железы, будут ключевыми для выяснения, может ли эта тщательно подобранная по времени стратегия привести к более долгой и качественной жизни пациентов.
Цитирование: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Ключевые слова: рак поджелудочной железы, мутация BRCA2, платиновая химиотерапия, ингибитор PARP, иммунотерапия PD-1