Clear Sky Science · ru
Исследование функционально значимых остатков фермента с помощью мониторинга ферментативной реакции в реальном времени методом ЯМР и вычислительных подходов
Почему это важно для будущих противовирусных средств
Фавипиравир — таблетка, уже применяемая против гриппа и испытываемая для лечения COVID-19, но в той форме, которую мы принимаем внутрь, он не борется с вирусами. Наши клетки сначала должны превратить его в активную молекулу, блокирующую вирус. В этом исследовании почти атом за атомом разобрано, как один человеческий фермент выполняет ключевой этап активации и какие крошечные участки фермента служат «горячими точками», определяющими скорость и эффективность превращения препарата. Понимание этих деталей может помочь в проектировании следующего поколения противовирусных средств, которые будут более мощными и предсказуемыми в организме пациентов.
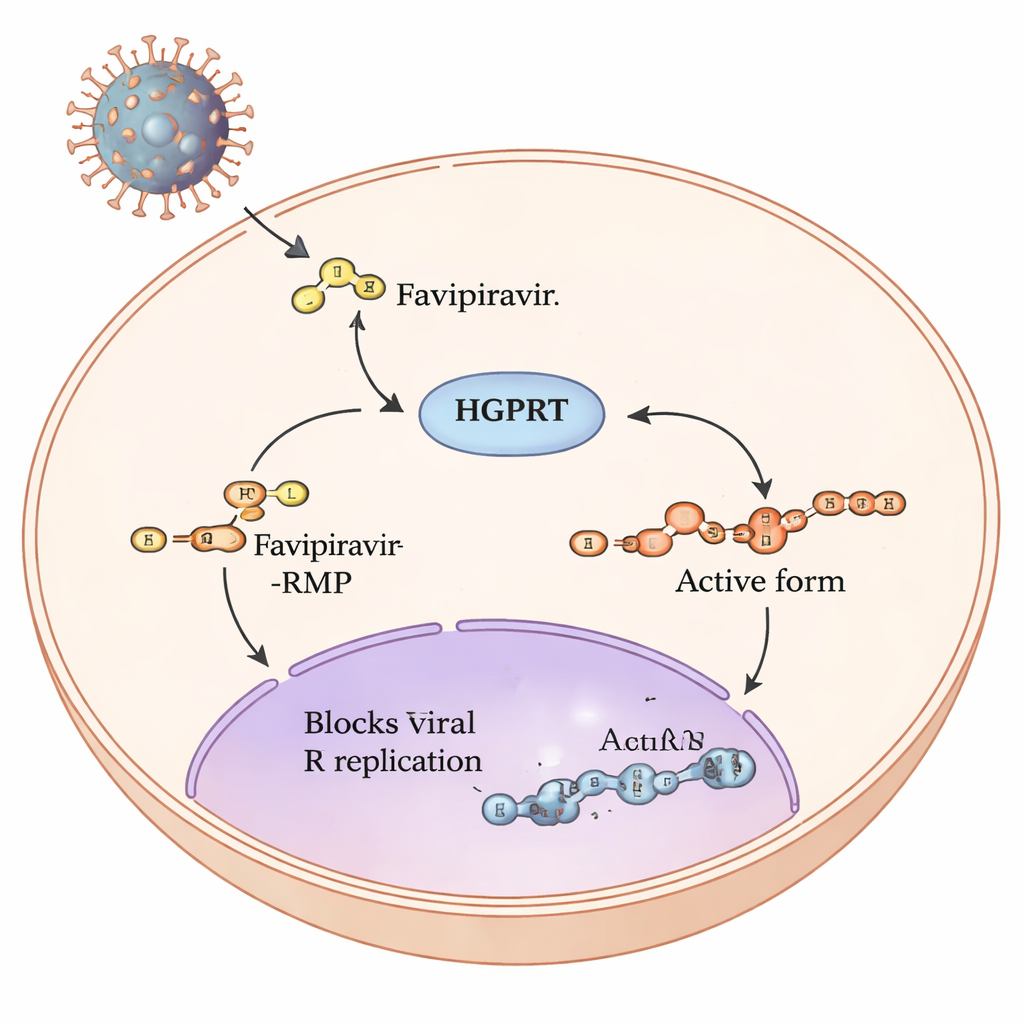
Путь пролекарства внутри наших клеток
Фавипиравир — так называемое пролекарство: попав в человеческие клетки, он претерпевает серию химических преобразований, превращающих его в форму, способную блокировать механизмы копирования РНК-вирусов, таких как грипп и SARS‑CoV‑2. Первый и самый медленный шаг в этом пути осуществляет человеческий фермент гипоксантин-гуанинфосфорибозилтрансфераза, или HGPRT. HGPRT присоединяет к фавипиравиру небольшой сахарофосфатный фрагмент, образуя фавипиравир‑RMP. Только после этого другие ферменты могут построить полностью активную трифосфатную форму, которая напрямую вмешивается в работу вирусной РНК-полимеразы. Поскольку первый шаг, управляемый HGPRT, действует как узкое место для образования активного препарата, авторы поставили целью определить, какие участки HGPRT наиболее важны для обработки фавипиравира.
Наблюдение химии в реальном времени с помощью ЯМР
Особенность фавипиравира в том, что он содержит атом фтора, который в магнитном поле ведет себя как крошечный радиопередатчик. Команда использовала это, записывая спектры методом фтор‑19 ЯМР, чтобы в реальном времени отслеживать, сколько фавипиравира и сколько фавипиравир‑RMP присутствует в пробирке по мере протекания реакции. Поскольку фтор есть только в самом препарате, сигналы ЯМР получаются чистыми и легко отслеживаемыми. Повторяя съёмку спектров в течение 12 часов, исследователи могли следить за исчезновением исходного препарата и нарастанием модифицированного продукта, а затем извлекать стандартные кинетические параметры, такие как скорость реакции и кажущаяся сила связывания фермента с препаратом.
Настройка ключевых позиций в ферменте
Ранние рентгеновские снимки HGPRT, связанного с фавипиравир‑RMP, указывали на несколько аминокислот, которые удерживают препарат в кармане. Новая работа проверяет три из этих позиций, вводя точечные замены аминокислот и сравнивая каждую мутантную версию фермента с естественной. Одна замена, обозначенная T138A, неожиданно увеличила скорость превращения фавипиравира примерно в четыре–шесть раз, хотя при этом была удалена химическая группа, которую ранее считали помогающей удерживать препарат. Вторая замена, K140M, умеренно замедлила реакцию и слегка ослабила кажущееся связывание. Третья замена, D193N, полностью лишила фермент способности синтезировать фавипиравир‑RMP, хотя изменённый белок всё ещё мог собираться и связывать продукт. В совокупности эти результаты показывают, что не все контактные точки равнозначны: одни действуют как тонкие регуляторы скорости, другие — как жизненно важные переключатели.
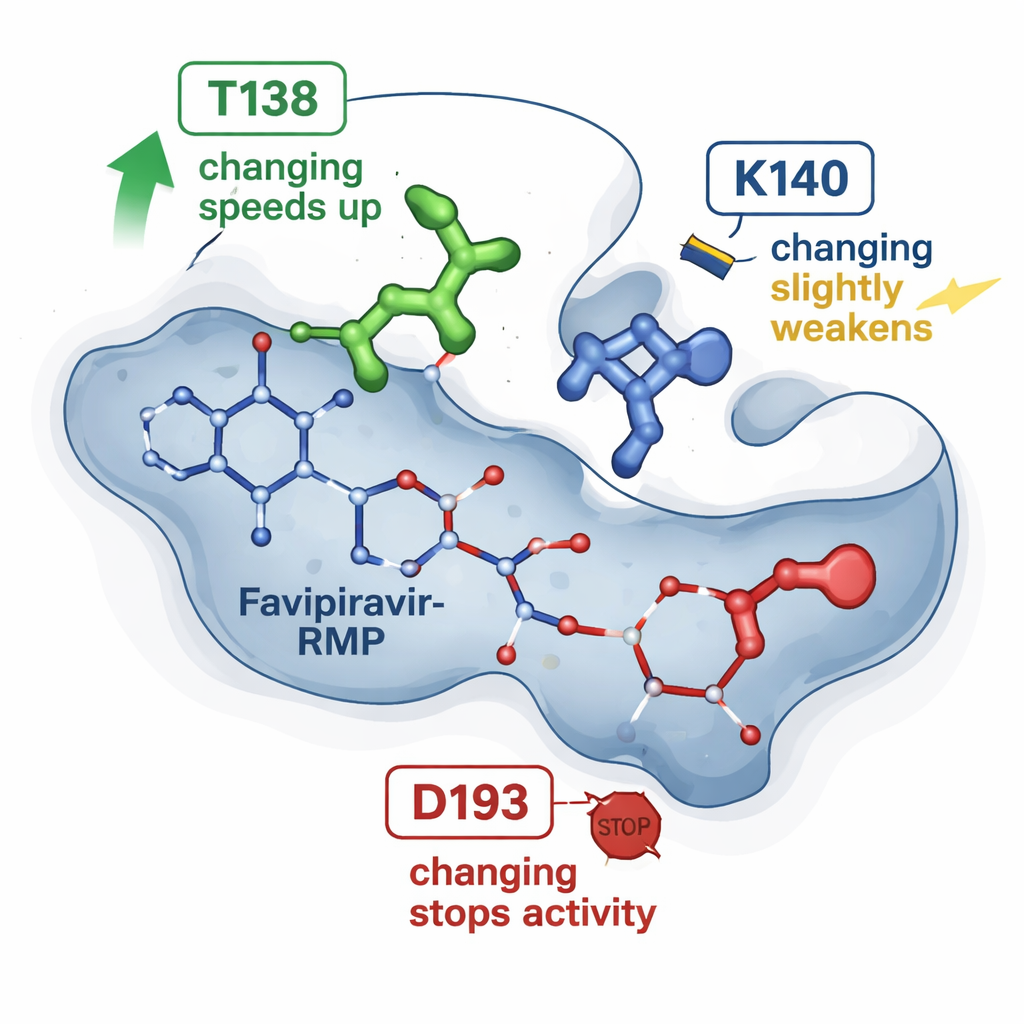
Моделирование подвижных частей на компьютере
Чтобы заглянуть дальше статичных структур, исследователи обратились к молекулярному моделированию. Исходя из известной трёхмерной структуры HGPRT с фавипиравир‑RMP, они использовали проверенные вычислительные инструменты для оценки силы связывания препарата в каждом мутанте и провели множество коротких молекулярно‑динамических симуляций. Эти симуляции отслеживают, как атомы дрожат и взаимодействуют в течение десятков наносекунд. Вычисления согласовались с наблюдаемыми ЯМР трендами: вариант T138A, как правило, удерживал фавипиравир‑RMP более благоприятно, но также демонстрировал эпизоды, когда препарат смещался к «пути побега», направляемому другой остаточной группой (K140), которая кратковременно якорит фосфатную группу перед высвобождением. Напротив, вариант D193N по‑прежнему удерживал продукт, но, вероятно, давал сбой на более раннем каталитическом этапе, требующем иона магния, что объясняет потерю активности несмотря на стабильное связывание.
Дорожная карта для более разумного проектирования противовирусных средств
Комбинируя измерения в реальном времени методом ЯМР с детальными компьютерными моделями, это исследование картирует функциональные «горячие точки» в HGPRT, управляющие эффективностью активации фавипиравира. Для неспециалистов основная идея такова: наши собственные ферменты могут значительно влиять на то, сколько активного противовирусного препарата накапливается внутри клеток, и изменение либо формы препарата, либо кармана фермента может кардинально изменить этот результат. Гибридная стратегия авторов предлагает общий план для изучения взаимодействий других лекарств с их целевыми белками, что потенциально ускорит разработку новых противовирусных соединений, лучше согласованных с клеточными механизмами активации.
Цитирование: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
Ключевые слова: фавипиравир, активация противовирусного препарата, фермент HGPRT, ЯМР-спектроскопия, разработка лекарств