Clear Sky Science · ru
Система метки REC без лизина для применений с proximity‑биотинилированием
Почему маленькие метки на белках важны
Внутри каждой клетки белки редко действуют в одиночку — они объединяются в меняющиеся партнёрства, которые управляют здоровьем и болезнью. Чтобы изучать эти партнёрства, учёные часто прикрепляют к белкам небольшие «именные ярлыки», чтобы отслеживать их, выделять из смеси или визуализировать под микроскопом. Популярный метод, называемый proximity‑биотинилированием, позволяет картировать, кто находится рядом с кем внутри клетки, но у него есть скрытая проблема: многие такие ярлыки химически модифицируются и фактически исчезают именно в тот момент, когда они наиболее нужны. В этом исследовании предложена новая разновидность метки, названная REC, разработанная так, чтобы оставаться видимой в этих тяжёлых условиях.
Химический маркер для соседей белка
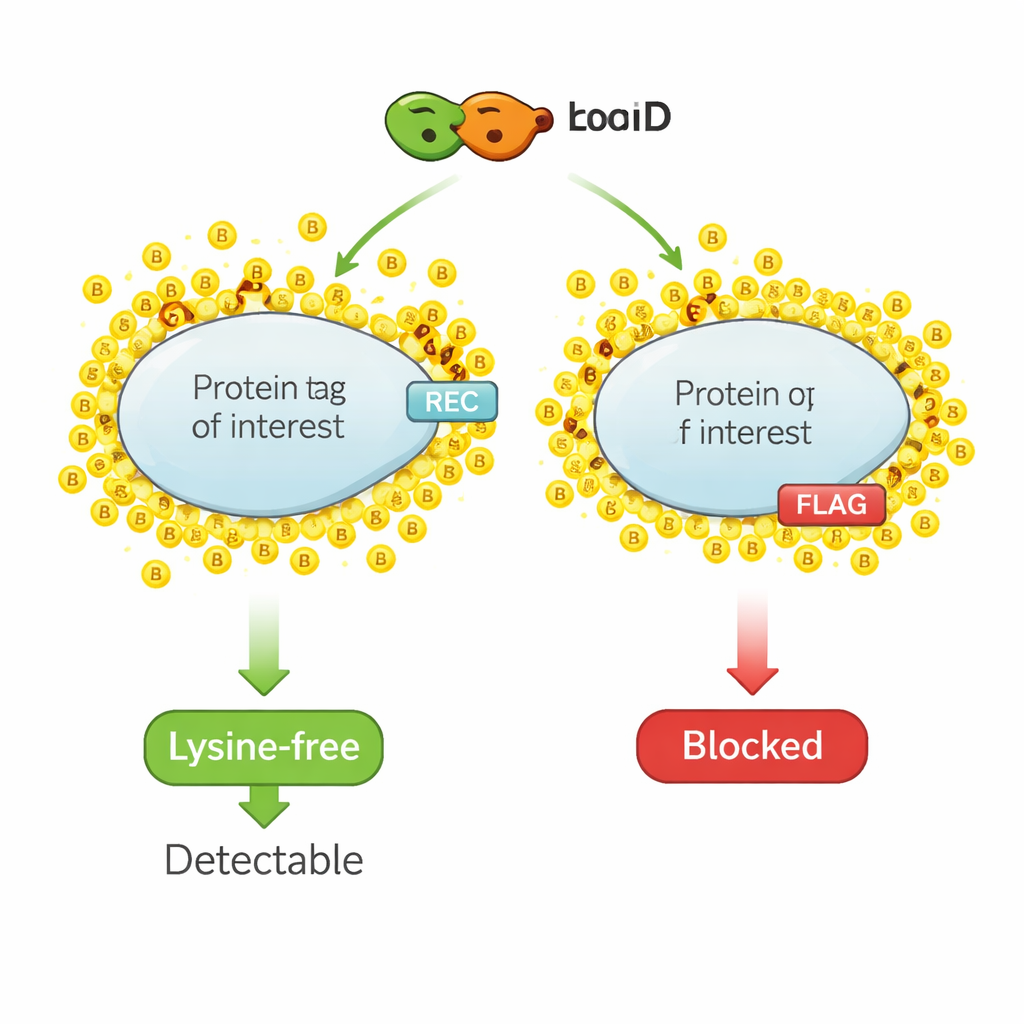
Proximity‑биотинилирование работает как молекулярный маркер‑хайлайтер. Инженерный фермент, такой как TurboID, сливают с интересующим белком. При добавлении биотина — маленького витамина — TurboID быстро присоединяет молекулы биотина к находящимся поблизости белкам. Исследователи затем извлекают все биотинилированные белки и идентифицируют их, получая моментальную «карту» соседства белков. Однако та же химия, которая маркирует соседние белки, также нацеливается на небольшие эпитопные метки, обычно используемые для детекции, потому что эти метки часто содержат лизин — аминокислоту, являющуюся основной мишенью для биотинилирования. Когда лизины в метке покрываются биотином, антитела больше не могут распознать метку, и сигнал в стандартных методах детекции падает или исчезает.
Проектирование метки, нечувствительной к модификации
Чтобы решить эту проблему, авторы поставили цель создать новую метку, полностью лишённую лизина. В качестве исходной точки они взяли фрагмент белка паразита малярии, называемый PfRipr5, который слабо похож на белки человека, что снижает риск нежелательных перекрёстных реакций. С помощью микрочипового скриннинга в кроликах они получили 22 моноклональных антитела против PfRipr5 и обнаружили одно, названное клон №6, с особенно сильным и специфичным сродством. Путём систематического укорачивания и мутаций фрагмента PfRipr5 они сузили эпитоп антитела до участка из 11 аминокислот. Эта минимальная последовательность содержала только один лизин, который они заменили на сходную аминокислоту — аргинин. Удивительно, но антитело по‑прежнему связывалось так же хорошо. Оптимизированная, лишённая лизина последовательность получила название метки REC, а соответствующее антитело — антитело REC.
Испытания метки REC
Затем команда проверила, может ли метка REC заменить широко используемые метки, такие как FLAG, в обычных лабораторных методах. При слиянии с флуоресцентными или сигнальными белками и при экспрессии в безклеточных системах и клетки млекопитающих REC‑метки легко обнаруживались при иммуноблоттинге, в чувствительном световом планшетном тесте AlphaScreen и при иммуногистохимии в клетках. Сила детекции была сопоставима с меткой FLAG и с другой системой безлизиновой метки (AGIA), а антитело REC демонстрировало очень низкий фон на ряде человеческих и обезьяньих линий клеток. Важно, что метка работала как при расположении на N‑терминальном, так и на C‑терминальном конце белка, а также на белках, находящихся в разных клеточных компартментах, включая ядро, митохондрии, эндоплазматический ретикулум и клеточную мембрану.
Оставаться видимым при интенсивной маркировке
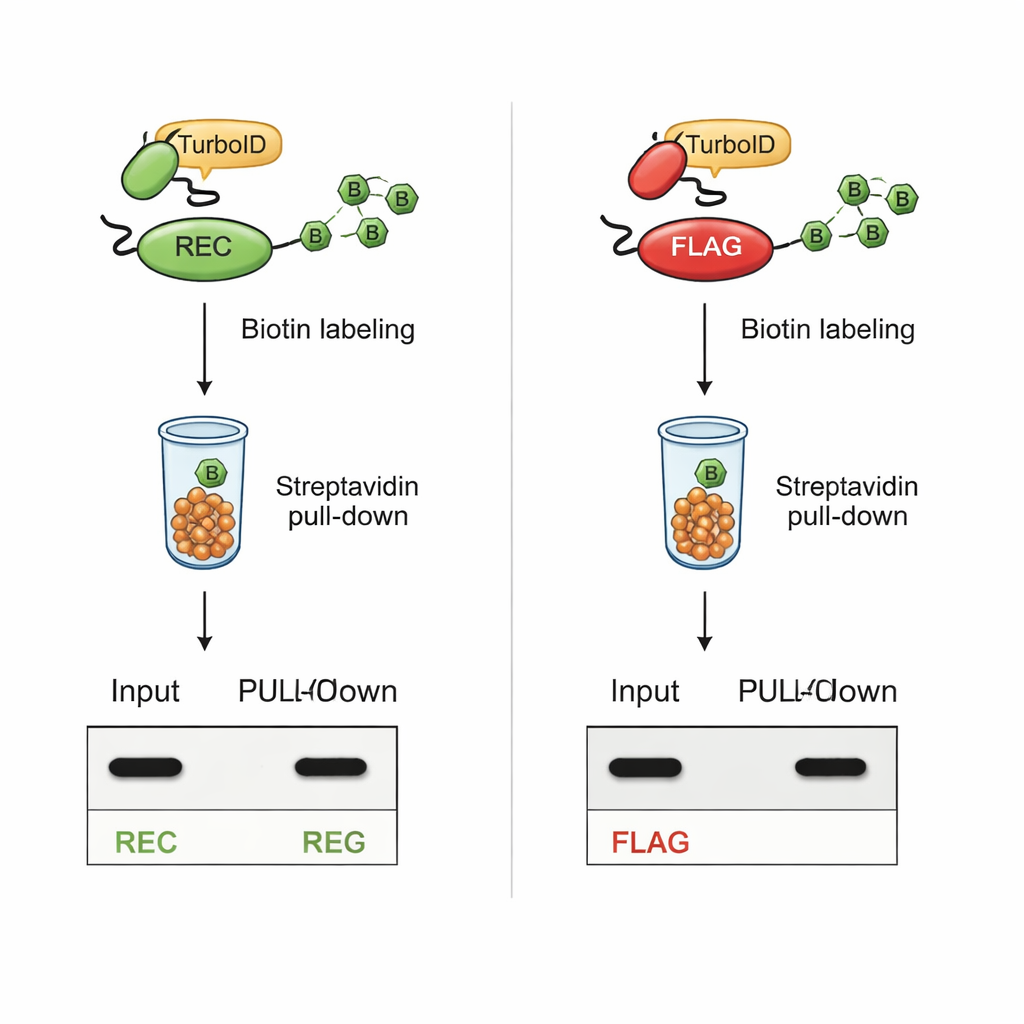
Ключевой проверкой было то, останется ли REC детектируемой после биотинилирования, основанного на TurboID. В клетках, где TurboID был слит с известными партнёрами по взаимодействию, белки с меткой REC оставались чётко видимыми как в цельных клеточных экстрактах, так и в очищенной биотинилированной фракции. Напротив, белки с классической меткой FLAG теряли сигнал FLAG при активации TurboID, хотя сами белки при этом всё ещё присутствовали. Дополнительные эксперименты с синтетическими пептидами показали, что TurboID напрямую биотинилирует лизины в последовательности FLAG, физически блокируя доступ антител. Метка REC, полностью лишённая лизина, оставалась нетронутой TurboID и продолжала легко детектироваться.
Что это значит для будущих экспериментов
Для исследователей, изучающих сети белковых взаимодействий в живых клетках, метка REC предлагает практичный новый инструмент: она ведёт себя как привычные метки в повседневных анализах, но продолжает работать даже при активности мощных ферментов proximity‑маркировки. Это позволяет учёным более надёжно удостоверяться, что их меченые белки присутствуют и правильно захвачены, а также изучать другие лизин‑зависимые модификации — например, убиквитинирование и ацетилирование — без вмешательства со стороны самой метки. Проще говоря, REC — небольшое изменение в дизайне с большим эффектом, помогающее сделать сложные эксперименты по картированию белков более понятными и надёжными.
Цитирование: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Ключевые слова: метки белков, proximity‑биотинилирование, TurboID, взаимодействия белков, эпитопные метки