Clear Sky Science · ru
Взаимодействие между метилированием ДНК ELMO1 и Med31 способствует EMT и кишечной метаплазии, индуцируемым H. pylori, через поляризацию M2
Почему бактерии желудка важны для риска рака
У большинства из нас в пищеварительном тракте обитают миллиарды бактерий, и одна из них — Helicobacter pylori — может тихо жить в желудке десятилетиями. Для некоторых людей эта инфекция безвредна, но у других она становится первым шагом на пути к раку желудка, одному из самых смертоносных видов рака в мире. В этом исследовании рассматривается, как крошечное химическое изменение в ДНК клеток желудка помогает превратить длительную инфекцию в предраковое повреждение и, в конечном счёте, в среду, благоприятную для развития опухоли.
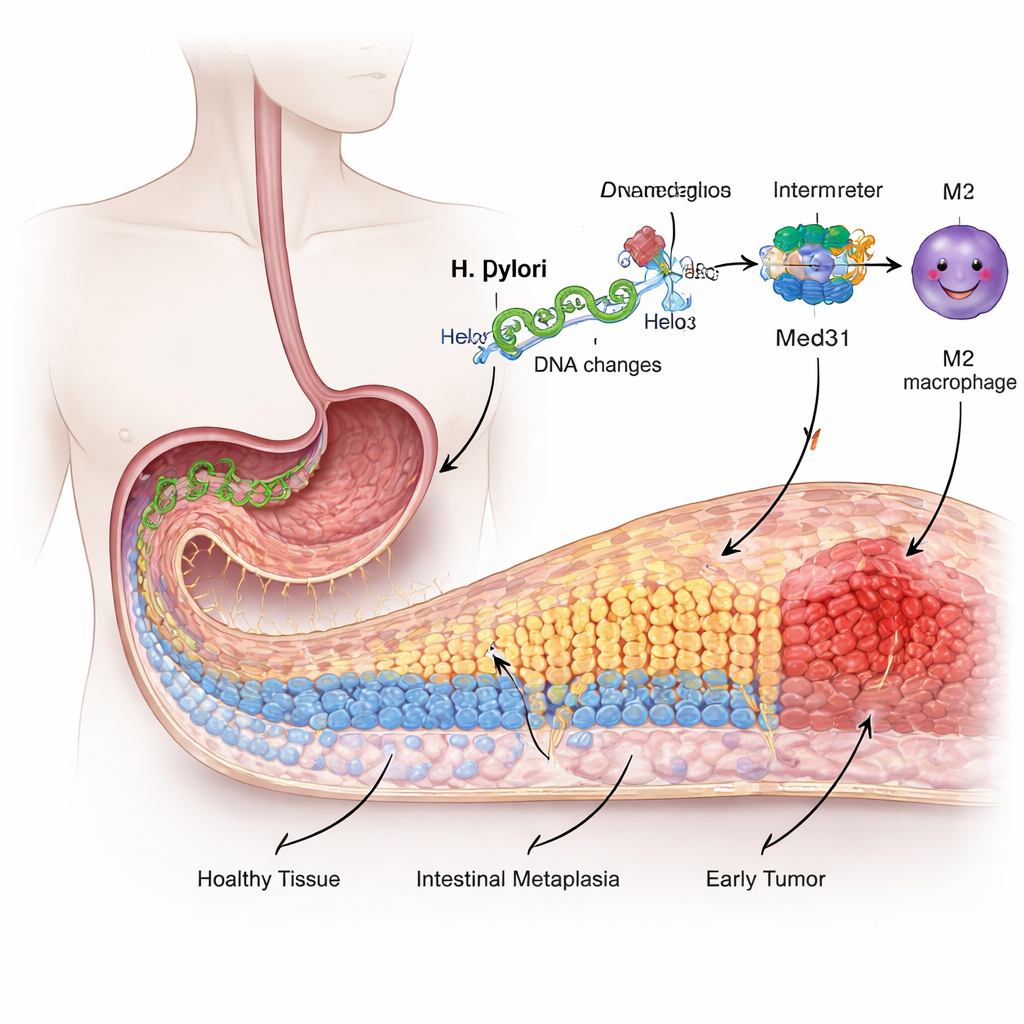
От привычной оболочки к рискованной перестройке
Внутренняя поверхность желудка выстлана специализированными клетками, приспособленными к работе в условиях сильной кислоты, а не к пищеварению, как в кишечнике. В течение многих лет раздражения и воспаления, вызванных H. pylori, часть этих клеток начинает «перестраивать» себя, приобретая признаки кишечных клеток в процессе, называемом кишечной метаплазией. Это изменение считается предраковым этапом. Исследователи использовали человеческую линию желудочных клеток, чтобы смоделировать инфекцию, и обнаружили, что воздействие H. pylori заставляло эти клетки быстрее делиться, лучше мигрировать и включать маркеры кишечного типа — все признаки того, что слизистая теряет свою нормальную идентичность.
Маленькие химические метки — большие последствия
Наша ДНК может быть помечена крошечными химическими группами — метильными группами, которые действуют как выключатели для генов, не меняя сам генетический код. Команда сосредоточилась на гене ELMO1, уже известном своей ролью в клеточном движении и распространении рака. Они показали, что инфекция H. pylori увеличивает метилирование гена ELMO1 и, что отчасти парадоксально, повышает его активность и уровни белка в желудочных клетках. Когда применяли препарат, снимающий эти метильные метки, клетки теряли многие изменения, вызванные инфекцией: они реже делились, меньше мигрировали и демонстрировали меньше признаков кишечной метаплазии. Это указывает на метилирование ELMO1 как на критический переключатель, который включает бактерия.
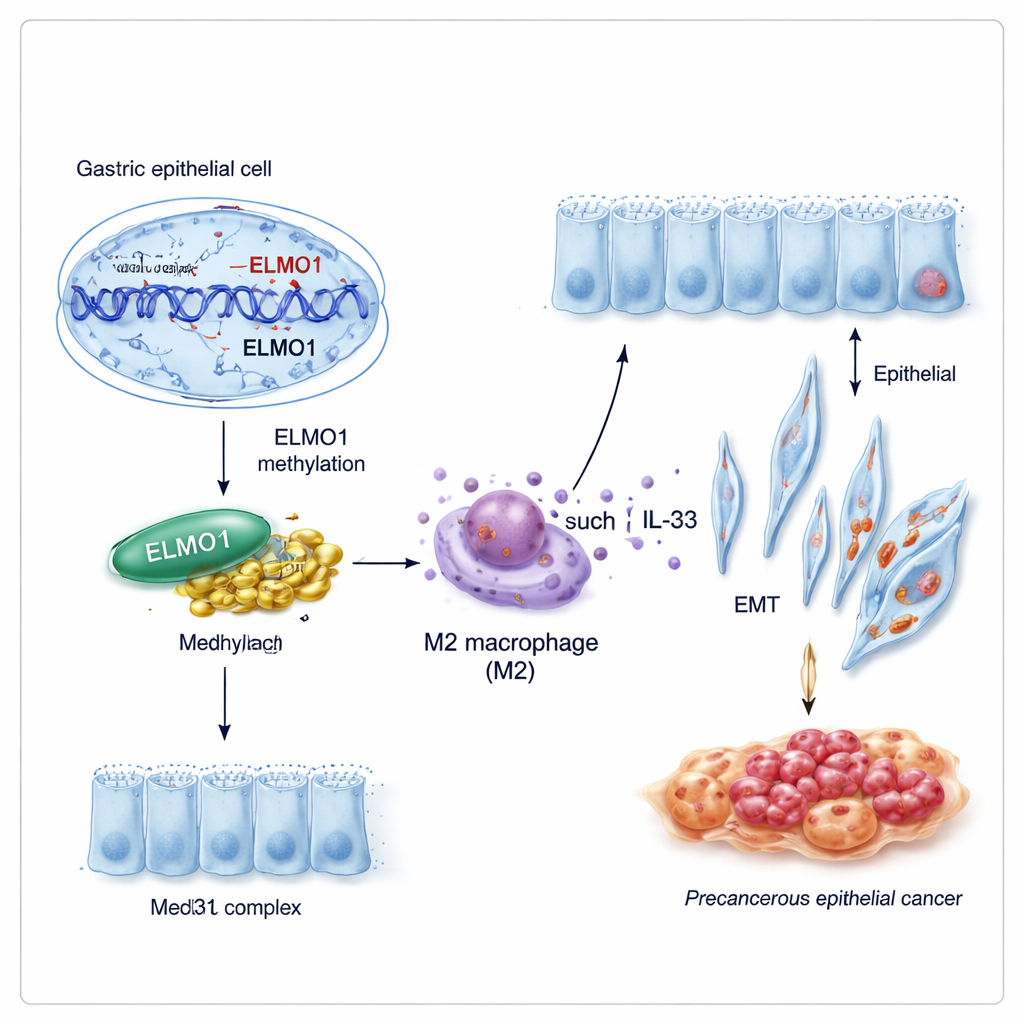
Новое партнёрство, перенастраивающее поведение клеток
Гены редко действуют в одиночку. Исследователи обнаружили, что метилированный ELMO1 способствует взаимодействию с другим белком, Med31, который входит в состав крупной «панели управления», помогающей определять, какие гены клетка включает. При условиях, способствующих метилированию ДНК, уровни ELMO1 росли, Med31 увеличивался, и оба белка физически связывались друг с другом, тогда как ранее известный партнёр ELMO1, DOCK10, отходил на задний план. Эта новая команда ELMO1–Med31, по-видимому, перенастраивает программу экспрессии генов в желудочных клетках таким образом, что стимулирует их приобретать кишечные черты и вести себя более агрессивно.
Как иммунные клетки заставляют помогать опухоли
Рак не развивается в изоляции; он растёт в сложном окружении иммунных и поддерживающих клеток. Исследование показывает, что инфицированные желудочные клетки с метилированным ELMO1 выделяют повышенные уровни IL‑33 — сигнала, который подталкивает соседние иммунные клетки, называемые макрофагами, к опухоль‑дружественному состоянию «M2». С помощью ко‑культуры авторы обнаружили, что макрофаги, подвергшиеся этим сигналам, сильно смещались в сторону типа M2 и, в свою очередь, выделяли факторы, которые побуждали свежие желудочные клетки становиться более подвижными, более инвазивными и более похожими на кишечные клетки. Маркеры эмт — эпителиально‑мезенхимального перехода, когда сидячие выстилочные клетки трансформируются в мигрирующие, способные к инвазии клетки — резко увеличивались под влиянием этих M2‑макрофагов.
Что это значит для предотвращения рака желудка
В совокупности работа описывает цепочку событий: инфекция H. pylori изменяет метилирование ДНК ELMO1, этот модифицированный ELMO1 объединяется с Med31, инфицированные клетки посылают сигналы, превращающие соседние иммунные клетки в помощников M2, и эти помощники затем способствуют как кишечной метаплазии, так и более инвазивному состоянию клеток. Для неспециалистов ключевая идея такова: обычная бактерия желудка может изменить и выстилку желудка, и местный иммунный ответ посредством обратимых химических меток на ДНК. Понимание этого пути может открыть возможности для новых тестов крови, выявляющих рискованные паттерны метилирования на ранней стадии, а также для препаратов, прерывающих ось ELMO1–Med31–M2 до того, как хроническая инфекция прогрессирует в рак желудка.
Цитирование: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Ключевые слова: гастральный рак, Helicobacter pylori, метилирование ДНК, кишечная метаплазия, микроокружение опухоли