Clear Sky Science · ru
Оценка биохимических основ устойчивости к системной амилоидозе
Когда крошечные изменения белка блокируют смертельное накопление
Многие хронические воспалительные заболевания — от ревматоидного артрита до туберкулёза — могут запускать редкое, но часто смертельное осложнение, называемое системным AA-амилоидозом. При этом состоянии обычный белок крови накапливается в виде жёстких волокон, засоряющих органы. В этом исследовании ставится удивительно обнадёживающий вопрос: могут ли небольшие, природные изменения в этом белке сделать некоторых животных в значительной степени невосприимчивыми к болезни — и если да, то как именно?
Скрытая угроза накоплений белка
AA-амилоидоз начинается с воспалительного сигнала в крови — сывороточного амилоида A (SAA). При тяжёлом или затяжном воспалении уровень SAA может возрасти в тысячи раз по сравнению с нормой. У некоторых людей и животных часть этого белка неправильно сворачивается и укладывается в длинные волокна, известные как амилоидные фибриллы, которые распространяются по органам, таким как селезёнка и почки. Со временем эти волокна нарушают работу органов. Однако не у каждого, у кого высокий уровень SAA, развивается амилоидоз, а некоторые штаммы мышей остаются удивительно устойчивыми даже при искусственном стимулировании болезни в лаборатории. Понимание причин этой устойчивости может указать пути для предотвращения амилоидных отложений у людей.
Устойчивые мыши и их особые версии белка
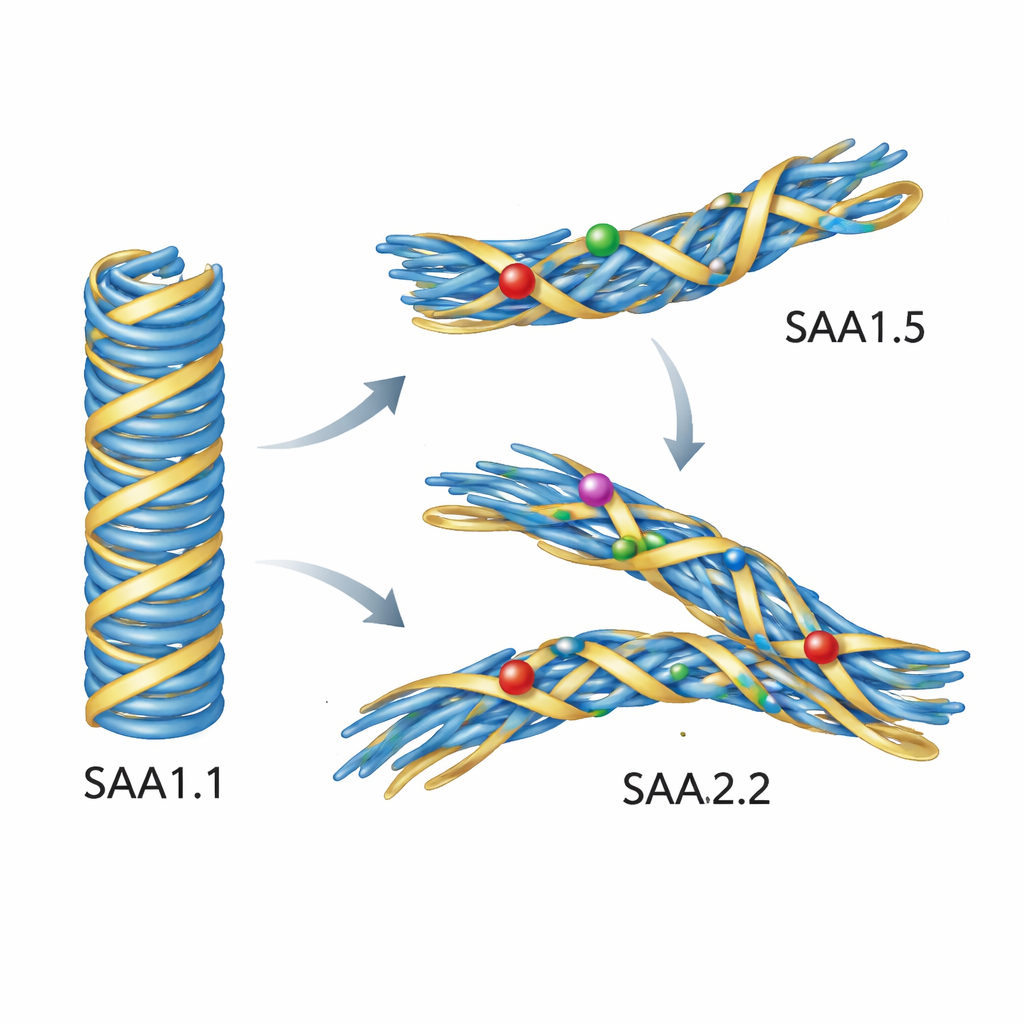
У мышей большинство AA-амилоидных фибрилл образуется из одной версии SAA, называемой SAA1.1, которая тесно связана с заболеванием. Однако некоторые штаммы преимущественно вырабатывают слегка изменённые варианты, именуемые SAA1.5 и SAA2.2, и эти штаммы редко развивают системный AA-амилоидоз. Белки отличаются всего несколькими строительными блоками (аминокислотами), но эти изменения сосредоточены в плотно упакованной области, формирующей внутреннее ядро патогенных волокон. Исследователи предположили, что эти небольшие отличия не мешают белкам вообще агрегироваться, но препятствуют им принять ту самую специфическую форму фибриллы, которая вредна.
Испытание белков в лаборатории
Чтобы проверить эту гипотезу, команда произвела все три варианта мышиного SAA в бактериях и наблюдала за их поведением в пробирочных экспериментах. Они отслеживали формирование фибрилл с помощью флуоресцентного красителя, который светится при образовании амилоида, и подтверждали структуры с помощью электронного микроскопа. SAA1.1, связанный с болезнью, легко образовывал длинные прямые волокна. SAA2.2 тоже мог образовывать фибриллы, но они были толще, сильнее закручены и структурно более разнообразны, и при этом не давали такой же сильной флуоресцентной реакции. SAA1.5, напротив, не образовывал фибрилл в тестируемых условиях. Когда учёные добавили в систему маленькие образцы реальных болезненных фибрилл, взятых из селезёнок больных мышей, в роли «затравок», SAA1.1 быстро вырастил новые волокна, которые точно копировали структуру оригинала, подобно приону. Поразительно, но SAA1.5 и SAA2.2 вообще не прирастали на эти затравки; экс виво-фибриллы не могли вовлечь их в патогенную форму.
Моделирование объясняет, почему мутантные белки отказываются принимать вредную форму
Одних экспериментов было недостаточно, чтобы показать, что именно происходит на атомном уровне, поэтому авторы обратились к детальным компьютерным симуляциям. Они взяли высокоразрешающую структуру патогенной мышиной AA-фибриллы, собранной из SAA1.1, и вычислительно подставили последовательности SAA1.5 и SAA2.2. При моделировании этих фибрилл в воде при температуре тела модель на основе SAA1.1 оставалась удивительно стабильной. В отличие от неё, фибриллы, построенные из SAA1.5 или SAA2.2, смещались и искажались. Ключевая петля в ядре выдвигалась наружу и ослабляла контакт с начальным сегментом белка, а несколько боковых цепей переворачивались в новые ориентации. Эти тонкие перестановки нарушали плотную упаковку, определяющую патогенную свёртку. Иными словами, вариантные последовательности не сопротивлялись образованию фибрилл вообще — но они не могли комфортно вписаться в «чертёж» патогенной AA-фибриллы.
Как устройство природы указывает на будущие терапии
В совокупности работа показывает, что «амилоид-устойчивые» штаммы мышей защищены не потому, что их SAA вообще не может агрегироваться. Скорее их версии SAA структурно несовместимы с той единственной формой волокна, которая вызывает системный AA-амилоидоз. Белки по-прежнему могут слипаться, но делают это в альтернативные, по-видимому, безвредные формы. Аналогичные защитные мутации известны и при других болезнях, связанных с мисфолдингом белков, включая некоторые случаи прионов и болезни Альцгеймера. Это указывает на более общий принцип: изменение белка, предрасположенного к болезни, так, чтобы он не мог принять токсичную архитектуру — при сохранении нормальной функции — может быть достаточно для предотвращения болезни. В долгосрочной перспективе терапии, вдохновлённые этими природными «устойчивыми» вариантами или короткими фрагментами, полученными из них, могли бы помочь направить белки в сторону безвредных свёрток, а не вредных.
Цитирование: Moderer, T., Schnell, A.F., Scheurmann, N.J. et al. Assessment of the biochemical basis underlying the resistance against systemic amyloidosis. Sci Rep 16, 1313 (2026). https://doi.org/10.1038/s41598-026-35297-9
Ключевые слова: AA-амилоидоз, сывороточный амилоид A, мисфолдинг белка, устойчивость к амилоидозу, модельные мыши