Clear Sky Science · ru
Никорандила ослабляет невропатическую и воспалительную боль через сигналы TNF-α, IL6/MAPKERK1/2 и NO/cGMP
Почему важно облегчать нервную боль
Миллионы людей живут с жгучей, стреляющей или покалывающей болью, которая сохраняется долго после заживления травмы. Такая «невропатическая» боль часто упорна к обычным обезболивающим и сопровождается побочными эффектами при длительном приёме лекарств. В этом обзоре рассматривается, может ли низкийник — никорандила, препарат для сердца, уже применяемый при стенокардии — смягчать чрезмерно активные болевые пути в нервной системе и каким образом он действует на клеточном уровне.
Сердечное средство в исследовании боли
Никорандила часто назначают при стенокардии, поскольку он расслабляет сосуды. Он делает это двумя основными путями: донорством небольших количеств оксида азота, сигнальной молекулы, и открытием определённых калиевых каналов в клетках. Предыдущие исследования на животных указывали, что никорандила также может уменьшать боль, воздействуя на рецепторы, участвующие в ощущении тепла и раздражении перцем чили, а также вовлекая собственную опиоидную систему организма. В настоящем исследовании учёные попытались проследить, что происходит далее по цепочке этих первичных эффектов, сосредоточившись на воспалении, оксидативном стрессе (своего рода химической «ржавчине») и специфических сигнальных путях внутри нервных клеток.
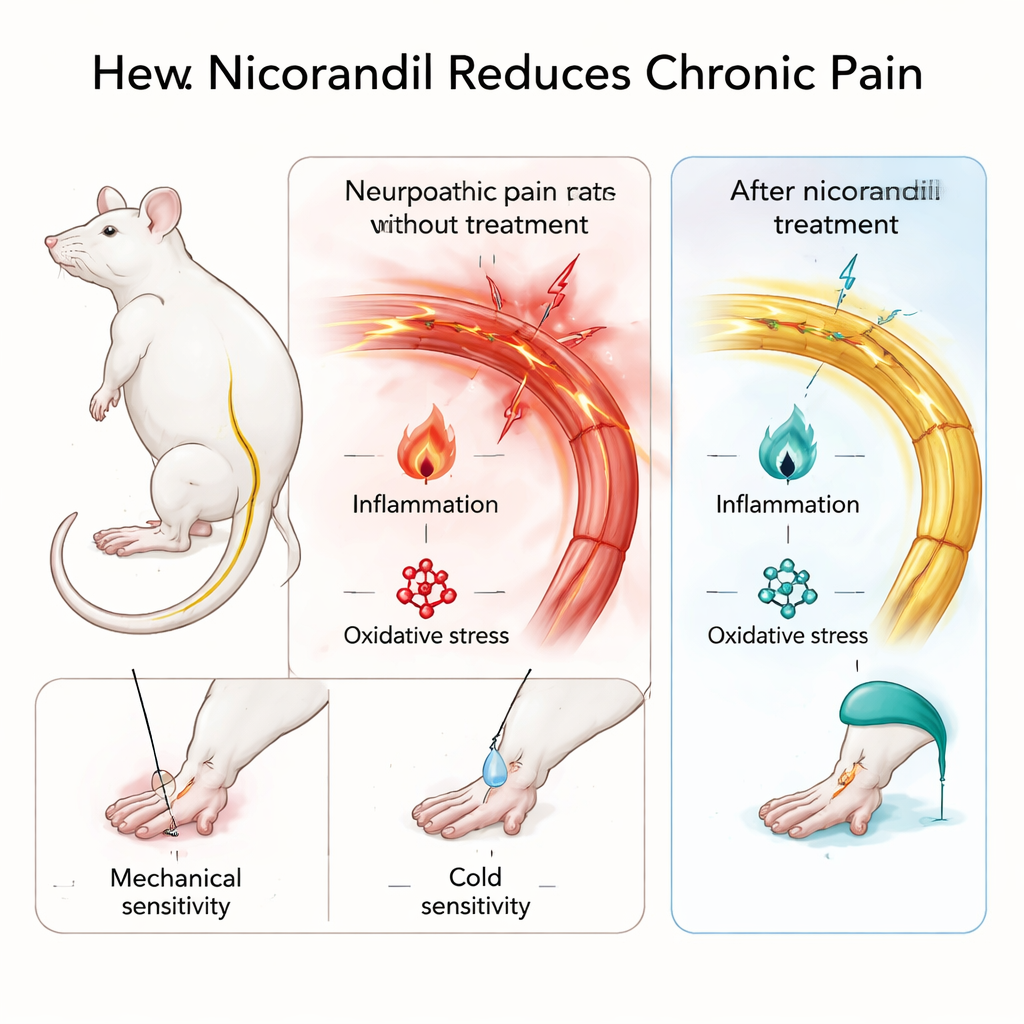
Испытания никорандила в моделях длительной боли
Чтобы воспроизвести длительную нервную боль, команда частично перевязала седалищный нерв у крыс — классическая процедура, вызывающая повышенную чувствительность к прикосновению и холоду, похожую на человеческую невропатическую боль. Также использовали тест с формалином: в лапу вводили мягкий химический раздражитель, создающий отчётливую и продолжительную воспалительную боль. Крыс кормили никорандилом в двух дозах, а исследователи измеряли реакцию на лёгкое прикосновение и холод в поражённой лапе, а также количество вылизываний и вздрагиваний после формалина. Важно, что никорандила не вызывал у животных вялости или неустойчивости в тесте на открытом пространстве, что говорит о том, что уменьшение поведенческих признаков боли не было просто следствием седативного эффекта.
Ослабление химических «сигналов тревоги»
Никорандила явно уменьшал как боль, вызванную повреждением нерва, так и боль, индуцированную формалином. Лекарство повышало порог терпимости к прикосновению и холоду и снижало число вздрагиваний и длительность вылизываний. Анализы крови показали, что никорандила снижает уровни мощных провоспалительных медиаторов — фактора некроза опухоли альфа (TNF-α) и интерлейкина-6 (IL‑6), а также циклооксигеназы‑2, фермента, участвующего в образовании простагландинов, связанных с болью. Он также уменьшал содержание малондиальдегида, маркера оксидативного стресса, что указывает на меньшее химическое повреждение клеточных мембран. Под микроскопом нервы животных, получавших никорандил, выглядели более здоровыми: наблюдалось меньше структурных повреждений и отёков в седалищном нерве и в ганглии дорсальных корешков — скоплении чувствительных нейронов.
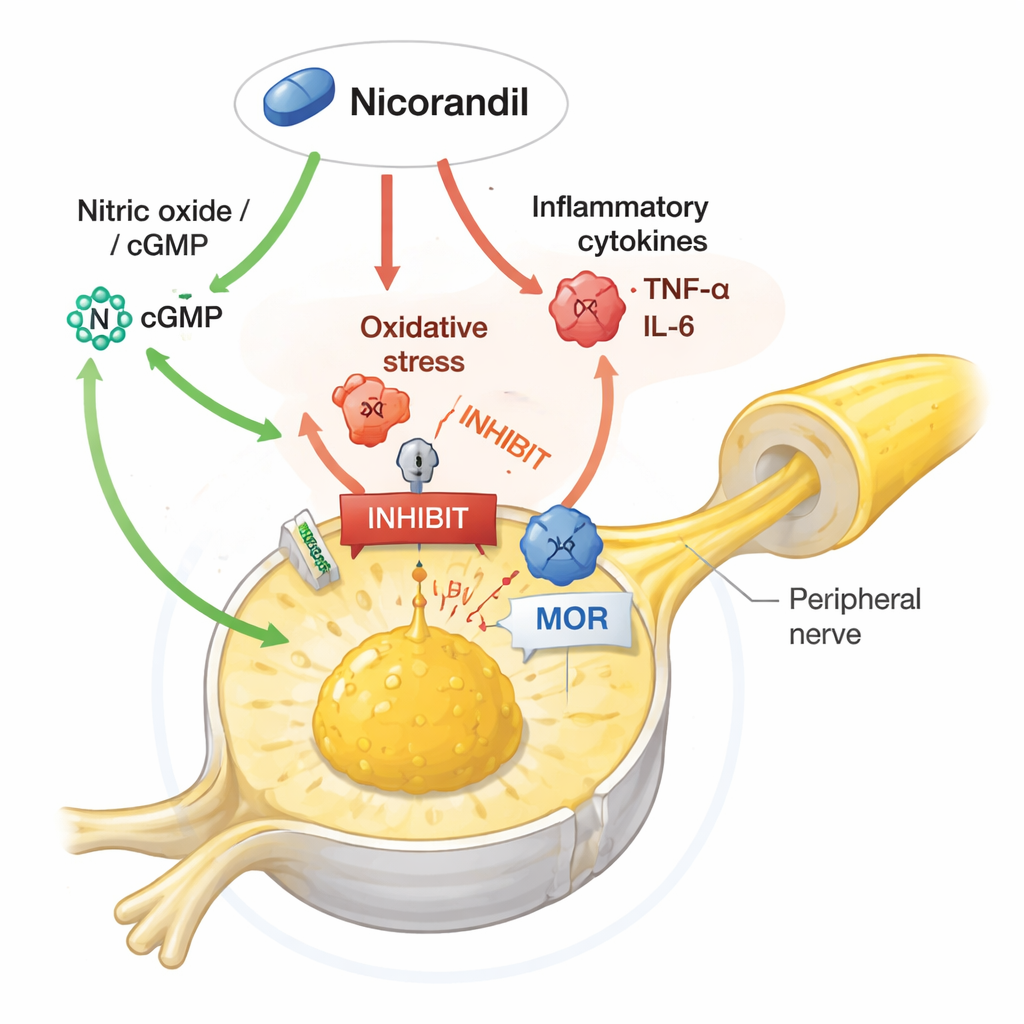
Распутывание сигнальной сети внутри болевых нервов
Исследование пошло дальше, проверяя, какие молекулярные пути необходимы для эффектов никорандила. Когда учёные вводили препараты, усиливающие действие оксида азота или повышающие уровни циклического ГМФ (молекулы‑мессенджера, связанной с оксидом азота), это частично сводило на нет способность никорандила уменьшать боль и нормализовать ключевые белки. Никорандила предотвращал обычный рост активности ERK1/2 — члена семейства MAP‑киназ, усиливающих болевые сигналы — и снижал уровни TRPV1, канала, делающего нервы более чувствительными к теплу и химическим раздражителям. Усиление сигнализации оксида азота или циклического ГМФ отменяло эти защитные изменения, тогда как блокада ферментов, синтезирующих оксид азота, иногда усиливала обезболивающий эффект никорандила. Удивительно, но блокада калиевых каналов, которые известны как мишень никорандила, не устраняла его антинокицептивного действия, что указывает на то, что в данном контексте обезболивающий эффект больше зависит от модуляции оксида азота, оксидативного стресса, воспаления и опиоидной сигнализации, чем от классического сосудистого механизма.
Что это может значить для людей с болью
В совокупности результаты представляют никорандил как многоцелевой модулятор боли: он успокаивает чрезмерно активные нервные пути, уменьшая окислительное повреждение и провоспалительные медиаторы, подавляя ERK1/2 и TRPV1 в чувствительных нейронах и взаимодействуя с сигнализацией оксида азота и собственной опиоидной системой организма. Поскольку эти данные получены на крысах и при краткосрочном приёме, требуется дальнейшая работа на людях, чтобы определить безопасные дозы, долгосрочные эффекты и подтвердить, действуют ли те же защитные механизмы в человеческих нервах.
Цитирование: Badr, R.M., Abuiessa, S.A., Elblehi, S.S. et al. Nicorandil ameliorates neuropathic and inflammatory pain via TNF-α, IL6/MAPKERK1/2 and NO/cGMP signaling. Sci Rep 16, 4722 (2026). https://doi.org/10.1038/s41598-026-35272-4
Ключевые слова: невропатическая боль, никорандила, воспаление, окислительный стресс, сигнализация оксида азота