Clear Sky Science · ru
Гены, связанные с деубиквитинированием, определяют иммунные подтипы колоректального рака и связаны с прогнозом и сигнатурами, релевантными для иммунотерапии
Почему это исследование важно для людей
Колоректальный рак — один из самых распространённых и смертоносных видов рака в мире, при этом опухоли, похожие под микроскопом, могут давать очень разные результаты и по прогнозу, и по ответу на современные методы лечения, такие как иммунотерапия. Это исследование задаёт новый вопрос: можно ли лучше разделить колоректальные раки на группы, изучая, как опухолевые клетки управляют «переработкой» белков, и как это связано с иммунной защитой организма? Ответ может помочь врачам точнее прогнозировать исход заболевания и в будущем разрабатывать более умные комбинации терапий.
Уборка белков и поведение рака
Внутри каждой клетки изношенные или повреждённые белки помечаются и перерабатываются, чтобы они не накапливались и не вызывали проблем. Одна ветвь этой системы — деубиквитинирование — удаляет эти метки и помогает точно регулировать, какие белки уничтожаются, а какие сохраняются. Авторы собрали большие публичные наборы данных о опухолях кишечника и здоровой ткани и просканировали тысячи генов, чтобы найти те, которые связаны и с этой системой очистки белков, и с выживаемостью пациентов. Они сократили список до 17 ключевых генов, тесно связанных с контролем деления клеток, восстановлением повреждений ДНК и структурой внеклеточного матрикса. Эти гены стали основой новой схемы группировки колоректальных раков.
Выделяются два основных типа опухолей
Используя закономерности активности в этих 17 генах, исследователи разделили опухоли на два основных подтипа. Пациенты в одной группе, как правило, жили дольше и имели заболевание на ранних стадиях. Другая группа отличалась худшим прогнозом. При более широком анализе включённых и выключенных генов в каждом подтипе выяснилось, что группа с худшим исходом демонстрировала сильные маркёры быстрого клеточного роста, реакций на повреждение ДНК и активной перестройки внеклеточного матрикса. Напротив, группа с лучшим прогнозом имела менее агрессивную ремоделировку и более сбалансированные признаки роста и восстановления клеток.
Окружение опухоли и иммунный ответ
Рак не растёт в изоляции; он живёт в окружении иммунных клеток, опорных клеток и рубцующейся ткани. Исследование использовало вычислительные инструменты для оценки состава иммунных клеток в каждой опухоли. Два подтипа продемонстрировали резко отличающиеся иммунные ландшафты. Подтип с плохим прогнозом был обогащён плотным коллагеном и фиброзной тканью, создающими физический и химический барьер, который может не пропускать Т‑клетки, борющиеся с раком. Он также нес сигналы иммунного подавления и имел более высокие показатели, предсказывающие устойчивость к иммунотерапии. Подтип с лучшим прогнозом характеризовался меньшим накоплением матрикса, более благоприятными соотношениями иммунных клеток, такими как цитотоксические и вспомогательные Т‑клетки, и показателями, указывающими на большую потенциальную чувствительность к иммунотерапии.
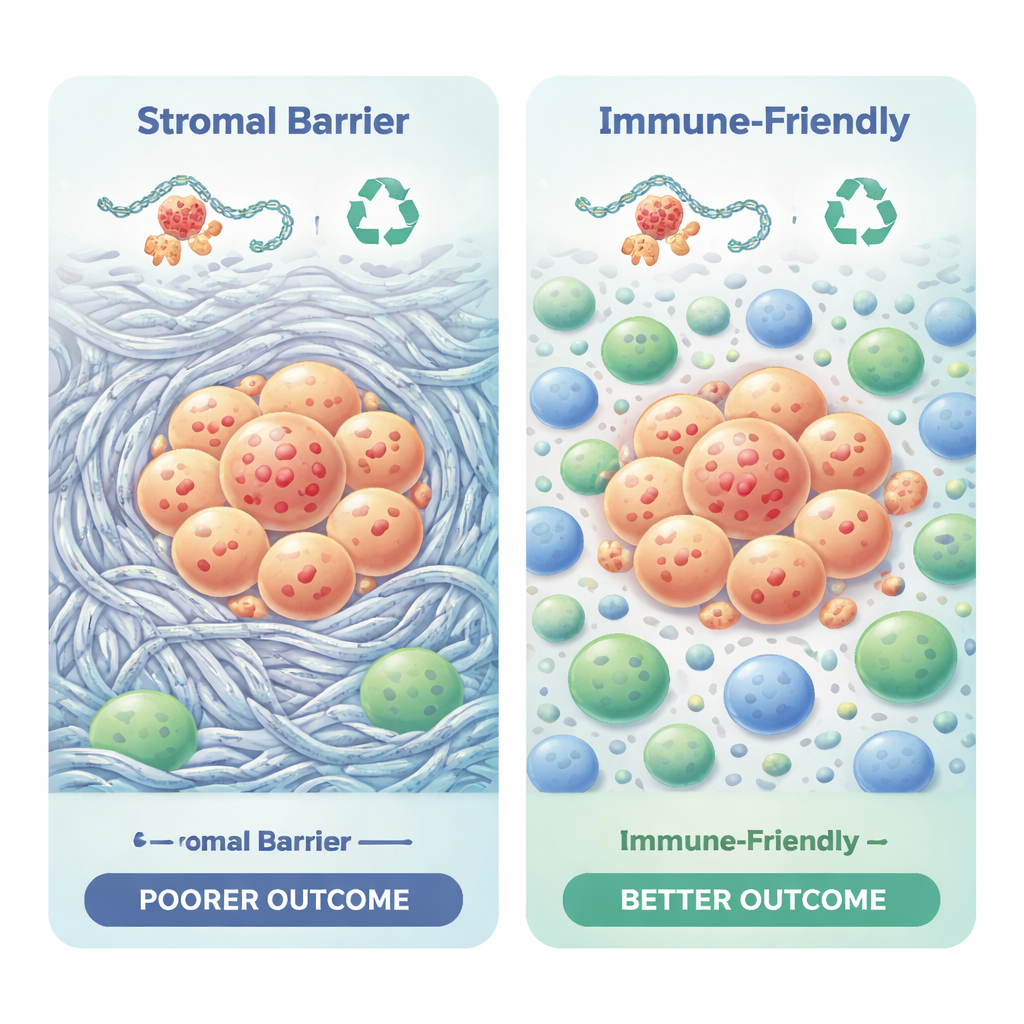
Ключевые структурные гены как предупредительные маячки
Чтобы перейти от общих закономерностей к практическим маркёрам, авторы построили сети взаимодействующих белков и искали центральные «хаб‑»гены. Они выделили девять генов, в основном участвующих в построении и ремоделировке внеклеточного матрикса опухоли, включая несколько коллагенов и такие молекулы, как фибронектин и периостин. Высокая активность некоторых из этих генов, особенно BGN, FN1 и POSTN, последовательно ассоциировалась с худшей выживаемостью в двух независимых когортах пациентов. Эти центральные гены находятся на пересечении механической жёсткости, химической сигнализации и привлечения иммунных клеток, что делает их перспективными кандидатами для будущих тестов, которые могли бы помочь предсказывать риск или направлять выбор терапии.
Что это значит в дальнейшем
Эта работа пока не меняет подходы к лечению пациентов, поскольку основана на вычислительном анализе существующих данных, а не на новых клинических испытаниях. Тем не менее, она даёт ясный вывод для неспециалистов: то, как колоректальная опухоль управляет переработкой белков и перестраивает своё локальное окружение, похоже, влияет на то, сможет ли иммунная система добраться до неё и атаковать. Опухоли с сильно нарушённым контролем белков и плотной фиброзной «раковиной» чаще отпугивают иммунные клетки и связаны с худшими исходами, тогда как опухоли с меньшим рубцеванием и более открытым доступом для иммунных клеток имеют лучшие результаты. В будущем комбинации препаратов, нацеленных на восстановление ДНК или на фиброзный матрикс, в сочетании с иммунотерапией могут оказаться особенно полезными для высокорисковой группы, выделенной в этом исследовании.
Цитирование: Xu, Y., Mo, Z., Jiang, Q. et al. Deubiquitination-related genes define immune subtypes of colorectal cancer and are associated with prognosis and immunotherapy-related signatures. Sci Rep 16, 4862 (2026). https://doi.org/10.1038/s41598-026-35271-5
Ключевые слова: колоректальный рак, опухолевый микроокружение, иммунные подтипы, распад белков, иммунотерапия