Clear Sky Science · ru
Нарушение гомеостаза цинка снижает уровни ацетилирования гистонов в нормальных и опухолевых клетках
Когда полезный металл становится вредным
Цинк прежде всего известен как питательное вещество в поливитаминах, которое помогает иммунной системе и заживлению ран. Но внутри клеток цинк должен поддерживаться в очень узком «золотом» диапазоне. В этом исследовании показано, что при слишком высоких уровнях цинка клетки могут тихо отключать важные гены, уплотняя упаковку ДНК, и даже сдвигать клетки в сторону самоперерабатывающегося процесса, называемого аутофагией. Поскольку добавки с цинком, ингредиенты против перхоти и экспериментальные противораковые препараты могут изменять уровни цинка, понимание этой скрытой системы контроля важно как для повседневного здоровья, так и для будущих терапий.
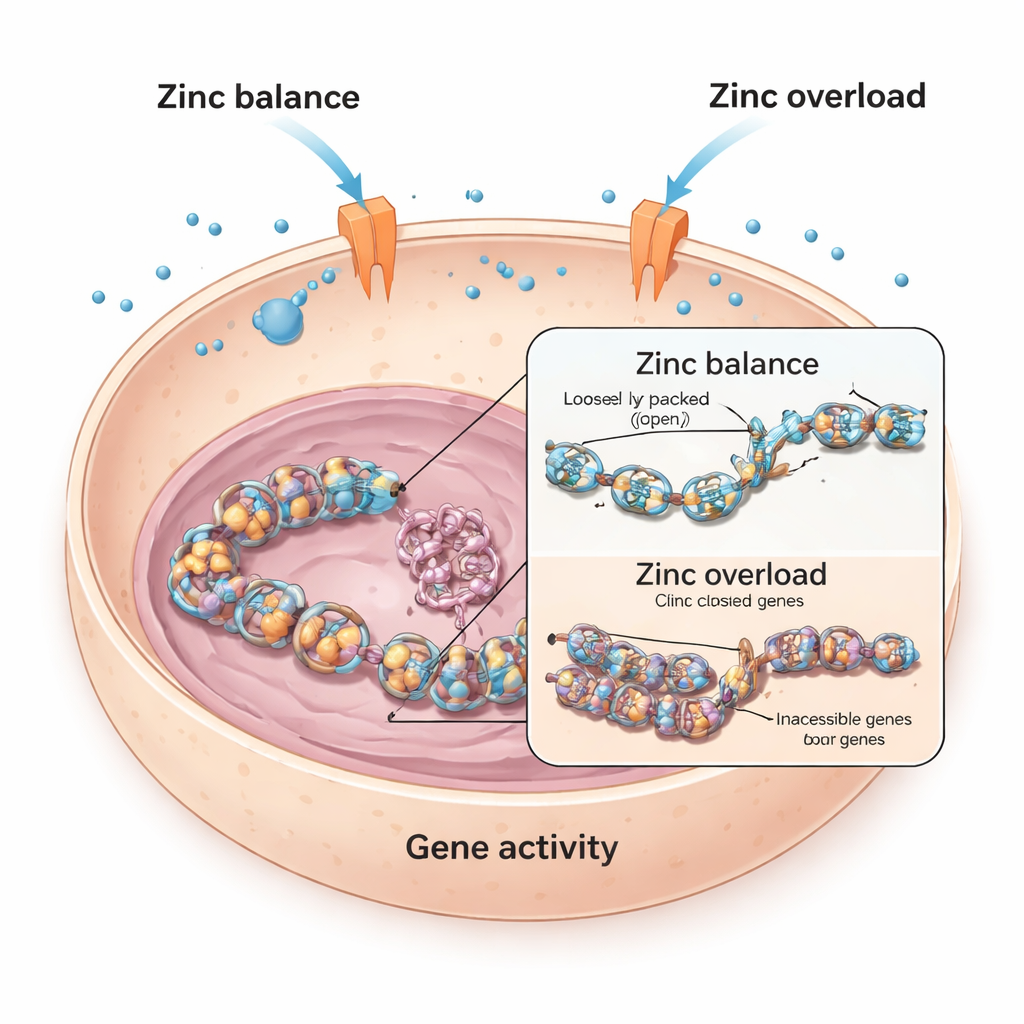
Баланс цинка внутри живых клеток
Каждая клетка нуждается в цинке, который помогает тысячам белков выполнять свои функции. Чтобы избежать как дефицита, так и перегруза, клетки используют специальные «ворота» в мембранах, называемые транспортерами цинка, чтобы перемещать цинк внутрь и наружу. Исследователи начали с сердечных мышечных клеток мышей и человека, задавшись вопросом, что происходит при воздействии дополнительного цинка. Они обнаружили, что в мышиных сердечных клетках высокий уровень цинка резко снижал активность ключевого гена, связанного с сердцем, под названием Bmp4, который участвует в развитии и функции сердца. Напротив, человеческие сердечные клетки были гораздо меньше подвержены этому влиянию, что указывает на то, что разные клетки по‑разному защищаются от перегруза цинком.
Как цинк уплотняет упаковку ДНК
Чтобы выяснить, как цинк заглушает гены вроде Bmp4, команда изучала гистоны — белки, вокруг которых наматывается ДНК. Когда к гистонам присоединяются небольшие химические метки — ацетильные группы, — ДНК становится более рыхлой и легче читаемой; при удалении этих меток ДНК уплотняется, и гены труднее включить. В исследовании показано, что избыток цинка в мышиных сердечных клетках приводил к снижению ацетилирования гистонов в конкретной позиции (известной как H3K9), что строго коррелировало с падением активности Bmp4. Препараты, блокирующие гистондеацетилазы, могли обратить эффект цинка и восстановить Bmp4, что указывает на то, что цинк смещает баланс этой системы химических меток.
Слишком много цинка внутри, а не только снаружи
Ключевым оказался цинк в водной цитоплазме клетки, а не только в окружающей среде. С использованием флуоресцентного зонда, который светится при наличии свободного цинка, исследователи заметили всплеск внутриклеточного цинка в мышиных сердечных клетках после обработки. Когда они использовали переносчик цинка, чтобы прямо ввести цинк в клетки, наблюдалось то же снижение ацетилирования гистонов и активности генов, даже при гораздо низших концентрациях цинка в окружающей среде. У человеческих сердечных клеток, напротив, транспортеры в мембране быстро отрегулировались: некоторые белки, ввозящие цинк, отключались, а выносящие — усиливались, что предотвращало значительный рост внутреннего цинка и защищало ацетилирование гистонов. Мышиные сердечные клетки продемонстрировали более «сбивающуюся» работу транспортеров, позволившую цинку сильнее проникать и нарушать контроль генов.
От регуляции генов до самопереработки в нормальных и опухолевых клетках
Затем исследователи проверили, уникально ли это цинком‑индуцированное уплотнение упаковки ДНК для сердечных клеток. Они протестировали несколько типов нормальных человеческих клеток и опухолевые линии из желудка, матки и яичников. Когда цинку позволяли накапливаться внутри с помощью переносчика, почти все эти клетки демонстрировали явное снижение ацетилирования гистонов. В некоторых опухолевых клетках, например в клетках рака желудка, это происходило при особенно низких дозах цинка, что указывает на повышенную чувствительность некоторых опухолей к дисбалансу цинка. Команда также связала падение ацетилирования с аутофагией — процессом, при котором клетки перерабатывают изношенные компоненты. Умеренное увеличение внутриклеточного цинка усиливало аутофагию, тогда как очень высокий уровень цинка в конце концов ослаблял её, что предполагает узкое окно, в котором цинк может тонко регулировать этот путь самопереработки.
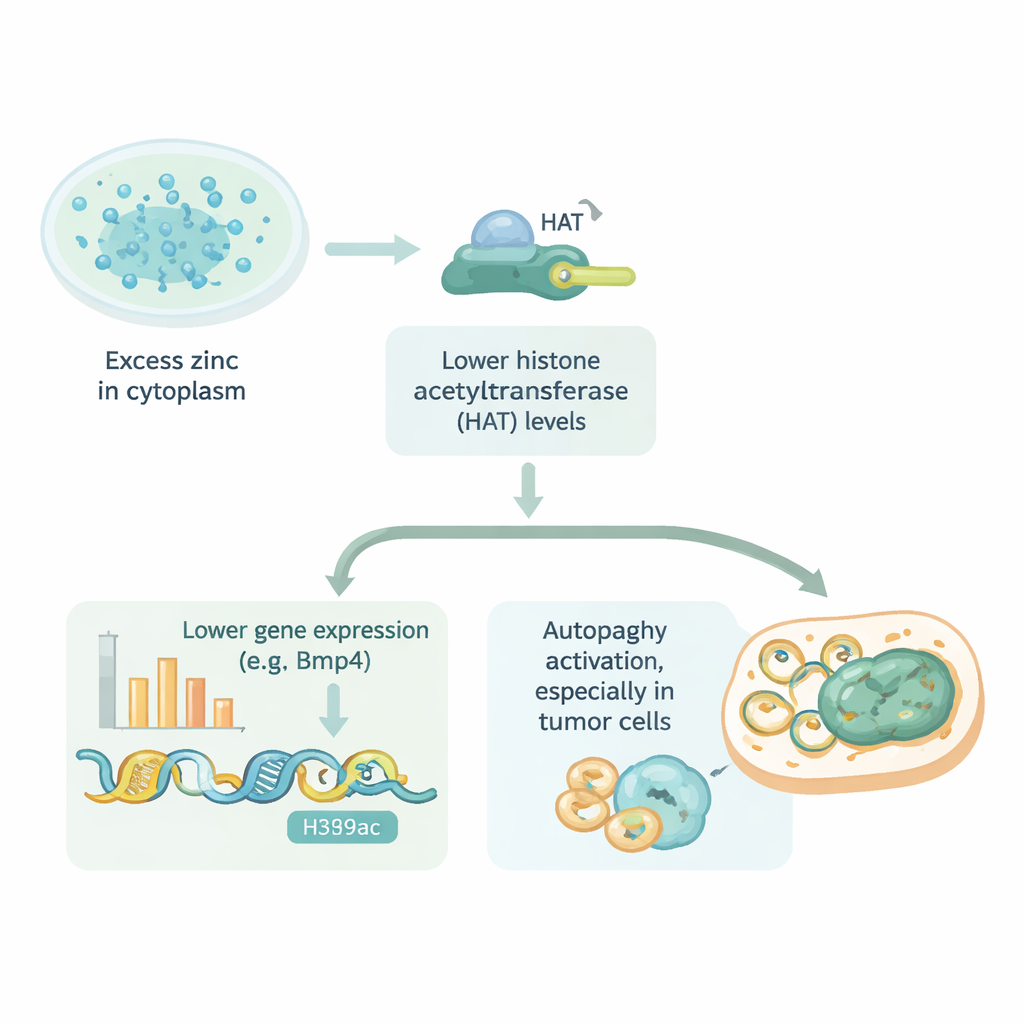
Что это значит для здоровья и лечения
Проще говоря, эта работа показывает, что избыток цинка внутри клеток может приглушать гены, делая ДНК менее доступной, и что тот же путь влияет на активность клеточной самопереработки. Эффект не ограничен сердечными клетками; он прослеживается в разных нормальных и опухолевых клетках, хотя некоторые лучше защищаются от перегруза цинком, чем другие. Эти выводы указывают на то, что крошечные «ворота» транспортёров цинка в мембранах клеток могут быть перспективными мишенями для лекарств — либо для защиты здоровых тканей от повреждений, связанных с цинком, либо для того, чтобы подтолкнуть уязвимые опухолевые клетки к гибели. Хотя результаты получены на клеточных культурах, они дают новое представление о том, как повседневный микронутриент может формировать активность генов и болезни при нарушении его тонкого баланса.
Цитирование: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Ключевые слова: гомеостаз цинка, регуляция генов, ацетилирование гистонов, аутофагия, раковые клетки