Clear Sky Science · ru
Метаболическая перенастройка повышает устойчивость к окислительному стрессу при дифференцировке кардиомиоцитов
Почему битва сердечных клеток с кислородом важна
Каждый удар вашего сердца зависит от специализированных мышечных клеток — кардиомиоцитов. В процессе развития эти клетки переживают драматическое изменение: они переходят от низкооксигенной, сахаро-обеспеченной среды в утробе к богатой кислородом среде после рождения. Кислород необходим, но он также порождает вредные побочные продукты, которые могут повреждать ДНК и убивать клетки. В этом исследовании изучается, как созревающие сердечные клетки перенастраивают свой метаболизм, чтобы выдерживать повышенное содержание кислорода, производить больше энергии и при этом защищать себя от окислительного повреждения — выводы, которые могут помочь в разработке будущих методов лечения заболеваний сердца и регенерации.
От простых строителей к энергетическим атлетам
Незрелые сердечные клетки, называемые кардиомиобластами, — это мелкие делящиеся клетки, которые в основном получают энергию за счёт расщепления глюкозы. По мере дифференцировки в зрелые кардиомиоциты они прекращают деление и увеличиваются в размерах, часто сливаясь в полинуклеированные, вытянутые клетки, лучше приспособленные для мощного сокращения. С помощью высокоразрешающей микроскопии исследователи наблюдали эту трансформацию в течение десяти дней в лабораторной клеточной модели. Маркеры пролиферации клеток снижались, а клетки растягивались и реорганизовывались в волокнистые структуры, похожие на ткань сердца, что подтверждало их переход в более взрослое, сократительное состояние. 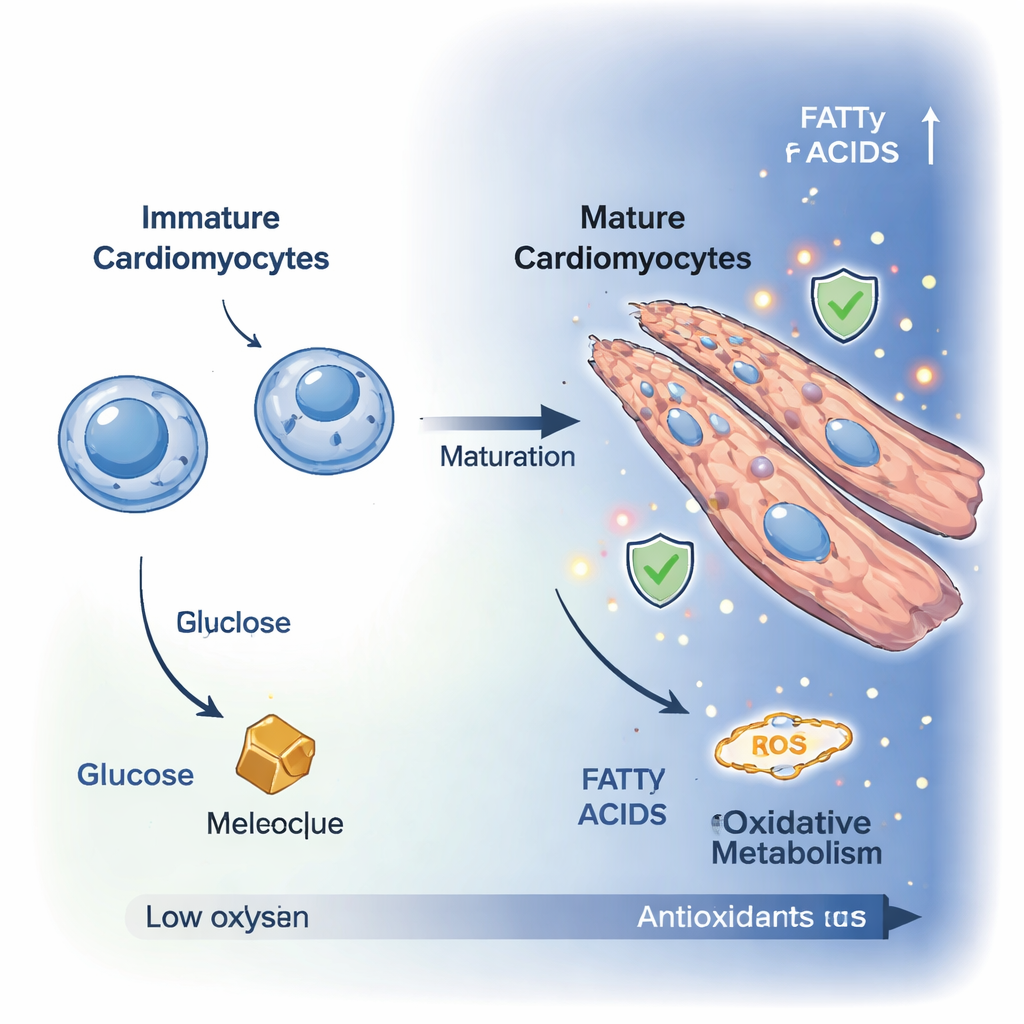
Смена топлива и прокладка новых энергетических путей
Чтобы понять, что происходит «под капотом», команда измеряла сотни малых молекул внутри клеток и использовала продвинутую визуализацию естественной флуоресценции клеток для отслеживания использования энергии в реальном времени. Вместе эти методы показали очевидный сдвиг от гликолитического состояния, в котором клетки в основном сжигают глюкозу, к окислительному состоянию, доминирующему за счёт митохондриального дыхания. Уровни глюкозы и фруктозы снижались, тогда как промежуточные метаболиты трикарбоновой кислоты (TCA), такие как лимонная кислота, малат и оксоглутарат, увеличивались. Анализ путей выявил усиление активности маршрутов, которые подают топливо в митохондрии, включая малат–аспартатный шаттл и распад аминокислот, что указывает на то, что зрелые кардиомиоциты расширяют спектр используемого топлива и более эффективно направляют энергию в свои «электростанции».
Жизнь с большим количеством кислорода — и большим стрессом
Более эффективное сжигание топлива в митохондриях имеет свою цену: повышенное образование реактивных форм кислорода (ROS) — химически активных молекул, способных повреждать липиды, белки и ДНК. Исследователи обнаружили, что по мере созревания кардиомиоцитов митохондрии становились крупнее и более вытянутыми, а маркеры окислительного стресса повышались. Флуоресцентная визуализация выявила больше гранул, похожих на липофусцин — признак окисленных липидов, а ядерный зонд показал повышенные уровни ROS в дифференцированных клетках. Метаболомика указала на изменения в метаболизме глутатиона — ключевой антиоксидантной системы, которая использует молекулу глутатион, собранную из аминокислот, таких как глутамат и глицин, для нейтрализации ROS. Эти результаты позволяют предположить, что по мере увеличения окислительного метаболизма сердечные клетки также настраивают свои антиоксидантные пути, чтобы сдерживать повреждения. 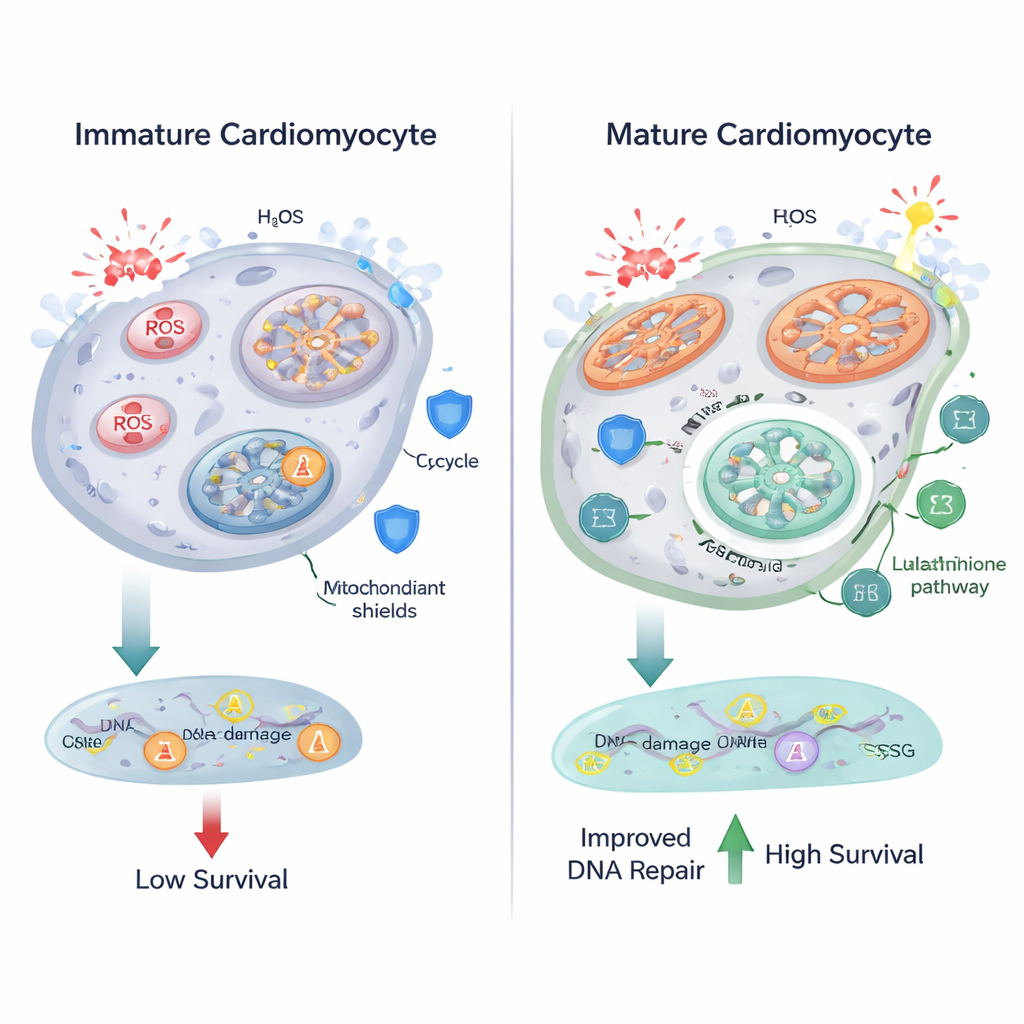
Повреждения локализованы, защиты усилены
Что удивительно, несмотря на более высокие уровни ROS, дифференцированные кардиомиоциты не проявляли большего числа разрывов ДНК по сравнению с незрелыми клетками при измерении по очагам γ-H2AX — чувствительному маркеру повреждения ДНК. Когда команда подвергала клетки воздействию перекиси водорода, мощного окислителя, и незрелые, и зрелые клетки накапливали ROS и разрывы ДНК — но зрелые клетки переносили это лучше. Они демонстрировали пропорционально меньшее число поражений ДНК относительно их более высоких уровней ROS, с меньшей склонностью к активации сигналов, связанных с гибелью клеток, таких как PUMA, и заметно более высокими показателями выживаемости. Эти результаты указывают на то, что мaturing кардиомиоциты не только корректируют свой метаболизм, но и укрепляют механизмы репарации ДНК и выживания, позволяя им выдерживать более суровые окислительные условия.
Что это значит для защиты сердца
Проще говоря, это исследование показывает, что по мере взросления сердечные клетки учатся работать интенсивнее, не «перегорев». Они переключаются с сахарозависимого, низкооксигенного образа жизни на кислородно-ориентированный режим, управляемый митохондриями, и одновременно строят более прочные щиты и команды по ремонту, чтобы справляться с окислительным стрессом. Понимание этого тонко настроенного баланса между производством энергии и самозащитой может помочь ученым разработать стратегии, которые сделают поврежденную ткань взрослого сердца более устойчивой, или направлять стволовые клетки в более безопасные и долговечные кардиомиоциты для регенеративной терапии.
Цитирование: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Ключевые слова: дифференцировка кардиомиоцитов, окислительный стресс, митохондрии, клеточный метаболизм, заболевания сердца