Clear Sky Science · ru
Удаление гликозилирования вызывает новую дистальную конформацию маннозного рецептора CD206
Почему сахарные покрытия на иммунных сенсорах имеют значение
Наши иммунные клетки полагаются на молекулярные «антенны» для обнаружения угроз, таких как микробы и раковые клетки. Одна из таких антенн, называемая маннозным рецептором CD206, помогает иммунным клеткам захватывать молекулы, украшенные сахарными цепями, и даже нацеливаться на опухоли. Как и многие белки, сам CD206 покрыт короткими сахарными цепочками. В этом исследовании ставится, на первый взгляд, простой, но важный вопрос: что происходит с формой и функцией CD206, когда эти сахара удаляют?
Гибкая «рука», считывающая сахарные сигналы
CD206 располагается на поверхности определённых иммунных клеток, особенно макрофагов, патрулирующих ткани и опухоли. Он имеет длинную, шарнирную структуру, выступающую от мембраны клетки и завершающуюся несколькими «лектиновыми» сегментами, которые распознают сахара на проходящих молекулах. CD206 также может отсоединяться и попадать в кровоток, где его концентрация коррелирует с воспалительными и фиброзными заболеваниями, что делает его потенциальным маркером болезни. Белок сильно гликозилирован связями N‑типа; ранние исследования показали, что эти сахарные цепи могут влиять на то, насколько эффективно разные сегменты рецептора распознают сахара. Многие сайты гликозилирования находятся далеко от основных карманов связывания, что наводит на мысль, что они действуют скорее как отдалённые переключатели, а не простые заграждения.
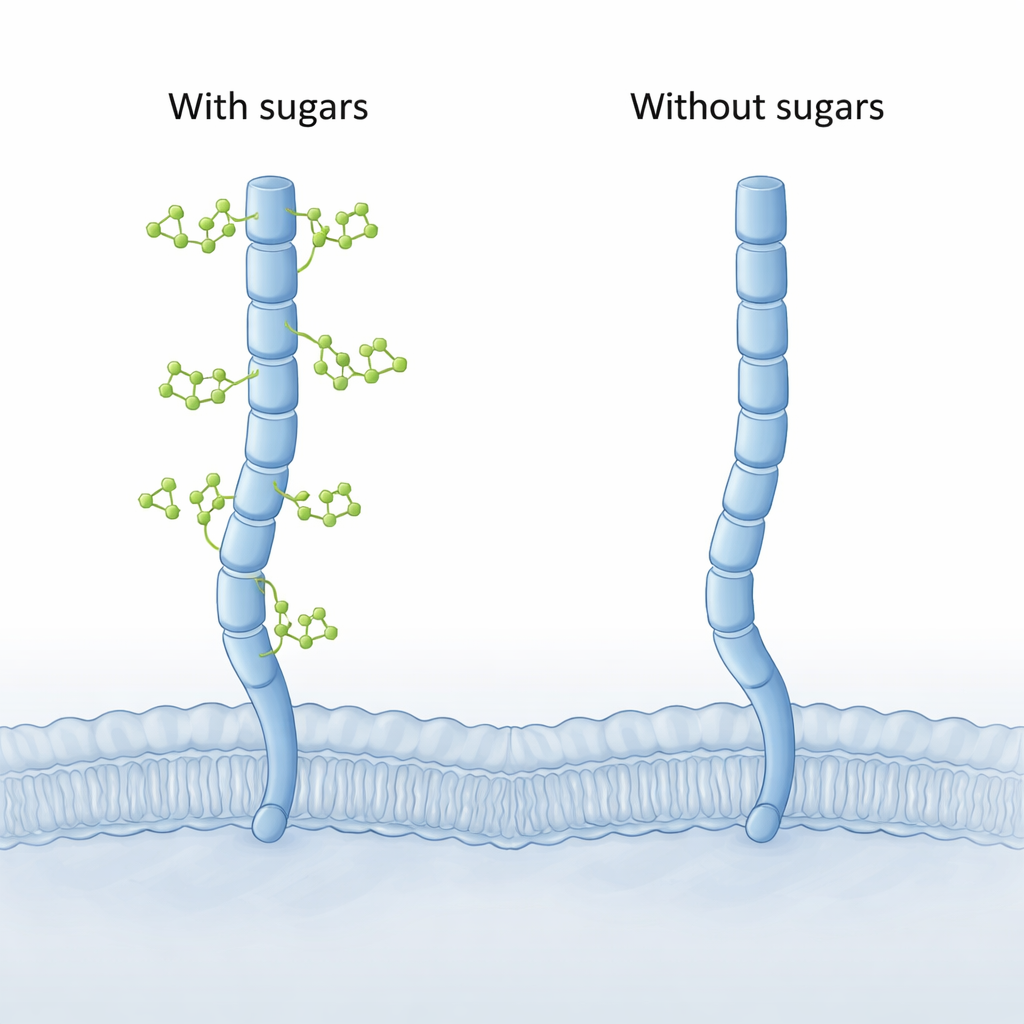
Компьютерные модели выявляют скрытый изгиб
Поскольку полная трёхмерная структура CD206 ещё не получена экспериментально, авторы использовали современные вычислительные инструменты. Сначала они применили AlphaFold для построения полноразмерных моделей рецептора, затем провели длительные детальные симуляции молекулярной динамики CD206 с прикреплёнными сахарными цепями и без них. Обе версии вели себя как вытянутая молекулярная «рука», но форма «безсахарной» версии продемонстрировала поразительное новое движение на своём далёком конце. Последние два лектиновых сегмента (обозначенные CTLD7 и CTLD8) могли заходить внутрь и формировать вогнутую, согнутую внутрь вершину — форму, никогда не наблюдавшуюся в гликозилированной версии, которая оставалась более выпуклой, или изогнутой наружу.
Как небольшое изменение перестраивает движение
Чтобы понять эту разницу, команда проанализировала доминирующие движения в своих симуляциях. Они обнаружили, что ключевое отличие между двумя формами — это именно изгиб дистального конца, и что он проявляется только при отсутствии сахаров. Удаление сахаров в целом сделало рецептор более гибким, особенно в дистальных лектиновых сегментах и, в меньшей степени, вблизи N‑терминального конца. Карты корреляции движений разных частей белка показали, что без сахаров последние два лектина движутся более согласованно и сильнее связаны с другими областями. По существу, сахара не просто лежат на поверхности; они помогают тонко настраивать, как вся «рука» сгибается и как по ней передаётся взаимодействие между сегментами.
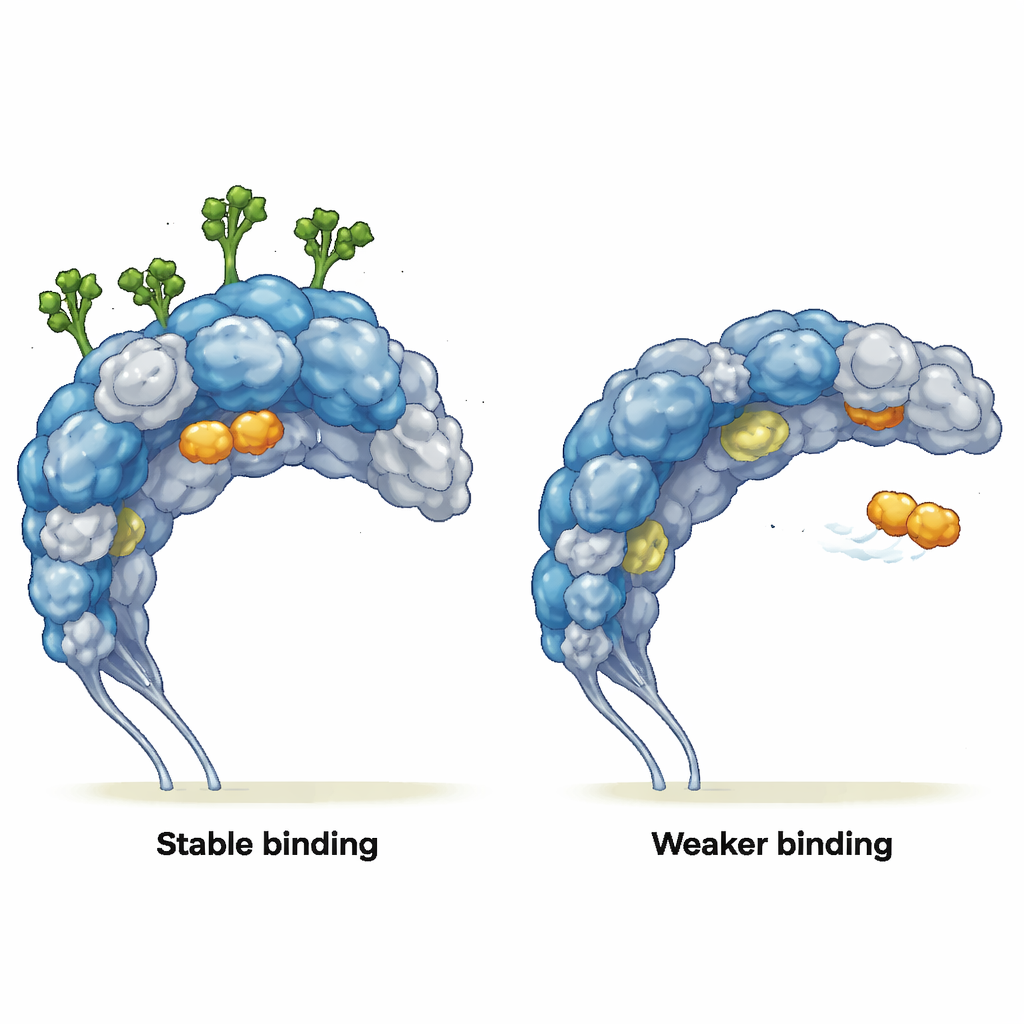
Изменение способов связывания партнёров
Затем авторы спросили, как это изменённое движение влияет на реальные молекулы‑партнёры. Они смоделировали взаимодействия с двумя лигандами: простым маннозоподобным сахаром (MMA), который помещается в чётко определённый карман, и пептидом, нацеленным на опухоли, называемым mUNO, который ориентирован на CD206‑положительные макрофаги, ассоциированные с опухолью. В гликозилированной версии MMA оставался плотно в своём кармане на протяжении всей симуляции, сохраняя ключевые контакты, хотя соседняя структура белка почти не менялась. Без сахаров MMA покидал карман, скользя по поверхности белка и образуя только кратковременные поверхностные контакты. Для mUNO гликозилированный рецептор демонстрировал несколько стабильных поз связывания с частыми длительными контактами. В дегликозилированном рецепторе связывание mUNO было слабее и более рассеяно; он также начал исследовать участки, которые обычно блокируются сахарными цепями, раскрывая новые, ранее скрытые сайты взаимодействия.
Что это значит для болезни и терапии
В совокупности эти результаты показывают, что сахара, присоединённые к CD206, действуют как отдалённые регуляторы его формы и липкости. Ограничивая определённые изгибы и организуя согласованные движения сегментов, гликозилирование помогает рецептору крепче удерживать некоторые лиганды и направлять другие к предпочитаемым точкам докинга, одновременно скрывая участки своей поверхности. В таких заболеваниях, как рак, где общие узоры гликозилирования белков часто изменены, CD206 может принимать иные формы и режимы связывания, меняя то, как иммунные клетки ощущают окружение. Понимание этого зависящего от сахаров «конформационного переключателя» не только проясняет механизм работы CD206, но и указывает новые пути для разработки лекарств или контрастных агентов, использующих изменяющийся ландшафт рецептора в опухолях и других патологических состояниях.
Цитирование: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Ключевые слова: маннозный рецептор, гликозилирование белков, распознавание иммунитетом, макрофаги, ассоциированные с опухолью, молекулярная динамика