Clear Sky Science · ru
Потеря Snhg5 нарушает регуляцию клеточного цикла, не меняя кистообразования в мышиной модели поликистозной болезни почек
Почему ген с загадочным названием важен
Поликистозная болезнь почек (ПКБ) — распространённое наследственное заболевание, при котором многочисленные заполненные жидкостью мешочки постепенно захватывают почки и часто приводят к почечной недостаточности. Учёным известно, что дефекты в двух генах, PKD1 и PKD2, вызывают заболевание, но многие другие генетические факторы могут влиять на скорость его прогрессирования. В этом исследовании изучается необычный тип гена — длинная некодирующая РНК под названием Snhg5, задавая простой, но важный вопрос: действительно ли эта молекула существенно влияет на развитие ПКБ, или же она в основном наблюдатель?
Более пристальный взгляд на малоизвестный генетический мессенджер
В отличие от обычных генов, дающих инструкции для белков, длинные некодирующие РНК действуют скорее как молекулярные организаторы или переключатели внутри клеток. Ранее было показано, что Snhg5 сильно повышен в мышиных моделях ПКБ и связан с несколькими видами рака и повреждениями почек, что наводит на мысль о его возможной роли в патогенном росте. Исследователи сначала проследили, где и когда активен Snhg5 в нормальных мышах. Они обнаружили, что он включён во многих органах, особенно высокие уровни отмечены в кишечнике, а его активность в почке резко снижается после рождения, когда орган переходит от быстрого роста к более стабильному зрелому состоянию. Внутри почечных клеток почти все молекулы Snhg5 локализуются в ядре, командном центре с ДНК, что указывает на роль Snhg5 в регулировании активности генов, а не в синтезе белков напрямую.
Шаблоны в больных почках не дают полного ответа
Затем команда сравнила уровни Snhg5 в ряде мышиных моделей ПКБ. В быстро прогрессирующих моделях, где кисты формируются стремительно, Snhg5 увеличивался в 2–3 раза в поражённых почках, а визуализация на уровне отдельных клеток показала сильный ядерный сигнал в клетках, выстилающих кисты, и в прилежащих тканях. Удивительно, что в более медленной, мягкой модели, лучше имитирующей длительное течение человеческой ПКБ, Snhg5 не повышался. Ещё более поразительно, что в тканях почек людей с прогрессирующей аутосомно-доминантной ПКБ человеческий аналог гена, называемый SNHG5, был фактически снижен более чем на 90 процентов. В совокупности эти данные указывают, что изменения этой РНК сопровождают формирование кист, но направление и временные рамки изменения различаются между видами и стадиями болезни, что ставит под сомнение роль Snhg5 как простого драйвера роста кист.
Что происходит при удалении гена
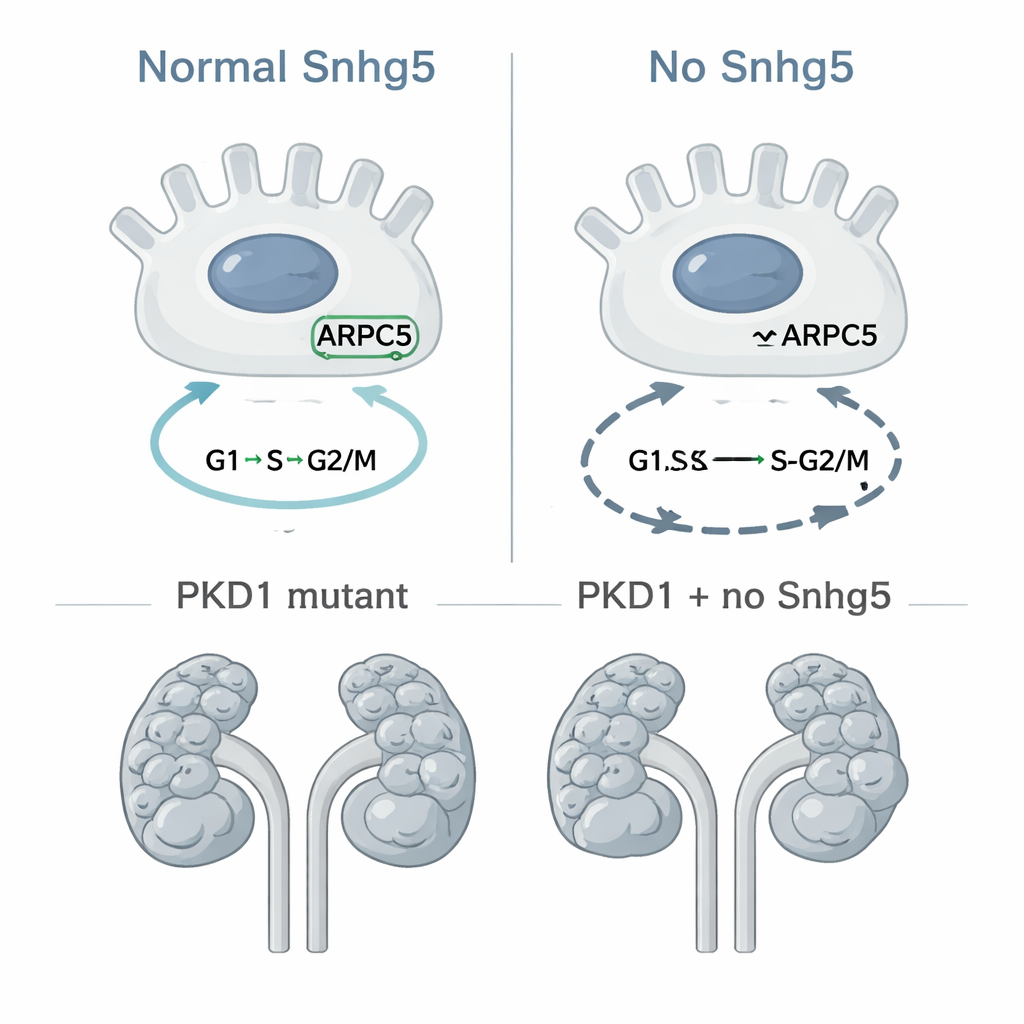
Чтобы выйти за рамки корреляции, исследователи использовали редактирование генома CRISPR для полного удаления гена Snhg5 у мышей, создав глобальную «нокаутную» линию. Вопреки опасениям, что удаление такой сильно изменённой молекулы может быть вредным, мыши без Snhg5 рождались в нормальных пропорциях, жили обычной продолжительностью и имели почки, которые выглядели и функционировали как у их здоровых сиблинг-противоположностей. Микроскопическое исследование показало нормальную структуру почки без рубцевания или воспаления, а анализ крови не выявил признаков нарушения фильтрации. На молекулярном уровне, однако, выявились более тонкие изменения: и в почках мышей, и в культивируемых клетках почечных канальцев без Snhg5 наблюдались устойчивые сдвиги в активности генов, связанных с делением клетки и репликацией ДНК. В культурах клеток больше клеток застревало на поздних стадиях клеточного цикла и в повреждённом состоянии sub-G1. В частности, один белок, ARPC5, часть комплекса, помогающего клеткам делиться за счёт перестройки внутреннего каркаса, был снижен при отсутствии Snhg5, что наводит на возможную цепочку причинно-следственных связей.
Прямое тестирование роли в росте кист
Поскольку неконтролируемое деление клеток является ключевой чертой ПКБ, команда затем проверила, замедлит ли удаление Snhg5 образование кист в хорошо зарекомендовавшей себя мышиной модели, где ген PKD1 отключён специфически в клетках собирательных протоков — источнике многих кист. Они скрещивали мышей так, чтобы у одних была только мутация PKD1, а у других отсутствовали и PKD1, и Snhg5. При осмотре животных на 10-й день жизни обе группы имели выраженные кистозные почки, а тщательные измерения размеров почек, площади кист и их количества не выявили значимой защиты от удаления Snhg5. Если и было отличие, то двунаследственные мутанты имели слегка большую кистовую нагрузку, хотя разница была небольшой и статистически недостоверной. Иными словами, несмотря на влияние Snhg5 на гены клеточного цикла в почечных клетках, его отсутствие заметно не меняет скорость появления или увеличения кист в этой конкретной модели ПКБ.
Что это означает для будущих методов лечения
Для пациентов и разработчиков лекарств главный вывод в том, что Snhg5, несмотря на то что является одним из наиболее значительно изменённых молекулярных сигналов в мышином ПКБ, не является краеугольным камнем кистообразования — по крайней мере на ранней, быстрорастущей фазе заболевания, происходящего из собирательных протоков. Ген, по-видимому, тонко настраивает прохождение клетками почки через цикл деления, вероятно через влияние на такие факторы, как ARPC5, но это влияние настолько слабое, что полная его потеря оставляет развитие почек и раннее прогрессирование ПКБ в основном неизменными. Эти результаты подчёркивают более общую мысль: не каждое заметное молекулярное изменение в больной ткани — перспективная терапевтическая мишень. Чтобы отличить причину от следствия, потребуется тестирование длинных некодирующих РНК, подобных Snhg5, на множестве моделей заболевания и на различных этапах, прежде чем их можно будет уверенно рассматривать как кандидатов в лекарственные цели.
Цитирование: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
Ключевые слова: поликистоз почек, длинная некодирующая РНК, Snhg5, клеточный цикл, кисты почек