Clear Sky Science · ru
Нанокапсулы на основе хитозана и декстрансульфата для повышения эффективности тигециклина против нетифоидных Salmonella enterica
Почему это важно для безопасности пищевых продуктов
Большинство людей считает Salmonella неприятной причиной пищевого отравления, часто связанной с недожаренной птицей. Мало кто осознаёт, что некоторые штаммы стали настолько устойчивыми к антибиотикам, что даже мощные «последние средства» могут оказаться бессильны. В этом исследовании изучается нанотехнологический подход, который позволяет «спасти» один из таких препаратов — тигециклин — поместив его в крошечные капсулы на основе сахаров, что помогает препарату проникать в инфицированные клетки и подавлять ключевые механизмы устойчивости у Salmonella.
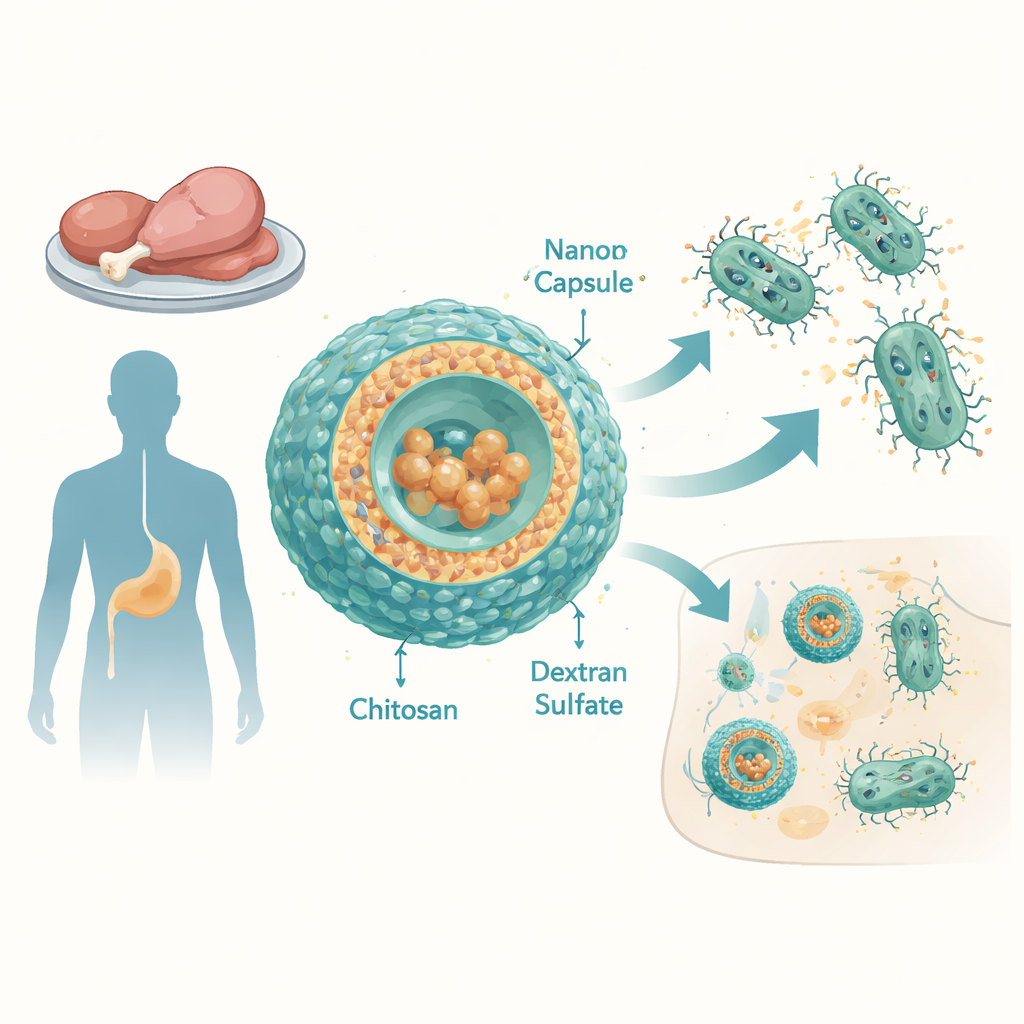
Растущая угроза со стороны устойчивых Salmonella
НетИфоидные серовары Salmonella (NTS) — одна из ведущих причин диареи и бактериемии в мире, особенно в странах с низким и средним доходом. Исследователи проанализировали 12 штаммов Salmonella enterica, выделенных из куриного и утино-го мяса в Египте. Эти штаммы были резистентны ко многим широко используемым антибиотикам, включая пенициллины, цефалоспорины, тетрациклины и другие, и демонстрировали высокие показатели множественной антибиотикорезистентности. Даже тигециклин, широкоспектровый препарат, зарезервированный для тяжёлых случаев, проявлял слабую активность: бактерии выдерживали очень высокие его концентрации. Основной причиной были гиперактивные «эффлюксные насосы» — молекулярные комплексы в мембране бактерий, постоянно выкачивающие антибиотики обратно наружу.
Создание «умной» лекарственной капсулы
Чтобы преодолеть это, команда разработала нановокапсулы из двух природных полимеров: хитозана, получаемого из хитина (входящего в состав панцирей ракообразных), и декстрансульфата, ветвящегося полисахарида. Тщательно подобрав соотношение компонентов, они получили стабильные частицы диаметром примерно 100–150 нанометров с положительным поверхностным зарядом, что способствует их взаимодействию с мембранами бактерий и клеток хозяина. Тигециклин был загружен в эти частицы с удивительно высокой эффективностью — практически весь препарат оказался внутри капсул. В лабораторных тестах, имитирующих условия крови, капсулы высвобождали большую часть тигециклина в течение нескольких часов, что указывает на способность доставлять мощный всплеск антибиотика в очаги инфекции.
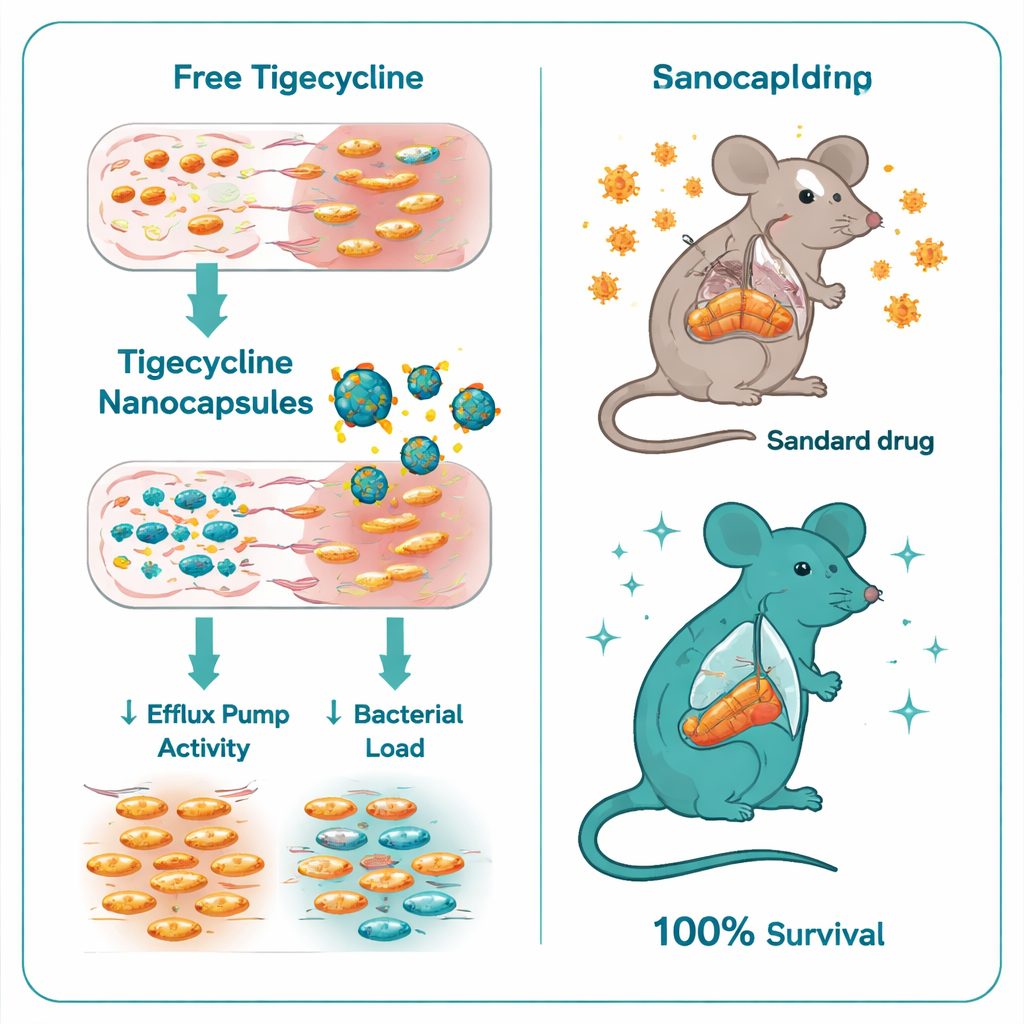
Ослабление защитных механизмов бактерий
При сравнении обычного тигециклина и тигециклина в хитозан–декстрансульфатных нанокапсулах разница оказалась поразительной. Минимальная концентрация препарата, необходимая для остановки роста бактерий, снизилась с 32–128 микрограмм на миллилитр для свободного тигециклина до всего 0,5–1 микрограмма на миллилитр при использовании нанокапсул — улучшение в шесть–семь раз. Эксперименты по времени гибели показали, что инкапсулированная форма убивает Salmonella значительно быстрее и эффективнее. На генетическом уровне нанокапсулы также подавляли ключевые регуляторы резистентности: экспрессия генов ramA и acrB, контролирующих и формирующих основные эффлюксные насосы, уменьшалась в несколько раз в обработанных бактериях. Иными словами, капсулы не просто доставляли больше препарата; они помогали выключить один из основных путей бегства бактерий.
Защита инфицированных мышей от летального исхода
Далее команда протестировала новую форму в модели тяжёлой инфекции Salmonella Typhimurium у мышей. Все инфицированные мыши без лечения погибли в течение восьми дней. Мыши, получавшие стандартный тигециклин, переносили инфекцию лучше, но смертность оставалась высокой — выжило лишь 40%. В резком контрасте все мыши, получавшие тигециклин в нанокапсулах, выжили. У этих животных значительно уменьшалось количество бактерий в печени и кишечнике, анализы крови ближе к норме по функциям печени и почек, а при микроскопическом исследовании тканей обнаруживалось гораздо меньше повреждений. Даже «пустые» хитозан–декстрансульфатные капсулы без антибиотика обеспечивали некоторую защиту, вероятно, за счёт умеренных антибактериальных и противовоспалительных свойств хитозана, но сочетание с тигециклином было явно более эффективным.
Что это может значить для будущих лечений
Для неспециалистов главный вывод таков: упаковка существующего антибиотика в «умную», биосовместимую нанокапсулу может вернуть ему эффективность против высокоустойчивых штаммов Salmonella. Помогая препарату добираться до бактерий, прячущихся внутри клеток, и снижая активность насосов, которые обычно выталкивают препарат, система хитозан–декстрансульфата превратила затруднённый препарат последней линии в высокоэффективное средство у мышей с 100% выживаемостью. Хотя прежде чем применять этот подход у людей или сельскохозяйственных животных потребуется дополнительная работа, он предлагает перспективный путь для продления срока службы важных антибиотиков и повышения безопасности продовольствия без необходимости изобретать полностью новые препараты с нуля.
Цитирование: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Ключевые слова: Сальмонелла, резистентность к антибиотикам, наночастицы, доставка лекарств, тигециклин