Clear Sky Science · ru
Генетические полиморфизмы в гене репарации ДНК XRCC1 и риск диабетической полинейропатии
Почему мелкие изменения в ДНК важны для людей с диабетом
Для многих людей с сахарным диабетом 2 типа первым признаком проблем являются не показания лаборатории по глюкозе, а покалывание, жжение или онемение в стопах и руках. Это состояние, называемое диабетической полинейропатией, может приводить к боли, потере равновесия и даже ампутации конечностей. Однако не все пациенты с диабетом развивают это осложнение, даже при схожих уровнях сахара. В этом исследовании поставили простой, но важный вопрос: могут ли небольшие наследственные различия в гене репарации ДНК объяснять, кто находится в группе повышенного риска, и может ли современная обработка данных помочь врачам выявлять таких людей раньше?
Ближе к механизму поражения нервов при диабете
Диабетическая полинейропатия развивается, когда длинные нервы, особенно в ногах и ступнях, постепенно повреждаются в течение многих лет под влиянием высокого уровня глюкозы, нарушенного кровотока и хронического «окислительного» повреждения клеток реактивными формами кислорода. Эти молекулы могут разрушать ключевые компоненты клеток, включая ДНК. Клетки не остаются беззащитными: у них есть механизмы ремонта, которые постоянно устраняют такие повреждения. Один из таких инструментов — белок, кодируемый геном XRCC1, который помогает восстанавливать однобреточные разрывы ДНК. Если эта система ремонта работает хуже, нервные клетки могут хуже выдерживать постоянный стресс при диабете, что увеличивает вероятность и тяжесть повреждений нервов.
Что проверяли исследователи на примере египетских пациентов
Команда исследовала 732 взрослых в Египте: 503 с сахарным диабетом 2 типа и 229 здоровых добровольцев. Среди больных диабетом примерно у половины уже были признаки поражения нервов, а у половины — нет. Ученые сосредоточились на двух распространённых «орфографических» вариантах в гене XRCC1, известных как Arg399Gln и Arg194Trp. Эти крошечные изменения, называемые однонуклеотидными полиморфизмами, заменяют один строительный блок белка XRCC1 на другой и могут менять эффективность его репаративной функции. С помощью стандартных генетических тестов на образцах крови исследователи определяли, какие варианты в этих участках были у каждого человека, а затем сопоставляли эти генетические профили с наличием и тяжестью нервных нарушений.
Генетические сочетания, связанные с более высоким риском поражения нервов
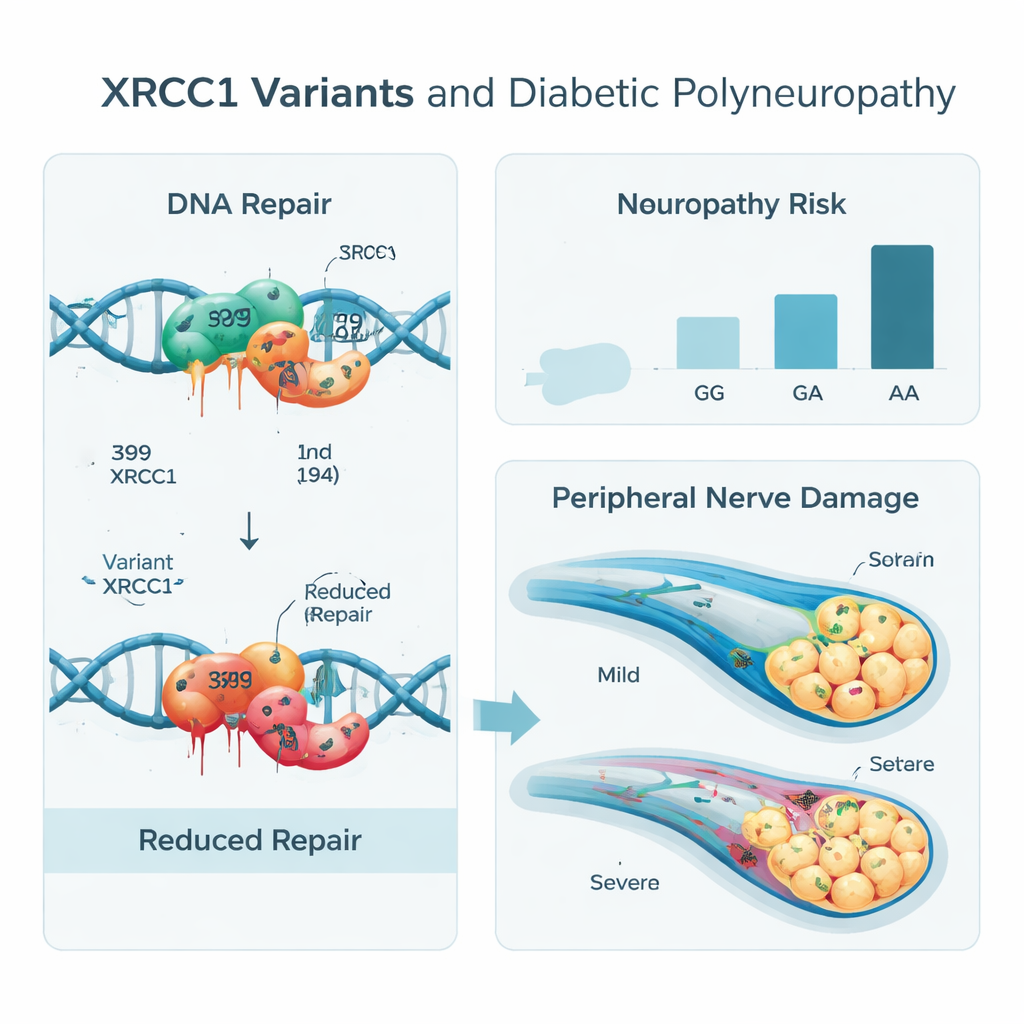
Результаты показали очевидную картину. Пациенты с диабетом, у которых были менее распространённые варианты XRCC1 — форма A в позиции 399 и форма T в позиции 194 — чаще имели повреждение нервов, чем носители обычных вариантов. В частности, у лиц с двумя копиями A в позиции 399 вероятность нейропатии была в несколько раз выше, чем у носителей двух копий G, даже с учётом возраста, пола и курения. Аналогично, наличие хотя бы одной копии T в позиции 194 повышало риск. Рассмотрение двух позиций совместно в виде гаплотипов выявило одну комбинацию (A–T), особенно связанную с риском нейропатии, тогда как другие сочетания, несмотря на наличие одного «рискованного» нуклеотида, выглядели защищающими, что указывает на более сложные взаимодействия между генами.
Как машинное обучение уточнило картину
Чтобы выйти за рамки простых сравнений, исследователи обратились к машинному обучению — разделу искусственного интеллекта, который умеет одновременно анализировать множество переменных. С помощью алгоритмов Random Forest и XGBoost они обучали модели на 80% данных и тестировали на оставшихся 20%. Эти модели выделили не только варианты XRCC1, но и традиционные клинические факторы — более длительную историю диабета, более высокий уровень натощак глюкозы и «плохого» LDL‑холестерола, более низкий уровень «хорошего» HDL, старший возраст и более высокий индекс массы тела — в качестве ключевых предикторов нейропатии. Инструмент объяснения моделей SHAP помог визуализировать, как каждый фактор повышает или снижает риск конкретного пациента. Команда также сравнила две клинические шкалы для оценки нейропатии, показав, что Toronto Clinical Neuropathy Score лучше отражает тяжесть заболевания по сравнению со старой шкалой инвалидности.
Что это означает для пациентов и профилактики
Проще говоря, исследование предполагает, что некоторые люди с сахарным диабетом 2 типа наследуют менее устойчивый набор инструментов для ремонта ДНК, из‑за чего их нервы становятся более уязвимыми к износу при высоком уровне сахара и нарушениях липидного обмена. Эти наследственные различия в гене XRCC1, по-видимому, не вызывают диабет сами по себе, но смещают шансы в сторону развития болезненных и инвалидизирующих поражений нервов у тех, кто уже болеет. Комбинируя простые анализы крови, клинические измерения, шкалы оценки состояния нервов и генетическую информацию в умных компьютерных моделях, врачи в будущем смогут раньше выявлять пациентов высокой группы риска и адаптировать последующее наблюдение и лечение — строгий контроль сахара и липидов, изменение образа жизни и нейропротективные терапии — до того, как разовьются серьёзные повреждения нервов.
Цитирование: Hashim, N.A., El-Baz, H.A., Afya, Z.I.A. et al. Genetic polymorphisms in DNA repair gene XRCC1 and the risk of diabetic polyneuropathy. Sci Rep 16, 4815 (2026). https://doi.org/10.1038/s41598-026-35213-1
Ключевые слова: диабетическая нейропатия, репарация ДНК, XRCC1, генетический риск, машинное обучение