Clear Sky Science · ru
Интегрированные протеомика и метаболомика показывают, что фитосесквитерпеновые лактоны ингибируют активность клеток ТНБК за счёт истощения синтеза АТФ и перепрограммирования первичного обмена веществ
Растительные соединения, лишающие питание агрессивный рак молочной железы
Тройственно‑негативный рак молочной железы — одна из самых трудноизлечимых форм рака молочной железы, поскольку он лишён обычных гормональных «ручек», к которым привыкли прицеливаться многие препараты. В этом исследовании изучаются две молекулы, извлечённые из лекарственного растения, которые, по-видимому, выключают внутренние электростанции этих раковых клеток, отрезая их от источника энергии при относительно небольшом вреде для нормальных клеток молочной железы. Понимание механизма действия могло бы открыть путь к более мягким и целенаправленным терапиям для пациентов, у которых сейчас ограничен выбор.
Почему важно нацеливаться на источник энергии рака
Каждая клетка зависит от крошечных структур — митохондрий — для производства АТФ, основного топлива клетки. Раковые клетки, особенно агрессивные, часто необычно зависят от митохондрий, чтобы поддерживать быстрый рост, метастазирование и выживание при стрессе. Исследователи сосредоточились на тройственно‑негативных клетках рака молочной железы, которые составляют примерно 15–20% случаев и склонны чаще давать рецидивы и метастазы, чем другие типы. Они изучали природную молекулу деоксyelephantopin (DET) и её модифицированный аналог DETD‑35, оба — сесквитерпеновые лактоны из растения Elephantopus. Ранее было показано, что эти соединения вызывают окислительный стресс и нетипичные формы гибели клеток в опухолевых клетках, но то, как они нарушают работу энергетических фабрик клеток, было плохо понятно.
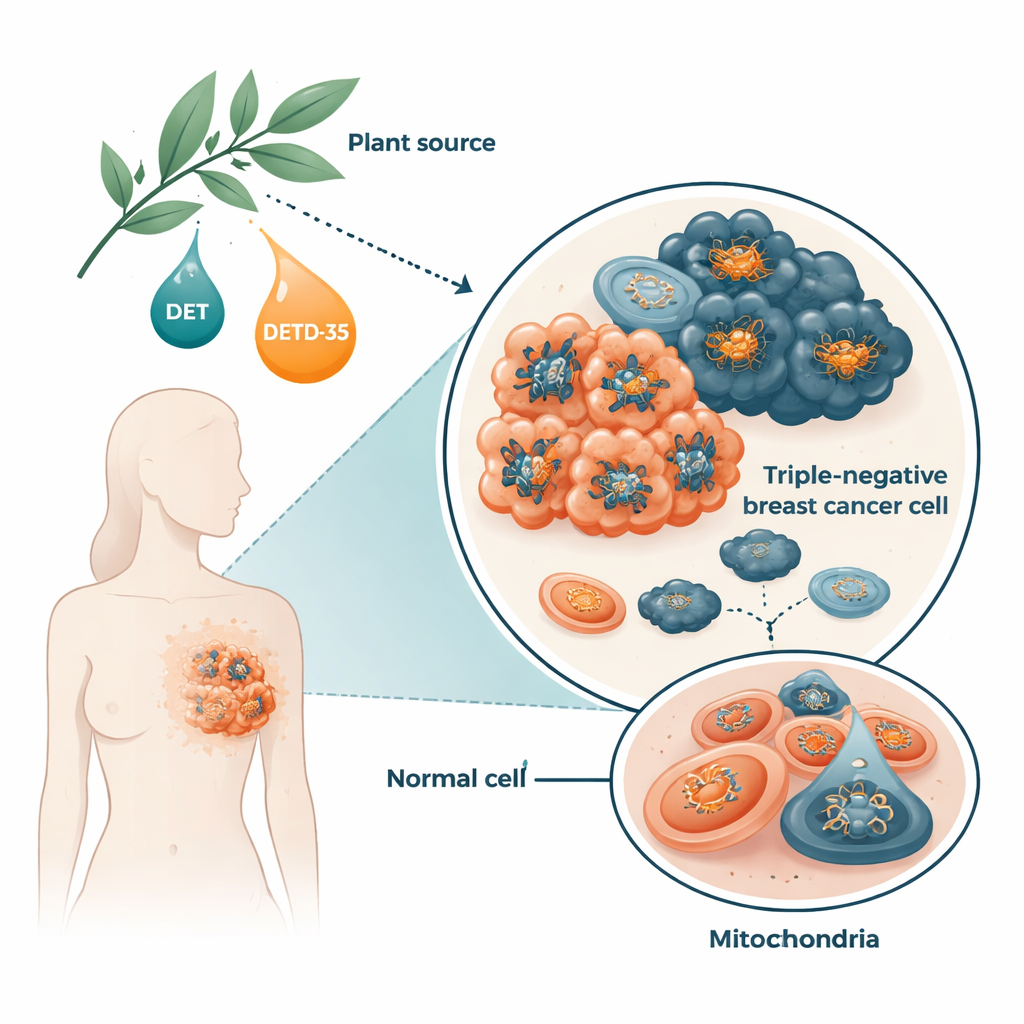
Как растительные молекулы нарушают митохондрии раковых клеток
На моделях человеческих тройственно‑негативных клеток рака молочной железы, выращенных в лаборатории, команда обнаружила, что DET и DETD‑35 быстро повышают выработку реактивных форм кислорода — типа химически активного «выхлопа», образующегося в ходе выработки энергии. В ответ клетки усиливали определённые защитные ферменты, но этого было недостаточно, чтобы восстановить равновесие. Соединения также вынуждали открываться канал в митохондриальной мембране, известный как порога проницаемости (permeability transition pore), изменение, связанное с набуханием, потерей мембранного потенциала и ранними этапами гибели клетки. Всего за несколько часов уровень АТФ в раковых клетках резко падал. При предварительном добавлении антиоксиданта эти повреждающие эффекты в значительной степени обращались, что свидетельствует о ключевой роли окислительного стресса в этом процессе.
Картирование повреждений белков и метаболизма
Чтобы понять общую картину, учёные объединили два мощных «омикс»‑подхода. Они каталогизировали тысячи митохондриальных белков и измерили множество низкомолекулярных метаболитов в обработанных и необработанных клетках. Эта интегрированная картина показала, что DET и DETD‑35 нарушают белки, участвующие в окислительном фосфорилировании — основном пути, с помощью которого митохондрии синтезируют АТФ — и активируют сигналы, связанные со смертью клетки. Одновременно были перепрограммированы ключевые метаболические маршруты, управляющие аминокислотами, жирами и строительными блоками для ДНК. Определённые липиды, формирующие внутреннюю митохондриальную мембрану, а также молекулы, связанные с антиоксидантной защитой и расщеплением сахаров, изменялись в направлениях, согласующихся со стрессовыми, лишёнными энергии раковыми клетками. Существенно, что этих широких изменений не наблюдалось в нормальных клетках молочной железы при тех же дозах, что указывает на степень селективности в отношении опухолевых клеток.
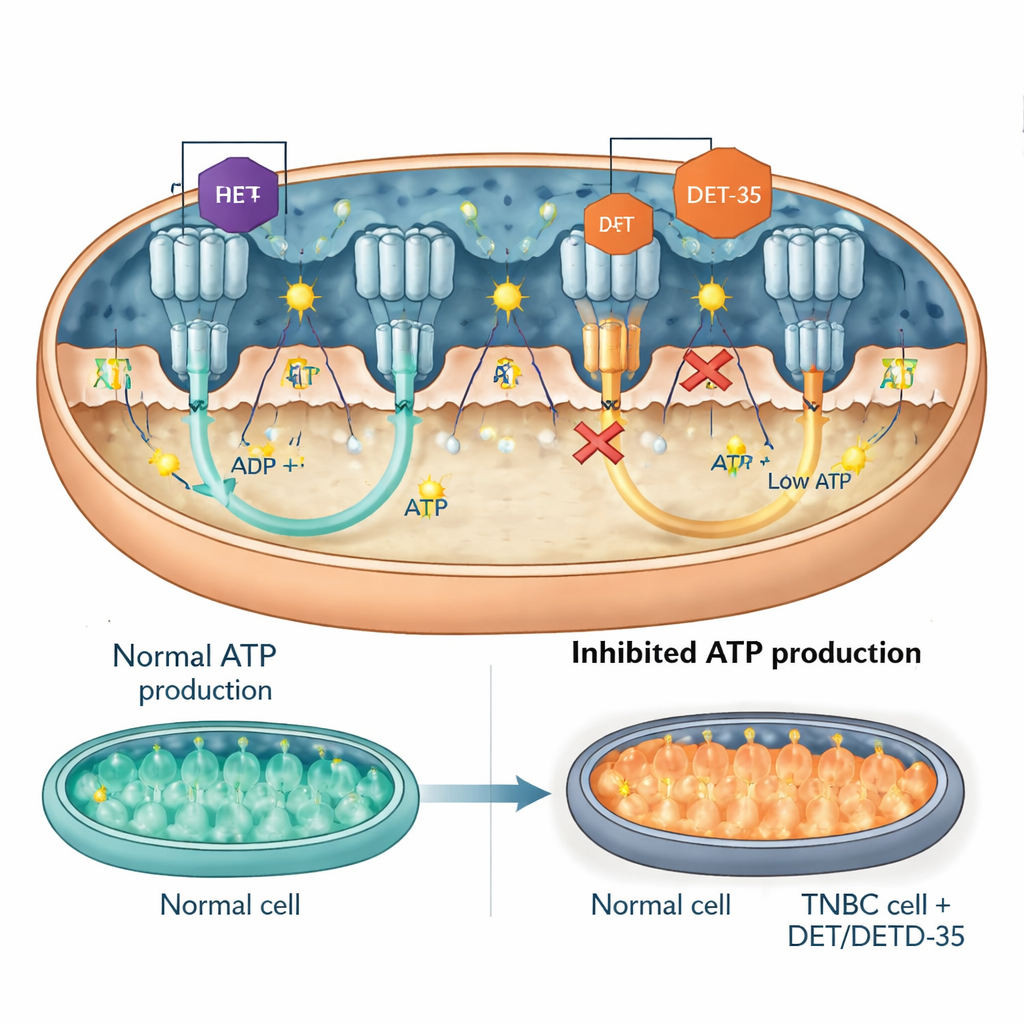
Ключевой сигнальный белок и сама «турбина» АТФ
Затем команда сосредоточилась на конкретных участниках нарушенных сетей. Одним из них оказался PRKCA — сигнальный белок, который может перемещаться в митохондрии и влиять как на выработку энергии, так и на реакции на стресс. DET и DETD‑35 повышали уровни PRKCA в раковых клетках. Когда исследователи с помощью генетических инструментов снижали экспрессию PRKCA, токсичность препаратов уменьшалась: раковые клетки с большей вероятностью выживали, производили больше АТФ и демонстрировали меньше признаков митохондриальных нарушений и апоптоза. Другой объект внимания — АТФ‑синтаза, молекулярная «турбина», которая вращается, чтобы синтезировать АТФ. Измерения показали, что DET и DETD‑35 прямо снижали активность АТФ‑синтазы в митохондриях раковых клеток. Компьютерное «докинг»‑моделирование предполагало, что оба соединения закрепляются на критических интерфейсах фермента, в тех же общих областях, где связываются известные блокаторы АТФ‑синтазы, физически затрудняя его движение и уменьшая выработку АТФ. У мышей с трансплантированными человеческими тройственно‑негативными опухолями лечение любым из соединений снижало уровни компонентов АТФ‑синтазы в опухолевой ткани, что подтверждало выводы клеточных моделей.
Что это может значить для будущего лечения рака
В целом исследование рисует связную картину: эти растительные соединения загоняют тройственно‑негативные раковые клетки молочной железы в энергетический кризис, перегружая их окислительным стрессом, раскрывая митохондриальные поры и напрямую блокируя машину по производству АТФ. По мере истощения АТФ и сбоев в обмене веществ раковые клетки теряют способность расти и выживать, тогда как нормальные клетки молочной железы при тех же условиях остаются в основном невредимыми. Для непрофессионального читателя вывод таков: учёные, возможно, смогут воспользоваться сильной зависимостью рака от его внутренних электростанций, применяя тщательно разработанные молекулы — частично вдохновлённые растениями — чтобы «разрядить батареи» опухолевых клеток, не отключая при этом здоровую ткань. Прежде чем такие агенты смогут попасть в клинику, потребуется ещё много работы, но этот интегрированный взгляд на белки, метаболиты и потоки энергии предлагает перспективную дорожную карту.
Цитирование: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
Ключевые слова: тройственно‑негативный рак молочной железы, митохондрии, АТФ‑синтаза, натуральные продукты, раковый метаболизм