Clear Sky Science · ru
Бактерии из пищевых продуктов и кишечная микробиота производят метилглиоксаль, и этот метаболит приводит к образованию биологически активных алкалоидов 1‑ацетил‑β‑карболинов
Почему важна «химическая лаборатория» вашего кишечника
Внутри наших кишечников и во многих ферментированных продуктах триллионы бактерий постоянно превращают потребляемые сахара в множество химических побочных продуктов. В этом исследовании подробно изучается один такой путь: как некоторые распространённые бактерии превращают сахара в очень реакционноспособное соединение — метилглиоксаль, а затем в семейство биологически активных молекул, называемых 1‑ацетил‑β‑карболинами. Поскольку эти вещества связаны как с патологическими процессами, так и с потенциальными новыми лекарствами, понимание того, когда и как бактерии их синтезируют, может изменить наше представление о пище, микробиоме и здоровье.
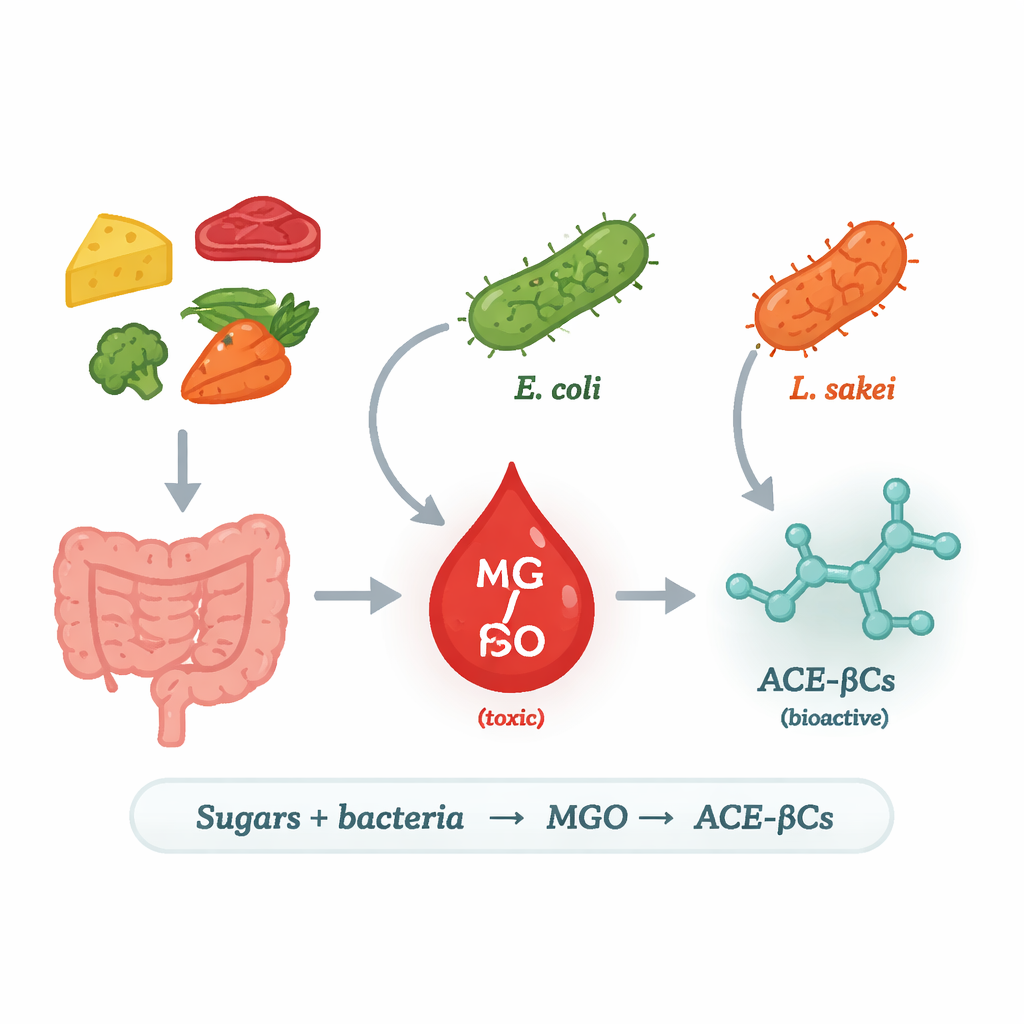
От обычных сахаров до опасной молекулы
Исследователи сосредоточились на метилглиоксале (MGO) — очень реактивном, токсичном побочном продукте распада сахаров. У людей избыток MGO связывают с диабетом, сердечно‑сосудистыми заболеваниями и нейродегенерацией, поскольку он способен повреждать белки и ДНК. Наши клетки обычно контролируют MGO с помощью систем детоксикации, но источником он является не только: бактерии тоже могут его образовывать. У некоторых микроорганизмов фермент под названием метилглиоксальсинтаза (MgsA) превращает промежуточный продукт переработки сахара непосредственно в MGO, создавая «кратчайший путь» в энергетическом метаболизме. Команда поставила вопрос, какие пищевые и кишечные бактерии используют этот маршрут, при каких условиях и что происходит с выделяемым ими MGO.
Кто эти бактериальные производители?
Чтобы выяснить это, учёные вырастили несколько штаммов молочнокислых бактерий, часто встречающихся в продуктах, а также лабораторный штамм Escherichia coli в контролируемой среде, содержащей либо глюкозу, либо галактозу. Затем они отслеживали уровни MGO и двух связанных алкалоидов в культуральной жидкости с течением времени с помощью высокоточной хроматографии и масс‑спектрометрии. Значительные количества MGO и алкалоидов продуцировали только E. coli и вид, связанный с мясом, Lactilactobacillus sakei; другие протестированные молочнокислые бактерии этого не делали. Поиск в геномах выявил ключевое различие: E. coli и L. sakei несут ген для MgsA, тогда как у большинства их молочнокислых родственников этот ген отсутствует. Когда исследователи вставили ген mgsA из L. sakei в штамм, который не продуцировал MGO, этот сконструированный микроорганизм начал синтезировать как MGO, так и алкалоиды, что подтвердило связь MgsA с этим путём.
Как из токсичного MGO образуются биоактивные алкалоиды
Следующий вопрос касался судьбы образованного MGO. Команда сосредоточилась на 1‑ацетил‑β‑карболинах (ACE‑βC) — небольших молекулах, для которых сообщались антимикробная, противовоспалительная и противоопухолевая активности. Они показали, что при выращивании MGO‑продуцирующих бактерий в присутствии аминокислоты L‑триптофан уровни двух ACE‑βC — 1‑ацетил‑β‑карболина и его 3‑карбоксильной формы — резко возрастали. Добавление дополнительного MGO в среду также усиливало их образование. Это указывает на то, что MGO просачивается из клеток и самопроизвольно реагирует с L‑триптофаном в окружающей жидкости, без участия дополнительных ферментов, образуя эти биологически активные соединения. Иными словами, та же химия, которая делает MGO опасным, одновременно превращает его в более сложные молекулы, которые могут обладать полезными эффектами.
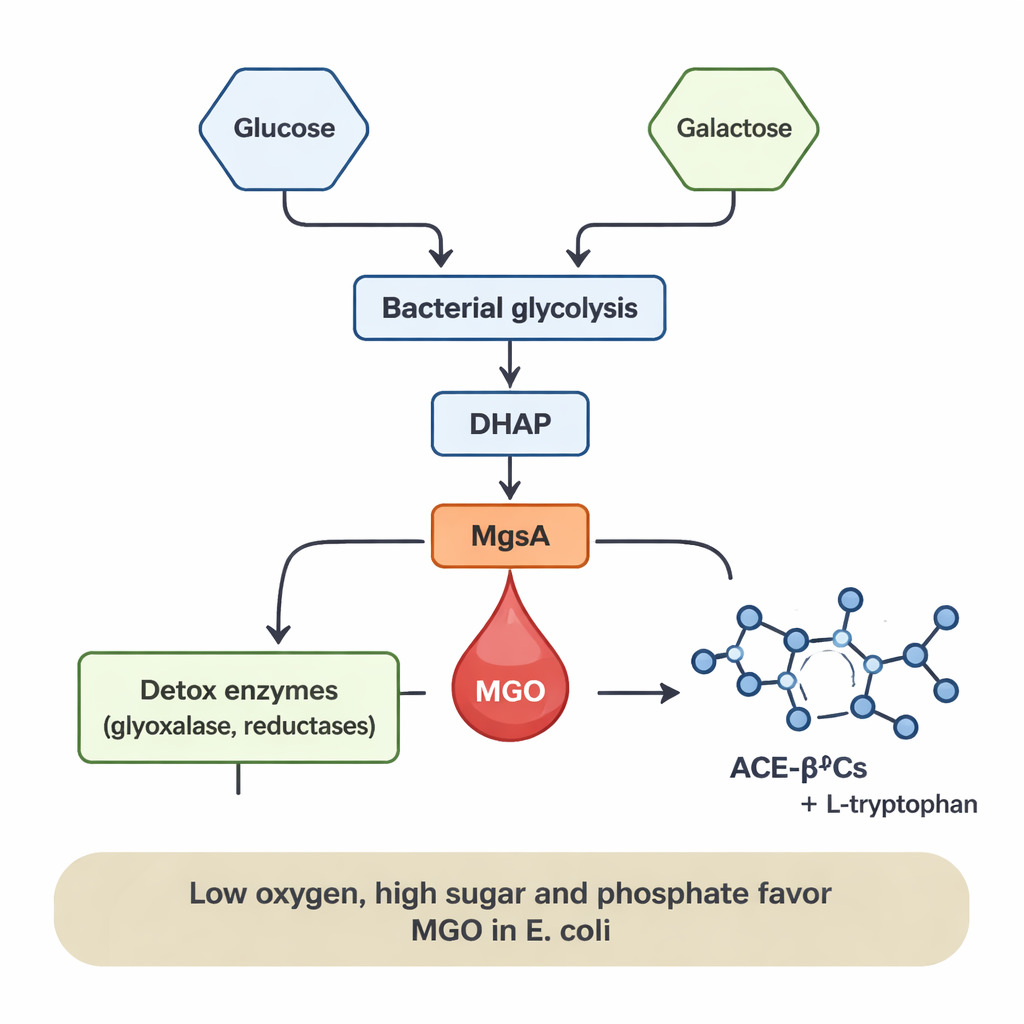
Что увеличивает или уменьшает его образование
Производство MGO не было постоянным; оно сильно зависело от «рациона» бактерий и условий среды. У E. coli MGO появлялся только в присутствии глюкозы, и его уровни росли с увеличением концентрации глюкозы. Добавление фосфата, распространённого минерального элемента, ещё больше усиливало образование MGO в несколько раз, вероятно потому, что фосфат способствует накоплению фосфорилированных промежуточных сахаров, которые питают «кратчайший путь» MgsA. Низко‑кислородные (анаэробные) условия — похожие на те, что в человеческом кишечнике — также способствовали выделению MGO, тогда как хорошо аэрированные условия резко снижали его при том, что рост бактерий оставался хорошим. В отличие от этого, L. sakei в основном вырабатывал MGO при росте на галактозе, и продукция увеличивалась с повышением уровня галактозы. Эти закономерности указывают, что когда поток сахаров через бактериальный метаболизм высок и кислород ограничен, MGO может действовать как «предохранительный клапан», снимая напряжение, вызванное накоплением промежуточных сахаров.
Что это может значить для пищи и здоровья
Результаты показывают, что не все кишечные или пищевые бактерии одинаково способны синтезировать MGO и ACE‑βC. Виды, несущие фермент MgsA, такие как некоторые штаммы L. sakei и E. coli, могут вносить заметный вклад, особенно в средах, богатых сахарами и бедных кислородом, например в кишечнике или при некоторых типах ферментации. Выделяемый ими MGO может увеличивать суммарную химическую нагрузку на ткани хозяина, но его превращение в ACE‑βC частично «поглощает» этот реактивный компонент при одновременном образовании молекул с собственными биологическими эффектами. Хотя это исследование проведено в лабораторных культурах, оно подчёркивает правдоподобный путь, через который диета, состав микробиоты и бактериальный метаболизм совместно формируют баланс между вредными и потенциально полезными химическими веществами в организме, и указывает на ACE‑βC как возможные маркеры бактериального производства MGO в пище и кишечнике.
Цитирование: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Ключевые слова: кишечная микробиота, метилглиоксаль, бактериальный метаболизм, ферментация пищевых продуктов, алкалоиды бета‑карболина