Clear Sky Science · ru
Выведение внутренняя биомаркера активности мозга для раннего предсказания когнитивного спада
Почему важны ранние изменения в мозге
Многие пожилые люди замечают едва заметные провалы в памяти задолго до того, как врач сможет поставить диагноз деменции. На этой стадии стандартные методы визуализации мозга и анализы крови часто не выявляют отклонений, однако патологический процесс уже может развиваться. В этом исследовании проверяли, может ли простой неинвазивный тест — электроэнцефалография (ЭЭГ) — выявлять очень ранние изменения в работе мозга и надежно прогнозировать, у кого в последующие годы наиболее вероятно развитие значимого когнитивного спада.
Слушая тихие сигналы мозга
Исследователи сосредоточились на людях с «субъективным когнитивным снижением» (СКС): пожилых людях, которые ощущают ухудшение памяти, но по стандартным тестам выступают нормально. Восемьдесят восемь таких добровольцев в возрасте от 52 до 85 лет прошли 20‑минутную запись ЭЭГ в состоянии покоя с закрытыми глазами и затем наблюдались в течение 5–7 лет. В ходе последующего наблюдения врачи отслеживали когнитивный статус каждого участника по устоявшимся шкалам. К концу периода некоторые участники оставались стабильными, а другие перешли в состояние легкого когнитивного расстройства или развили деменцию. Эти исходы позволили команде проверить, могли ли тонкие паттерны в исходной ЭЭГ предсказать, кто впоследствии ухудшится.
Преобразование мозговых волн в предсказательный отпечаток
Вместо визуального анализа ЭЭГ команда применяла количественную ЭЭГ (qEEG), которая переводит сырые мозговые волны в тысячи числовых признаков. Эти признаки отражают мощность различных частотных диапазонов (например, альфа‑ и тета‑ритмов), степень синхронизации отдаленных областей мозга между собой (связность и фазовая задержка), а также то, насколько сложным или дезорганизованным выглядит общий паттерн активности. Поскольку нормальное старение также меняет ЭЭГ, исследователи математически скорректировали все признаки по возрасту, а затем стандартизовали их так, чтобы «ноль» обозначал ожидаемое значение для здорового человека того же возраста. Чтобы избежать переобучения, они систематически сократили более 6000 кандидатных показателей до компактного набора, которые были стабильными, не избыточными и лучше всего разделяли тех, кто оставался стабильным, от тех, кто ухудшался.
Машинное обучение как хрустальный шар
С этим сокращённым набором признаков команда обучила несколько моделей машинного обучения — логистическую регрессию, опорные векторные машины и случайные леса — чтобы оценивать вероятность будущего ухудшения для каждого участника. Для реалистичной оценки использовалась повторная кросс‑валидация и специализированный бутстрэп‑метод. По всем моделям точность прогнозирования составила примерно 80%, а площадь под кривой оператора приёмника (AUC) была около 0.90, что указывает на сильную способность отделять стабильных от ухудшающихся людей. Финальные фиксированные модели использовали лишь 14 qEEG‑признаков, в основном полученных из лобных областей мозга с небольшим набором электродов, что делает подход практически применимым в клинике.
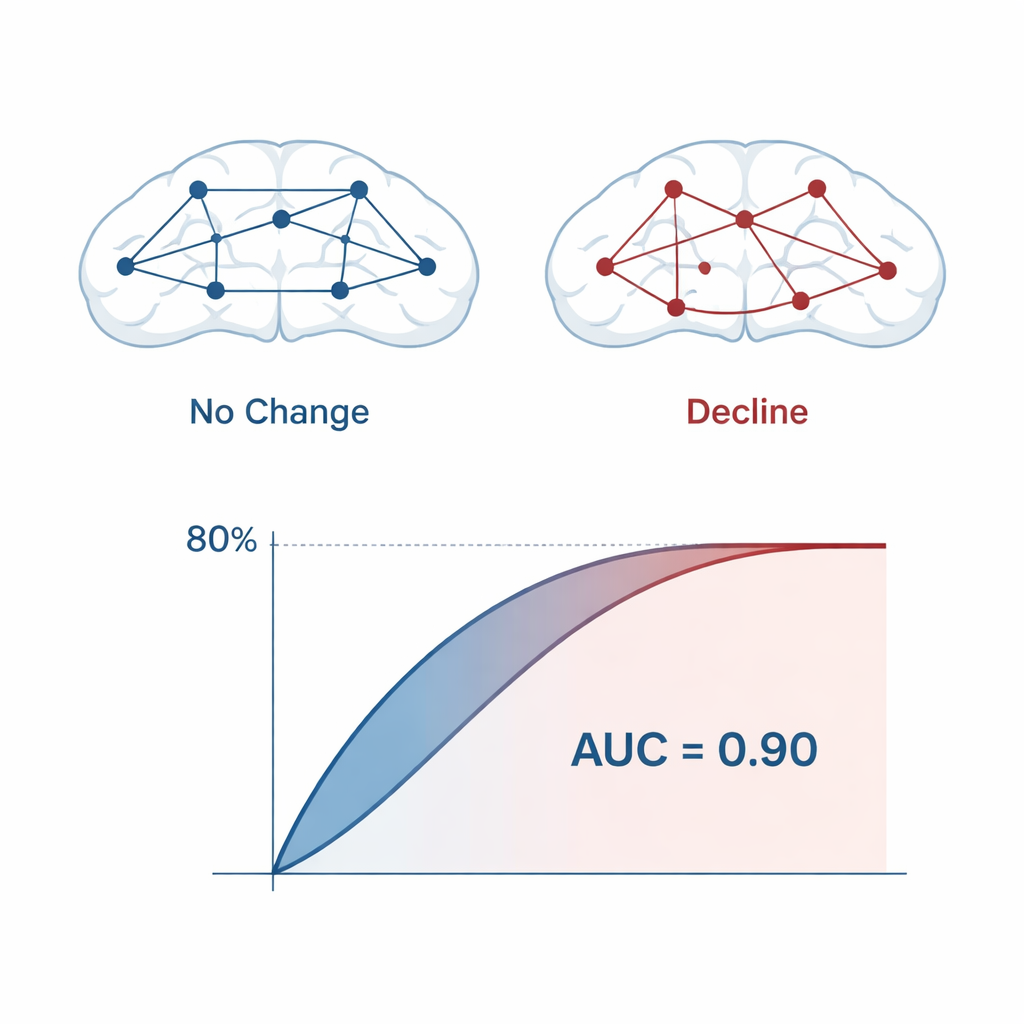
Что меняется в мозге
Признаки, которые обеспечивали наиболее точное предсказание, указывали на раннее нарушение взаимодействия между областями мозга. В модели ключевыми были показатели связности, особенно фазовая задержка и асимметрия между левыми и правыми лобными областями. Выделялись отклонения в альфа‑ и тета‑диапазонах: повышение или смещение тета‑активности в других исследованиях связывали с атрофией гиппокампа и истончением коры, тогда как изменения в мощности и частоте альфа‑ритма могут отражать начальные компенсаторные реакции мозга на появляющееся повреждение. Важно, что ни один отдельный ЭЭГ‑показатель не давал полного ответа. Именно специфическая комбинация — «отпечаток» биомаркера — сигнализировала о повышенном риске за годы до появления явных симптомов.
Испытание инструмента в реальных условиях
Чтобы проверить, будет ли их биомаркер работать за пределами исходной когорты, исследователи протестировали его на двух независимых выборках из США и Италии с разными условиями записи и характеристиками пациентов. Как и ожидалось для принципиально новых данных, точность несколько упала — до примерно 60–70% — но модель всё ещё работала значительно лучше случайного угадывания, что говорит о прочности захваченного сигнала. Команда также показала, что клиницисты могут настраивать порог принятия решения: его понижение повышает чувствительность (ловя больше будущих ухудшающихся при большем числе ложных срабатываний), тогда как повышение порога увеличивает специфичность (меньше ложноположительных, но больше пропущенных случаев). Эта гибкость позволяет адаптировать инструмент под разные клинические приоритеты.
Что это значит для пациентов и врачей
Проще говоря, работа показывает, что короткая и безболезненная запись ЭЭГ — с использованием всего нескольких электродов на лбу — может помочь выявить пожилых людей, которые сегодня выглядят нормально, но имеют высокий риск когнитивного спада в ближайшие годы. Хотя нужны более крупные исследования и сравнения с другими биомаркерами, подход недорогой, неинвазивный и повторяемый, что делает его привлекательным для широкого скрининга, особенно в условиях, где продвинутая визуализация или анализ спинномозговой жидкости затруднительны. При дальнейшем подтверждении такие ЭЭГ‑основанные биомаркеры могут помочь врачам вмешиваться раньше, отслеживать прогрессирование болезни и отбирать участников для клинических испытаний на той стадии, когда лечение наиболее вероятно будет иметь длительный эффект.
Цитирование: Prichep, L.S., Zaidi, S.N., Brink, K. et al. Derivation of an intrinsic brain activity biomarker for the earliest prediction of cognitive decline. Sci Rep 16, 5500 (2026). https://doi.org/10.1038/s41598-026-35144-x
Ключевые слова: раннее предсказание деменции, ЭЭГ мозговые волны, субъективное когнитивное снижение, биомаркер машинного обучения, риск болезни Альцгеймера