Clear Sky Science · ru
Проектирование и анализ характеристик вертикально сложенного nanosheet FET с окружённым нанокамерой для приложений в биосенсинге
Меньше сенсоров — более ранние предупреждения
Раннее выявление рака часто зависит от того, как быстро и точно мы можем обнаружить крошечные следы заболевания в крови или других биологических жидкостях. В этой работе исследуется новый тип ультракомпактного электронного сенсора — выполненного с использованием той же технологии, что и в передовых компьютерных чипах — который способен обнаруживать молекулы, связанные с раком, с значительно большей чувствительностью, чем многие существующие устройства, при очень низком энергопотреблении.
Преобразование транзистора в детектор рака
В основе работы — переработанный транзистор, базовый переключающий элемент электроники. Авторы исходят из передового типа устройства, называемого nanosheet FET, которое уже применяется крупными производителями чипов для 3 нм техпроцессов. Они переосмысливают его как биосенсор, вырезая крошечные полые области, или нанокамеры, вокруг изолированного затвора, контролирующего ток. Когда молекулы, связанные с раком — например клетки опухолей толстой кишки или почек, фрагменты ДНК или желатиноподобные белки — оседают в этих полостях, они тонко изменяют поведение электрического заряда внутри устройства. Транзистор «чувствует» это изменение как сдвиг в токе, превращая биохимическое событие в электрический сигнал, который можно измерить.
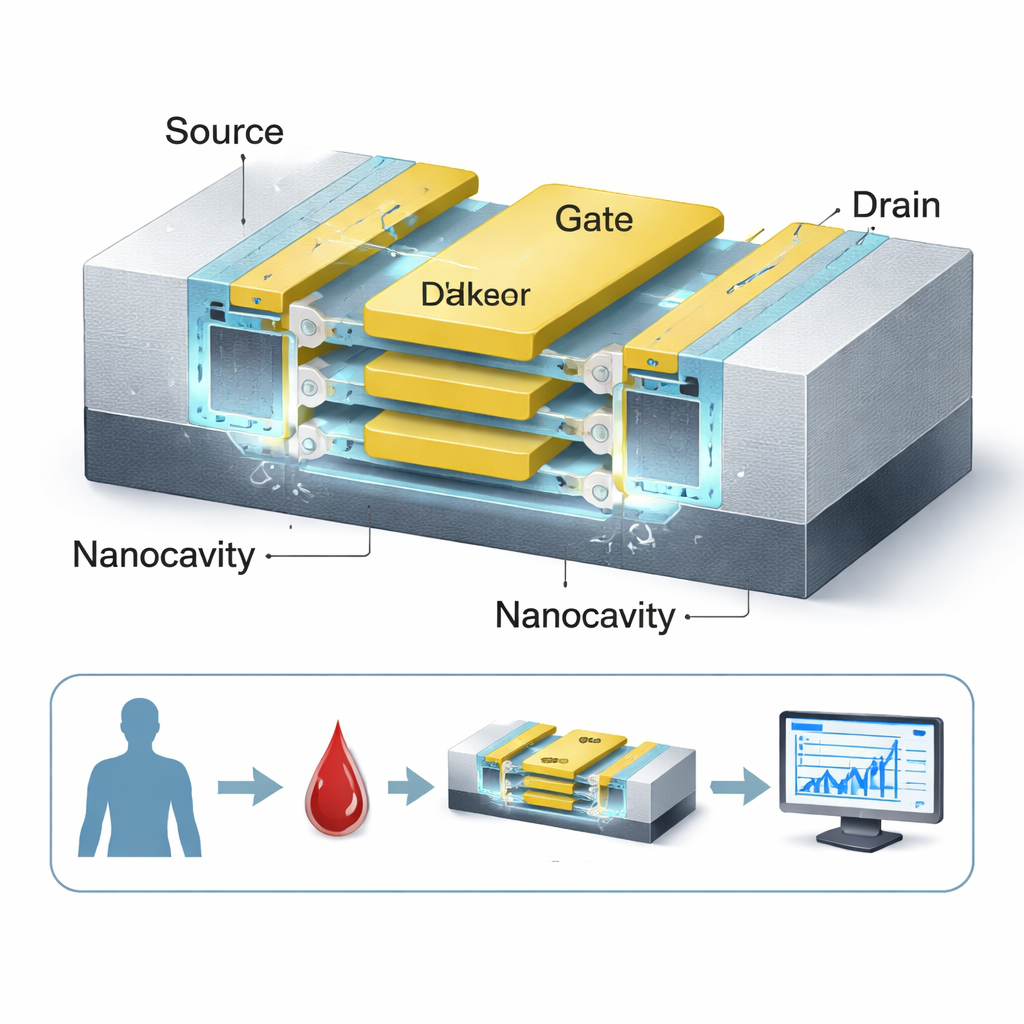
Сложенные слои для более сильного сигнала
Ключевая особенность дизайна в том, что чувствительный канал представляет собой не одну проволоку, а три сверхтонких кремниевых листа, сложенных вертикально и охваченных общим затвором. Такая конструкция «затвор-вокруг-всего» обеспечивает более плотный контроль затвора над каналом, чем у традиционных плоских транзисторов, что повышает резкость включения/выключения и усиливает измеряемое изменение при наличии биомолекул. Две нанокамеры расположены по обе стороны слоя высоко-k диэлектрика (HfO₂), максимально увеличивая область, где молекулы могут взаимодействовать с электрическим полем. Поскольку канал не содержит легирования (doping-less), то есть избегает сильных химических примесей, отклик сенсора становится более однородным и менее чувствительным к вариациям процессов изготовления — это преимущество для надежных медицинских тестов.
Настройка крошечных камер для максимального отклика
С помощью подробных компьютерных моделирований (TCAD) исследователи систематически регулируют геометрию камер: их длину, толщину и степень заполнения молекулами. Более короткие и тонкие камеры приближают затвор и канал в электростатическом плане, что увеличивает ток в открытом состоянии и уменьшает так называемый субпороговый наклон — меру того, как резко устройство включается. В их оптимальном дизайне сенсор достигает исключительно низкого наклона порядка 28 миллиовольт на декаду, что значительно ниже предела 60 мВ/дек для стандартных транзисторов. Это означает, что устройство сильно реагирует на очень небольшие изменения напряжения — критическое свойство для обнаружения низких концентраций биомолекул. Они также показывают, что по мере увеличения заполнения объёма камер — или если молекулы располагаются ближе к точке, где начинается ток — сигнал усиливается, что поясняет, как плотность и расположение целей влияют на характеристики.
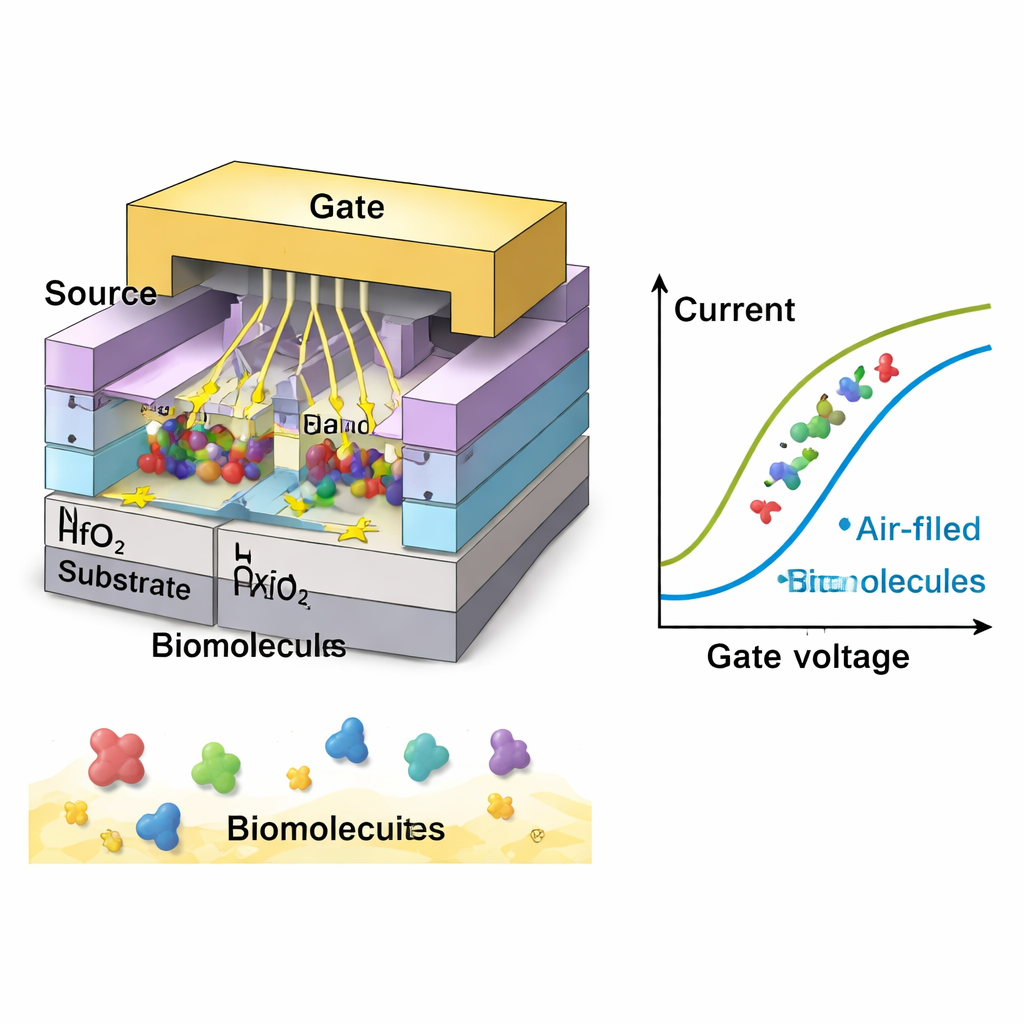
Чтение подсказок о раке в электрических сигналах
Далее команда изучает, как различные типы биомолекул будут выглядеть с электрической точки зрения. Нейтральные виды с более высокой собственной диэлектрической проницаемостью (свойство, связанное с тем, как они поляризуются в поле) приводят к большим изменениям тока и лучшей чувствительности; наибольший отклик наблюдается при значениях, типичных для желатина и некоторых плотных биологических тканей. Заряженные молекулы, такие как ДНК или определённые клеточные поверхности, могут ещё больше усилить сигнал. В моделированиях отрицательно заряженные биомолекулы дают наибольший сдвиг тока, затем следуют положительные заряды и потом нейтральные. При оптимальных условиях устройство достигает чувствительности тока более чем в 3000 раз выше базовой и свыше 9000 для сильно отрицательных зарядов — превосходя несколько ранее предложенных биосенсоров на базе nanosheet. Сенсор также демонстрирует быструю скорость отклика, стабильную работу при близких к комнатной температуре условиях и хорошую специфичность, то есть способность отличать целевые молекулы от похожих, но нежелательных.
К практическим чип‑уровневым тестам на рак
Чтобы убедиться в реализуемости концепции, авторы описывают технологическую последовательность изготовления, которая близко следует современным передовым методам производства чипов, с использованием стандартных пластин silicon-on-insulator, известных оксидных и металлизационных слоёв и общих этапов травления для формирования нанокамер. Поскольку структура остаётся компактной и совместимой с массовыми CMOS-процессами, её, в принципе, можно интегрировать в плотные массивы на одном кристалле. Для неспециалиста вывод таков: эта работа приближает транзисторно‑базирующиеся биосенсоры к практическим устройствам «лаборатория-на-чипе», которые однажды могут быстро скринировать маркёры рака с высокой чувствительностью и без необходимости меток или сложной химии, используя технологию, очень похожую на ту, что уже питает современную электронику.
Цитирование: Prasanna, R.L., Karumuri, S.R., Sreenivasulu, V.B. et al. Design and performance analysis of a vertically stacked gate-all-around nanosheet FET with embedded nanocavity for biosensing applications. Sci Rep 16, 5508 (2026). https://doi.org/10.1038/s41598-026-35132-1
Ключевые слова: биосенсор рака, nanosheet FET, лаборатория-на-чипе, датчик с нанокамерой, раннее обнаружение