Clear Sky Science · ru
Лактат регулирует ось YTHDF2–FTH1, способствуя ферроптозу кардиомиоцитов и усугубляя ишемически-реперфузионное повреждение миокарда
Почему эта химия важна для пациентов с заболеваниями сердца
Когда врачи вновь открывают закупоренную коронарную артерию после инфаркта, приток свежей крови спасает мышцу, но может также вызвать дополнительное повреждение — ишемически‑реперфузионное повреждение. В этом исследовании обнаружен неожиданный виновник внутри сердечных клеток: обычный метаболит лактат. Авторы показывают, что лактат способен переключать молекулярный механизм, подталкивающий кардиомиоциты к определённому виду железозависимой гибели клеток, усиливая повреждение. Понимание этого скрытого пути может указать на новые лекарства, которые лучше защитят сердце при экстренном лечении.
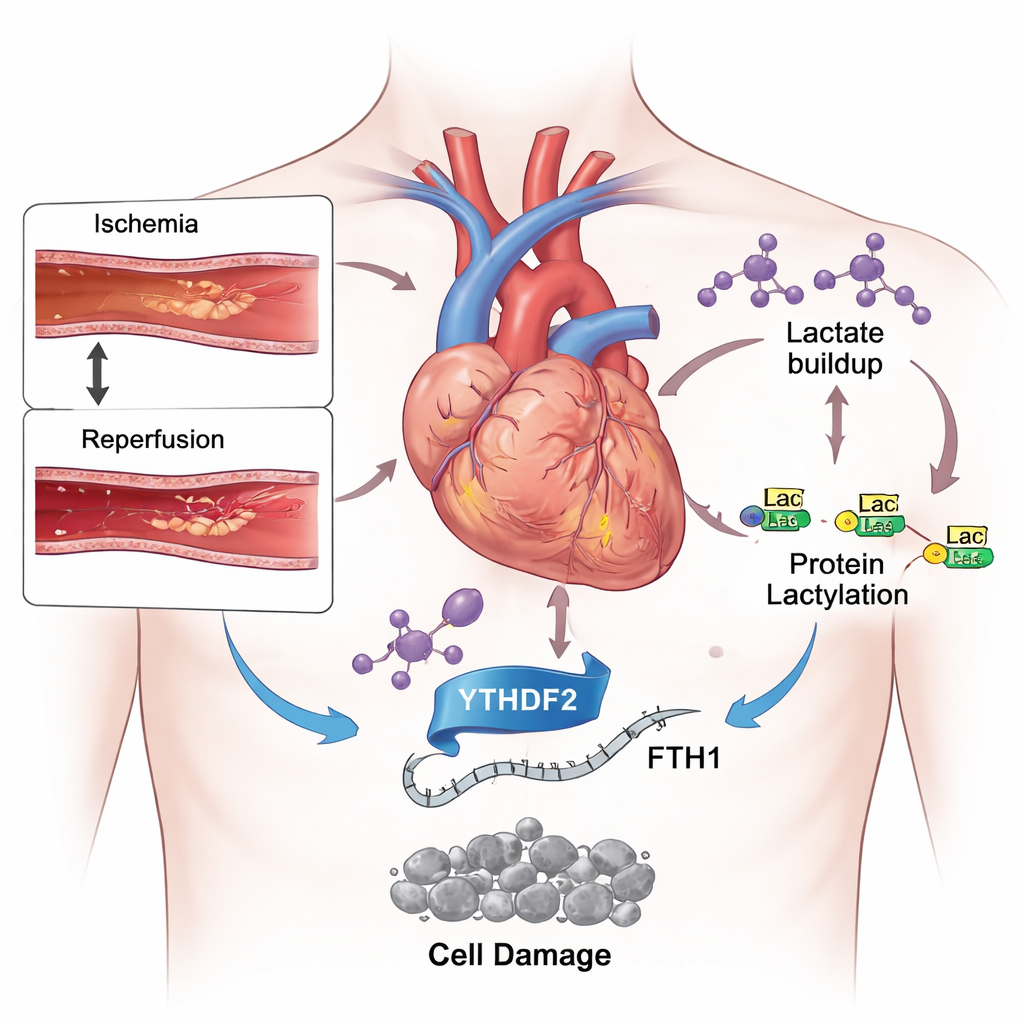
Двуострый меч в лечении инфаркта
Современная медицина научилась быстро восстанавливать проходимость коронарных артерий, ограничивая первоначальное повреждение при инфаркте. Тем не менее у пациентов всё ещё могут отмирать большие участки сердечной мышцы после восстановления кровотока. Одна из причин — внезапное возвращение кислорода и питательных веществ, которое вызывает лавину химического стресса в кардиомиоцитах. Среди нескольких типов гибели клеток, запускаемых в этой ситуации, особое внимание привлекает сравнительно новый тип — ферроптоз. В отличие от более знакомых форм, таких как апоптоз, ферроптоз зависит от железа и неконтролируемой перекисного окисления липидов мембран клеток, что может необратимо ослабить сердце.
Как лактат становится чем‑то большим, чем «жжение в мышцах»
Во время инфаркта истощённая сердечная мышца переключается на гликолиз — аварийный путь расщепления сахаров, который быстро вырабатывает много лактата. На моделях с мышами, которым кратковременно блокировали и затем восстанавливали кровоток в артерии, а также в культуре кардиомиоцитоподобных клеток, подвергнутых гипоксии и повторной оксигенации, исследователи обнаружили резкое повышение уровня лактата. Одновременно они зафиксировали увеличение лактилации — химической метки — на многих белках и на гистонах, каркасных белках, организующих ДНК. Когда животным вводили препарат, замедляющий гликолиз и уменьшающий продукцию лактата, повреждение сердца сокращалось, в крови падали маркеры травмы, а соотношение вредного железа и защитных антиоксидантов улучшалось. Эти результаты свидетельствуют о том, что избыток лактата — не просто побочный продукт стресса, а активный фактор повреждения.
Молекулярный переключатель, ослабляющий стропы железа
Углубляясь, команда сосредоточилась на белке YTHDF2, который распознаёт химические метки на РНК и определяет скорость разрушения некоторых сообщений. Они обнаружили, что ишемия–реперфузия и добавленный лактат повышают уровни YTHDF2 и увеличивают лактилацию в окрестности гена, его кодирующего, усиливая его продукцию. Одной из ключевых мишеней YTHDF2 оказалась РНК тяжёлой цепи ферритина (FTH1) — центрального компонента клеточной «клетки хранения» железа. FTH1 обычно надёжно удерживает железо в безопасной форме, не позволяя ему запускать повреждающие реакции. В стрессовых сердечных клетках YTHDF2 сильнее связывался с РНК FTH1 и ускорял её разрушение, оставляя клетки с меньшим числом ферритиновых «ячей», большим количеством свободного железа, повышенным окислительным стрессом и признаками ферроптоза.
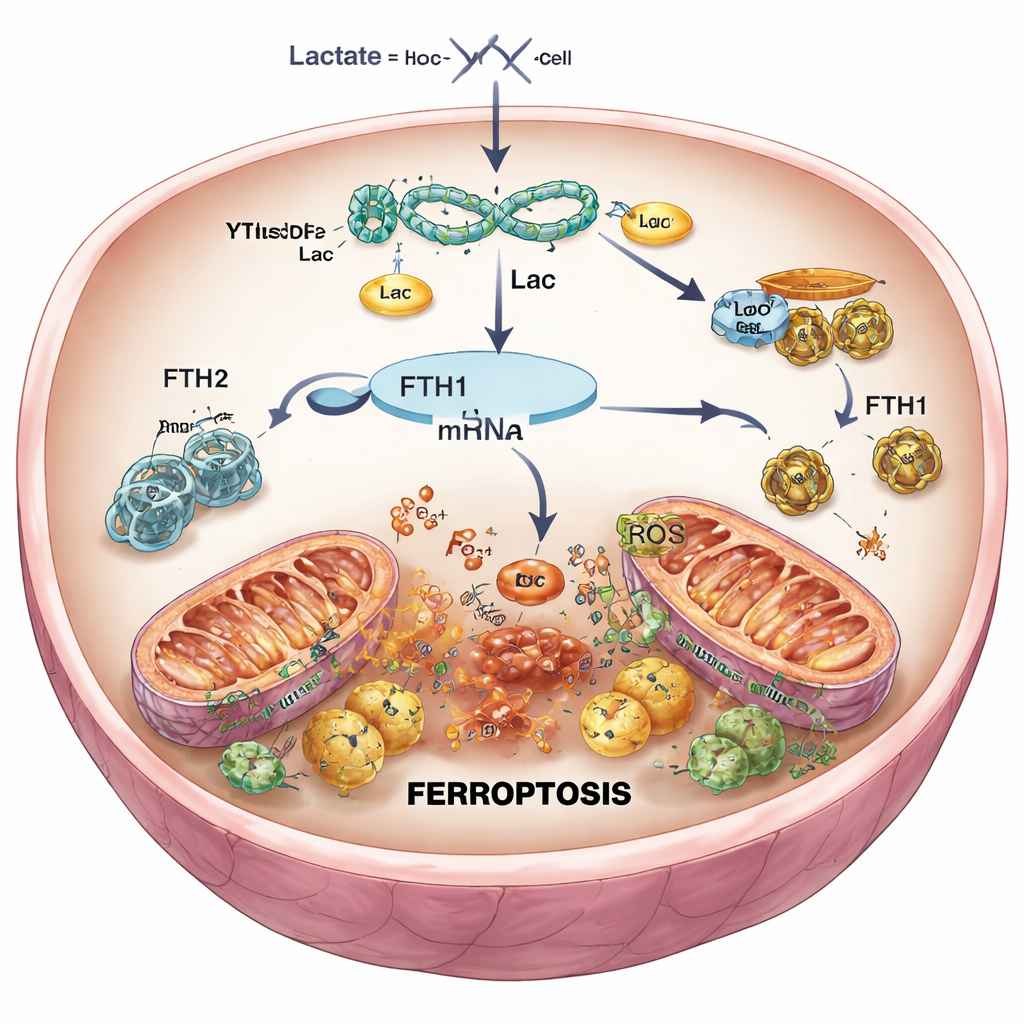
Ослабление сигнала смерти в кардиомиоцитах
Чтобы проверить причинно‑следственную связь, исследователи с помощью генетических инструментов выборочно сократили YTHDF2 в кардиомиоцитах и у мышей. При подавлении YTHDF2 уровни FTH1 восстанавливались, количество железа и реактивных форм кислорода снижалось, митохондрии сохраняли более нормальную форму, а выживаемость клеток после моделируемой реперфузии улучшалась. У мышей пониженный YTHDF2 приводил к меньшим рубцам после инфаркта и более здоровой ткани. Однако при одновременном снижении FTH1 эти преимущества в основном исчезали: железо снова росло, окислительное повреждение возвращалось, а площадь инфаркта увеличивалась. Это подтвердило, что YTHDF2 продвигает ферроптоз преимущественно за счёт подавления FTH1, ослабляя контроль за железом в сердце.
Что это значит для будущей терапии сердца
Собрав воедино данные, исследование описывает новую цепочку событий: блокированная, а затем вновь открытая артерия вызывает накопление лактата; лактат повышает YTHDF2 через лактилацию; YTHDF2 разрушает РНК, кодирующую железозащитный белок FTH1; и последующая перегрузка железом запускает ферроптоз, усугубляя повреждение сердца. Для пациентов посыл обнадёживает: этот путь предлагает несколько точек для вмешательства. Препараты, ограничивающие вредную лактат‑сигнацию, блокирующие специфическую модификацию YTHDF2 или сохраняющие функцию FTH1, могут сделать экстренную реперфузию безопаснее и защитить больше сердечной мышцы. Хотя эти выводы ещё требуют подтверждения на тканях человека, они открывают перспективное направление к более мягким и эффективным методам лечения выживших после инфаркта.
Цитирование: Xiang, Z., Xiang, B., Ouyang, T. et al. Lactate regulates the YTHDF2-FTH1 axis to promote cardiomyocyte ferroptosis and aggravate myocardial ischemia-reperfusion injury. Sci Rep 16, 4865 (2026). https://doi.org/10.1038/s41598-026-35130-3
Ключевые слова: сердечный приступ, лактат, железозависимая гибель клеток, ишемия–реперфузия, защита кардиомиоцитов