Clear Sky Science · ru
Компактные модели глубокого обучения для гистопатологии толстой кишки: проблемы производительности и обобщения
Почему это исследование важно для пациентов и врачей
Рак толстой кишки — один из смертельных видов рака в мире, однако его диагностика по‑прежнему во многом зависит от того, что специалисты внимательно изучают под микроскопом изображения ткани; эта задача медленная и подвержена расхождению мнений. В работе исследуется, могут ли очень маленькие и эффективные модели искусственного интеллекта (ИИ) достаточно точно отмечать опухолевую ткань толстой кишки, чтобы быть полезными в повседневной клинической практике, в том числе в условиях ограниченных вычислительных ресурсов. Также выявлена скрытая уязвимость: модели, которые выглядят почти идеальными в процессе разработки, могут сильно ошибаться на новых, реальных данных.
Обучение компьютеров «читать» микроскопические изображения
При взятии биопсии толстой кишки патологи рассматривают тонкие, окрашенные срезы ткани под микроскопом. Раковая ткань демонстрирует искажённые железы, неправильную форму клеток и инвазии в окружающие структуры, тогда как здоровая ткань имеет упорядоченные, регулярные узоры. Авторы использовали общедоступную коллекцию из 24 000 цифровых изображений таких срезов, поровну распределённых между раком (аденокарцинома толстой кишки) и доброкачественной тканью. Все изображения были приведены к стандартному небольшому формату и подвергнуты реалистичным преобразованиям — небольшим поворотам, отражениям, увеличению и мягким изменениям цвета — чтобы имитировать естественные различия в том, как срезы режут, окрашивают и сканируют. Такая тщательная подготовка помогает моделям ИИ сосредоточиться на содержательных паттернах ткани, а не на поверхностных деталях вроде точной ориентации или яркости.
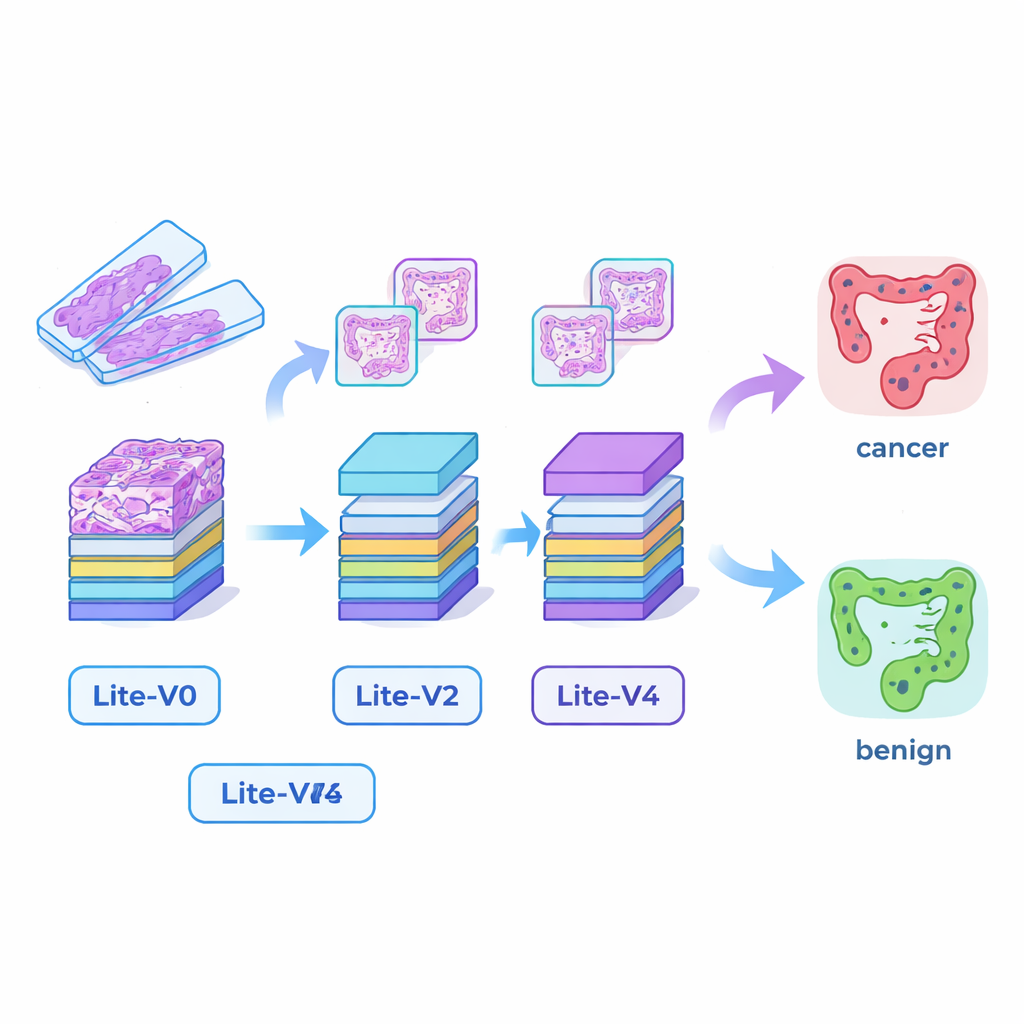
Создание крошечных, но способных «глаз» ИИ
Многие успешные медицинские системы ИИ опираются на очень большие модели глубокого обучения, требующие мощных видеокарт и много памяти, что затрудняет их развёртывание в небольших больницах или у постели пациента. Чтобы сократить этот разрыв, исследователи разработали четыре компактные сверточные нейронные сети — Lite‑V0, Lite‑V1, Lite‑V2 и Lite‑V4. Каждая из них анализирует одни и те же фрагменты входного изображения, но различается по числу слоёв и фильтров, используемых для обнаружения визуальных признаков, таких как края, текстуры и форма желёз. Все четыре модели имеют простую и прозрачную архитектуру: повторяющиеся блоки стандартной свёртки, нормализации и пулинга, за которыми следует небольшой «решающий» модуль, выдающий вероятность наличия рака или доброкачественной ткани. Цель состояла в том, чтобы понять, сколько точности можно выжать из моделей, достаточно маленьких, чтобы комфортно размещаться на базовом клиническом оборудовании.
Впечатляющие показатели в условиях лаборатории
Команда обучила и сравнила все четыре модели на фиксированном разбиении набора данных, используя общепринятые метрики: точность, сбалансированный F1‑скор, учитывающий ошибки в обоих классах, матрицы ошибок и диагностические графики вроде ROC и кривых точность‑полнота. В центре внимания оказалась модель среднего размера Lite‑V2. Несмотря на то, что её объём составлял всего около 1,5 мегабайта и в ней было примерно 128 000 настраиваемых параметров, она показала почти безупречные результаты на внутреннем валидационном наборе: макро F1‑скор около 0,999 и почти идеальная чувствительность и специфичность. Иными словами, в этой тщательно подготовленной среде Lite‑V2 почти всегда могла отличать раковую ткань от доброкачественной, оставаясь быстрой и лёгкой для использования на скромных компьютерах.
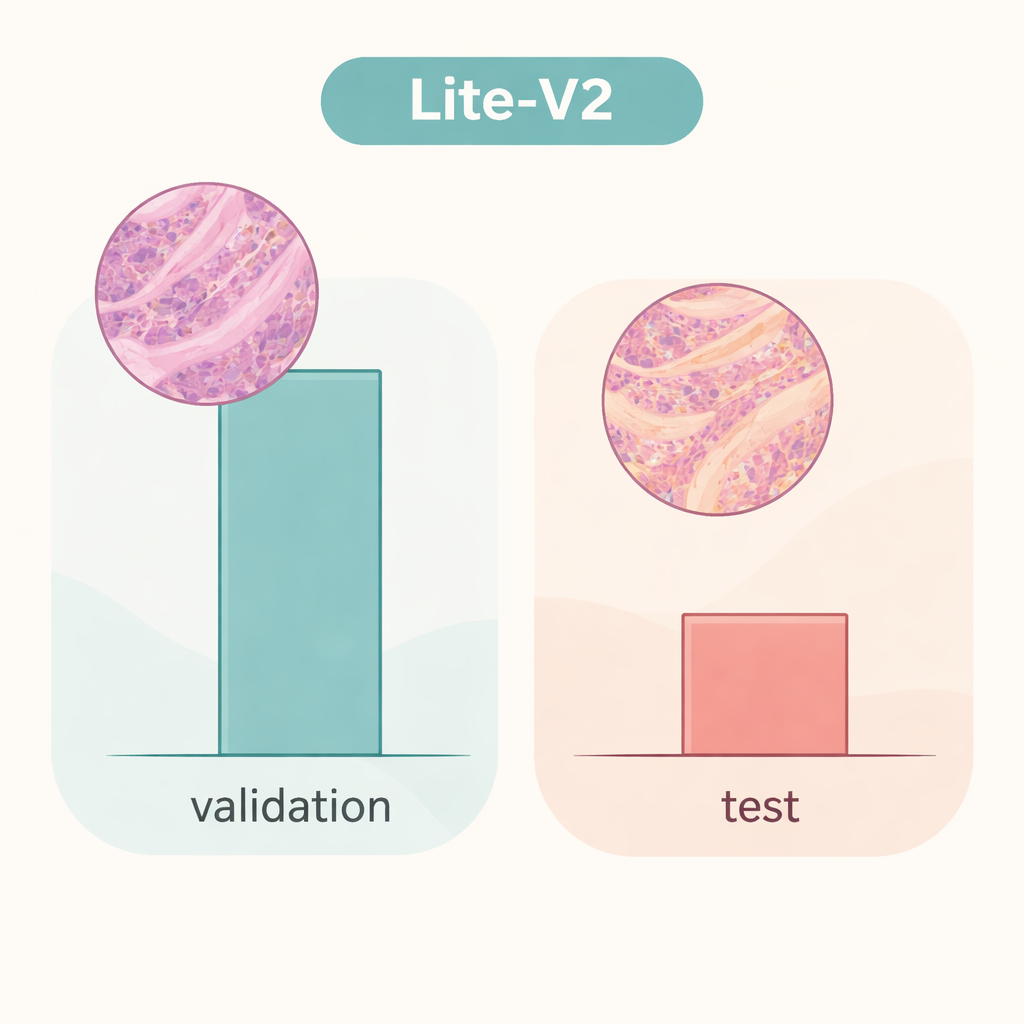
Когда реальная вариативность нарушает магию
Однако картина резко меняется, когда ту же модель Lite‑V2 испытывают на независимом наборе изображений, которые отличаются тонкими признаками, имитирующими слайды из другой лаборатории — то, что исследователи называют «смещением домена». На этом невиданном тестовом наборе общая точность упала примерно до 50%, а сбалансированный F1‑скор снизился примерно до 0,33. Модель продолжала распознавать многие образцы рака, но серьёзно ошибалась с доброкачественной тканью, помечая значительную часть как злокачественную. Это показывает, что сеть выучила детали, тесно связанные с исходным источником данных — например, стиль окрашивания или характеристики сканера — вместо устойчивых, переносимых маркеров болезни. Работа подчёркивает, что впечатляющие результаты на внутренней валидации могут создать ложное чувство уверенности, если модели не испытывать на по‑настоящему отличающихся данных.
Что это значит для будущих инструментов ИИ в диагностике
Для неспециалиста вывод двойной. Во‑первых, компактные системы ИИ действительно могут достигать уровня экспертов при анализе изображений ткани толстой кишки, оставаясь достаточно маленькими и эффективными для широкого внедрения — это открывает путь к более быстрому скринингу и поддержке перегруженных патологов. Во‑вторых, и не менее важно: модель, выглядящая «идеальной» на своём домашнем наборе данных, может сильно подвести при встрече с изображениями из новой больницы. Авторы утверждают, что будущая работа должна быть направлена на повышение устойчивости этих лёгковесных моделей к изменениям в окрашивании, сканерах и популяциях пациентов — с помощью стратегий вроде обучения, устойчивого к вариациям окрашивания, адаптации домена и более широких многоцентровых наборов данных. До тех пор ИИ следует рассматривать как многообещающего помощника, а не как автономный инструмент принятия решений при диагностике рака.
Цитирование: Hanif, F., Raza, A. & Mohammed, H.A. Compact deep learning models for colon histopathology focusing performance and generalization challenges. Sci Rep 16, 5489 (2026). https://doi.org/10.1038/s41598-026-35119-y
Ключевые слова: рак толстой кишки, гистопатология, глубокое обучение, легковесная CNN, смещение домена