Clear Sky Science · ru
Фосфатаза двойной специфичности 6 мешает репрессивной активности факторa транскрипции FOXO1 в отношении CYP4A11, что способствует накоплению липидов в печени
Почему жир в печени имеет значение
Чрезмерное количество жира в печени, часто называемое жировой болезнью печени, становится всё более распространённым на фоне современных диет, богатых сахаром и жирами. Если о холестерине или уровне глюкозы в крови многие слышали, то меньше людей знают, что крошечные молекулярные переключатели внутри печёночных клеток помогают решать, будет ли жир сжигаться или накапливаться. В этом исследовании рассматриваются три таких переключателя — белки DUSP6, FOXO1 и CYP4A11 — и выясняется, как их взаимодействие может склонить печёночные клетки к накоплению избытка жира. Понимание этой скрытой системы управления может указать путь к новым методам лечения жировой болезни печени и связанных с ней метаболических нарушений.
Скрытый регулятор трафика внутри печёночных клеток
Исследователи сосредоточились на белке DUSP6, который прежде всего известен как выключатель сигнального пути ERK. Предыдущие работы показали, что мыши, лишённые DUSP6, оказались удивительно устойчивы к диетически индуцированной жировой болезни печени, и в их печени были снижены уровни ферментов CYP4A, участвующих в обмене жиров. В этой работе команда задала вопрос, что делает DUSP6 в клетках, происходящих от человеческой печени, и как он может влиять на человеческую форму этих ферментов — CYP4A11. Использовали два стандартных клеточных ряда рака печени, HepG2 и HuH‑7, в качестве заменителей человеческих печёночных клеток и нагружали их смесью жирных кислот (пальмитиновой и олеиновой), чтобы смоделировать неблагоприятную среду с высоким содержанием жира. 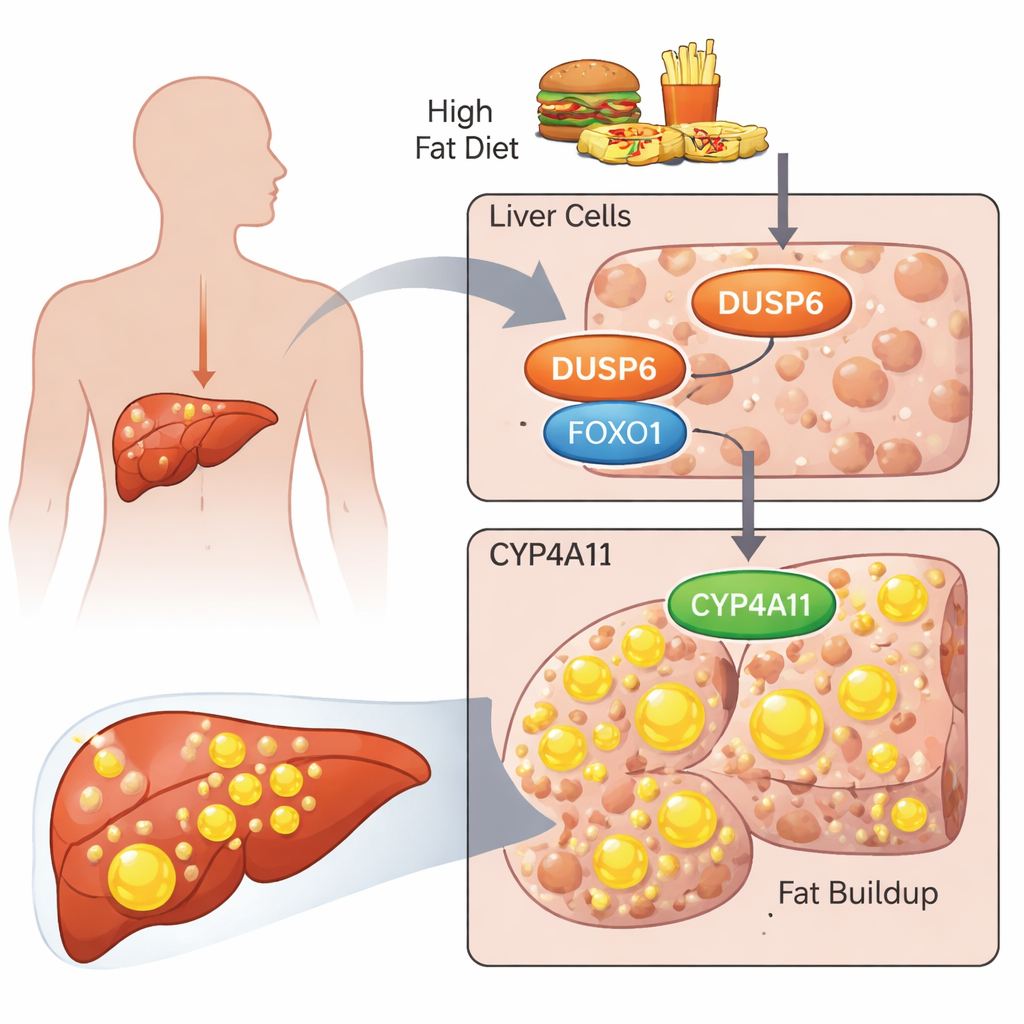
От жирных кислот к клетке, заполненной жиром
Когда клетки подвергали воздействию этих жирных кислот, они наглядно накапливали жировые капли, которые учёные красили и измеряли. Одновременно повышались уровни DUSP6 и CYP4A11, а также активированных форм двух основных сигнальных белков — AKT и FOXO1. Понижение уровня DUSP6 с помощью направленных РНК отменяло эту картину: клетки откладывали меньше жира, уровни CYP4A11 снижались, но при этом возрастала активность ERK, AKT и FOXO1. Блокада только пути ERK фактически усугубляла накопление жира, тогда как блокада только AKT уменьшала его. Когда блокировали оба пути — ERK и AKT — накопление жира снижалось, и уровни CYP4A11 падали. Эти эксперименты связали CYP4A11 с масштабом накопления жира и показали, что активность AKT особенно важна для продвижения отложения липидов.
Тормоз для генов, способствующих накоплению жира
Другой ключевой участник, FOXO1, — это фактор транскрипции, белок, который может проникать в ядро клетки и включать или выключать гены. Известно, что FOXO1 действует как тормоз для нескольких членов того же семейства ферментов, что и CYP4A11. Команда обнаружила, что снижение уровня FOXO1 заставляло клетки запасать больше жира и повышало CYP4A11, тогда как прямое повышение экспрессии CYP4A11 делало клетки ещё «жирнее». Напротив, вынужденная экспрессия FOXO1 снижала и CYP4A11, и накопление жира. Препарат, блокирующий активность CYP4A11 (HET0016), уменьшал избыток жира, вызванный низким уровнем FOXO1, что поддерживает идею о том, что CYP4A11 не просто наблюдатель, а драйвер накопления липидов. Химические анализы показали, что HET0016 снижает уровень 20‑HETE — продукта, образуемого CYP4A11, связанного с оксидативным стрессом и воспалением, — что дополнительно связывает этот путь с повреждением печени.
Как DUSP6 обезоруживает тормоз
Чтобы понять, как FOXO1 контролирует CYP4A11, учёные изучили участок ДНК перед геном CYP4A11 и обнаружили последовательности, где FOXO1 может связываться. С помощью хроматин‑иммунопреципитационного анализа они показали, что FOXO1 — в частности его нефосфорилированная форма — непосредственно связывается с промотором CYP4A11, что согласуется с его репрессивной, тормозящей ролью по отношению к этому гену. Эксперименты ко‑иммунопреципитации выявили, что DUSP6 физически взаимодействует с FOXO1, но не с его фосфорилированной формой. Фракционирование и микроскопия показали, что DUSP6 локализуется в цитоплазме клетки и, когда присутствует, удерживает больше FOXO1 вне ядра. При снижении DUSP6 больше FOXO1 перемещалось в ядро, где он мог связываться с ДНК и подавлять CYP4A11. По сути, DUSP6 действует как якорь, секвестрируя FOXO1 в цитоплазме и препятствуя его работе в роли тормоза для CYP4A11. 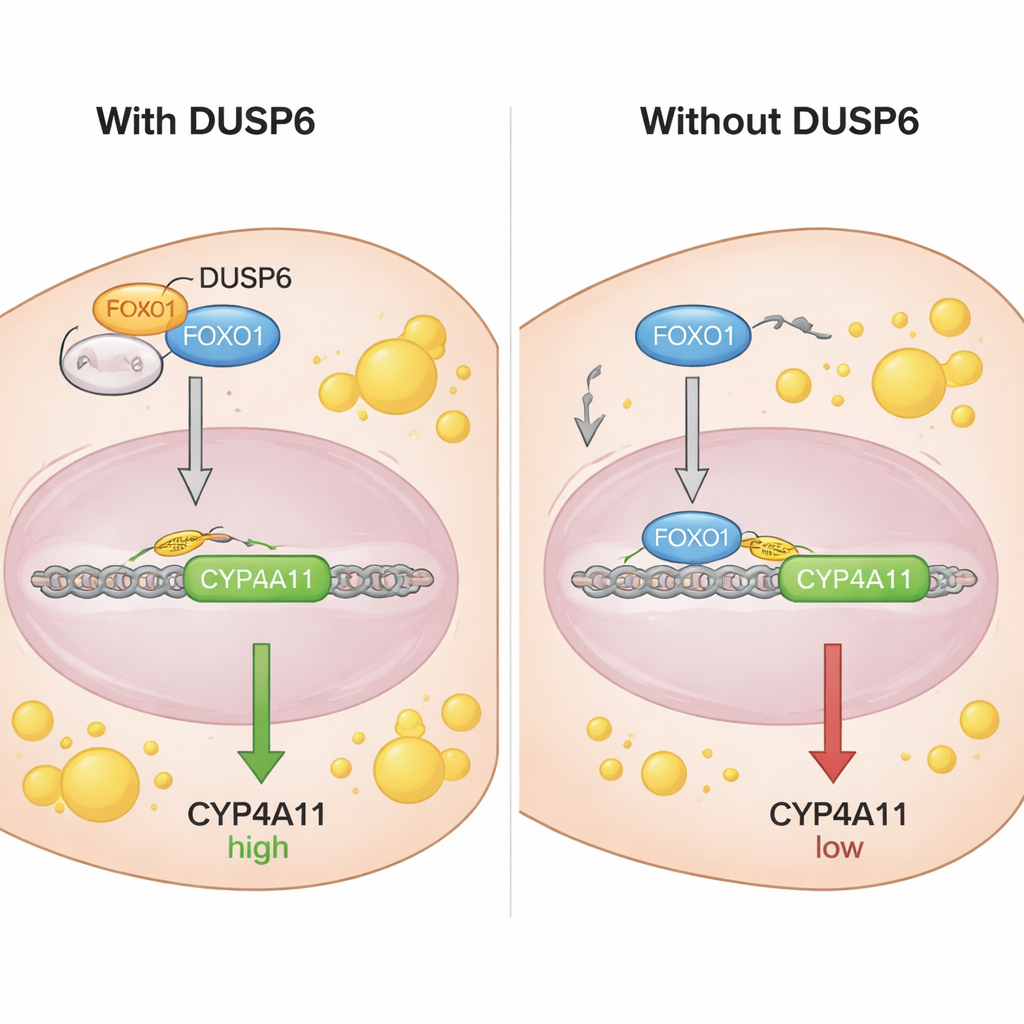
Что это означает для жировой болезни печени и не только
Проще говоря, эта работа описывает цепочку событий внутри печёночных клеток: DUSP6 удерживает FOXO1 в цитоплазме, что ослабляет способность FOXO1 отключать ген CYP4A11. Когда FOXO1 отстранён, CYP4A11 становится более активным, способствуя накоплению жира в клетке и образованию молекул вроде 20‑HETE, которые могут способствовать оксидативному стрессу и воспалению. Хотя эти выводы получены на культивируемых клетках, происходящих из печени, а не на образцах здоровой человеческой печени, они выделяют DUSP6 и CYP4A11 как потенциальные новые мишени для терапии метаболически ассоциированной стеатозной болезни печени. Терапии, которые снижают активность DUSP6 или ослабляют эффекты CYP4A11, теоретически могли бы восстановить тормозящее действие FOXO1 и помочь контролировать жировые отложения в печени.
Цитирование: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Ключевые слова: жировая болезнь печени, DUSP6, FOXO1, CYP4A11, метаболизм печени