Clear Sky Science · ru
Графовая нейронная сеть с физическими соображениями для аппроксимации связывающей аффинности на основе докинга для DYRK2 в репозиционировании препаратов при болезни Альцгеймера
Почему это важно для болезни Альцгеймера
Заболеваемость болезнью Альцгеймера растёт во всём мире, тогда как большинство существующих препаратов лишь смягчают симптомы, но не останавливают болезнь. Лабораторное тестирование новых лекарств занимает много времени и стоит дорого, особенно для малоизученных белков мозга, которые могут играть роль в памяти и здоровье нейронов. В этом исследовании изучается интеллектуальная короткая дорога: использование физически осведомлённой модели искусственного интеллекта для предсказания того, насколько хорошо уже существующие препараты против Альцгеймера могут связываться с малоизученным белком DYRK2, что потенциально открывает новые пути лечения.
Новый взгляд на старые лекарства
Вместо разработки совершенно новых соединений исследователи сосредотачиваются на репозиционировании — поиске новых применений для уже одобренных и относительно безопасных препаратов. Они рассматривают четыре знакомых препарата при Альцгеймере (брексипипразол, донепезил, галантамин и ривастигмин) и оценивают, насколько плотно каждый из них может связываться с DYRK2, белковой киназой, участвующей в росте и функциях нервных клеток. DYRK2 мало изучена в контексте болезни Альцгеймера, но ранние данные связывают её с синапсами, аксонами и памятью, делая её интересной целью, которая могла бы дополнить существующие терапии.
Преобразование молекул в сети
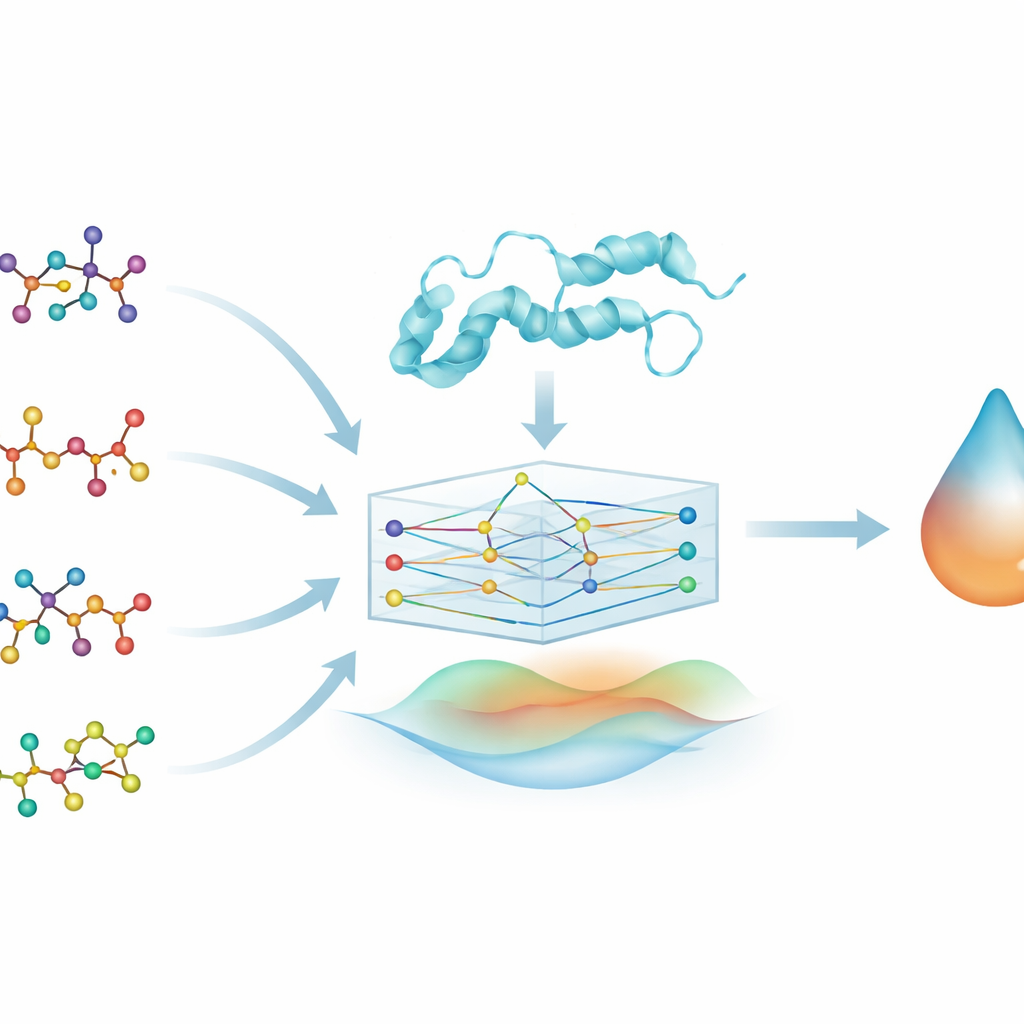
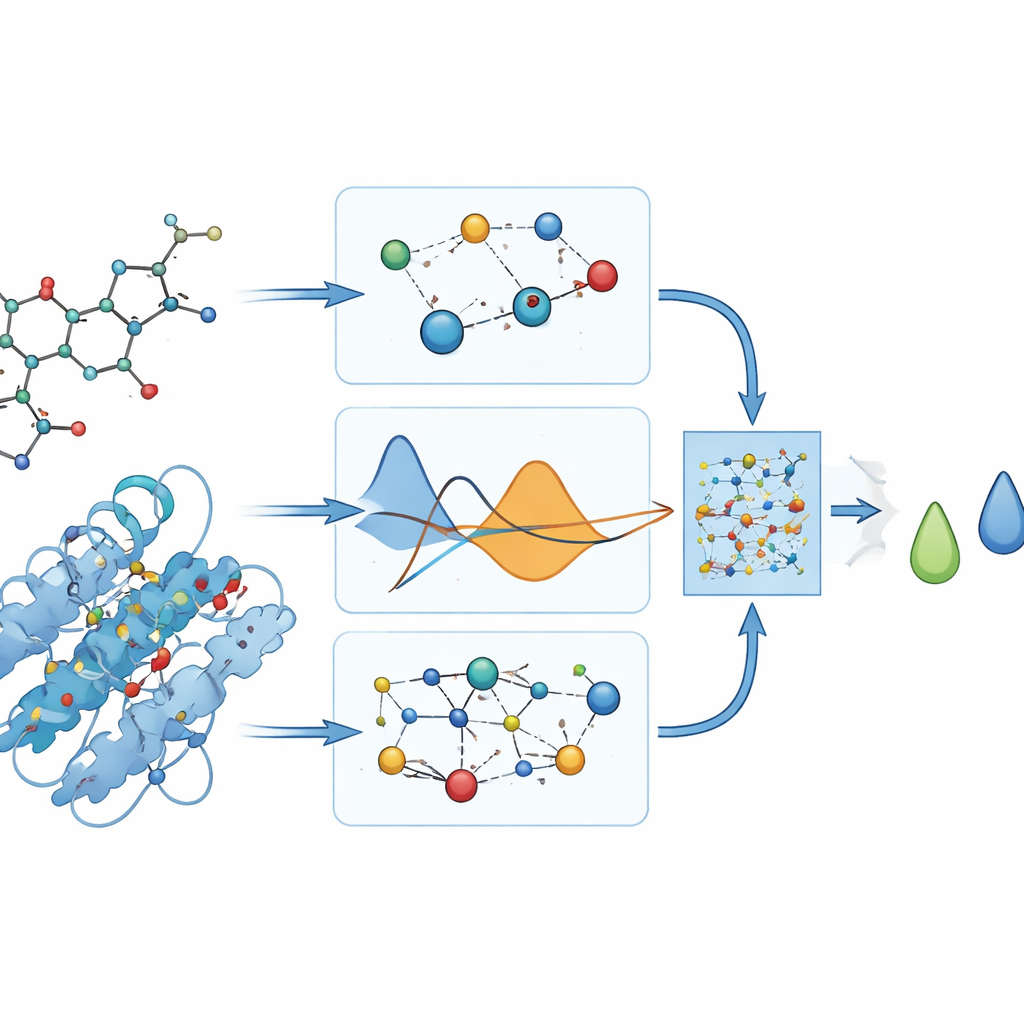
Чтобы исследовать взаимодействия препарат–белок, команда представила каждую молекулу препарата в виде графа: атомы становятся узлами, а химические связи — ребрами между ними. Аналогично они представили белок DYRK2, описав аминокислотную последовательность как цепочку связанных элементов. Тип модели машинного обучения, называемый графовой нейронной сетью (GNN), естественно работает с такими графовыми входами, передавая информацию по связям и выявляя закономерности в форме и химии. Это позволяет модели, названной PhysDual‑GCN, «читать» и препарат, и DYRK2 как взаимодействующие сети, а не как простые строки или списки признаков.
Смешение физики с искусственным интеллектом
Большинство инструментов глубинного обучения в разработке лекарств учатся только на данных, что затрудняет интерпретацию их внутренней логики. Здесь авторы целенаправленно вводят базовые физические идеи о взаимодействиях атомов. Наряду с извлекаемыми графовыми признаками PhysDual‑GCN вычисляет два классических энергетических члена: один отражает электрическое притяжение и отталкивание между частичными зарядами, а другой описывает силы ван‑дер‑Ваальса. Эти физически обоснованные энергии комбинируются с внутренним представлением GNN перед выдачей предсказанной силы связывания. Фактически модель обучают имитировать поведение стандартных программ докинга — в частности AutoDock Vina и родственных инструментов — но работать быстрее и при этом оставаться привязанной к понятным физическим принципам.
Что на самом деле предсказывает модель
Поскольку лабораторных измерений силы связывания этих препаратов с DYRK2 нет, авторы опираются на программы докинга, которые дают «опорные» оценки связывания в единицах энергии. Они тщательно избегают использования этих оценок в процессе обучения и используют их только впоследствии для оценки того, насколько хорошо PhysDual‑GCN выучила закономерности. Для четырёх препаратов при Альцгеймере модель воспроизводит значения докинга с малыми средними ошибками (около трети килокалории на моль) и правильно ранжирует соединения: донепезил и брексипипразол оказываются сильнейшими лигандами, тогда как галантамин и ривастигмин выглядят слабее, но всё ещё относительно стабильными. Эти результаты показывают, что физически информированная GNN может служить вычислительным суррогатом для более медленных запусков докинга.
Обещания и ограничения подхода
Несмотря на обнадёживающие цифры, авторы подчёркивают строгие границы своего исследования. Проанализированы лишь четыре препарата, и все оценки опираются на другие компьютерные программы, а не на реальные биохимические эксперименты. Белок DYRK2 моделируется главным образом как одномерный граф последовательности, а не как полная трёхмерная структура, поэтому модель ещё не может учесть детальную форму карманов связывания. Сами физические энергии упрощены, используются стандартные параметры силовых полей и отсечки. В результате работу следует рассматривать как демонстрацию концепции: она показывает, что графовые нейронные сети, руководимые физикой, могут близко повторять классические оценки докинга в условиях малого объёма данных, но ещё не доказывает, что прогнозы соответствуют реальности в пробирке или клинике.
Что это означает для будущих исследований болезни Альцгеймера
Для неспециалистов главный вывод таков: интеллектуальные алгоритмы с учётом физических принципов могут помочь учёным быстрее, чем традиционные методы в одиночку, исследовать новые мишени при Альцгеймере, такие как DYRK2. Выделяя донепезил и брексипипразол как перспективные связывающие молекулы DYRK2 и предлагая прозрачный способ аппроксимации результатов докинга, PhysDual‑GCN даёт отправную точку для более глубоких лабораторных исследований. С расширением библиотек препаратов, обогащением 3D‑информации о белках и экспериментальной валидацией такие модели могут стать практическим инструментом для скрининга кандидатов и руководства репозиционированием препаратов с целью замедления или изменения течения болезни Альцгеймера.
Цитирование: Gider, V., Budak, C. A physics-informed graph neural network to approximate docking-based binding affinity for DYRK2 in Alzheimer’s drug repurposing. Sci Rep 16, 8357 (2026). https://doi.org/10.1038/s41598-026-35102-7
Ключевые слова: болезнь Альцгеймера, репозиционирование лекарств, графовые нейронные сети, связывание белок–лиганд, киназа DYRK2