Clear Sky Science · ru
Кристаллическая структура цистатина B Echinococcus multilocularis выявляет новую особенность в классических стефиных
Почему «секретное оружие» печёночного паразита важно
Альвеолярный эхинококкоз — громоздкое название для крошечной тени глиста, которая в печени ведёт себя подобно медленно растущей опухоли. Заболевание часто смертельно, существующие лекарства действуют плохо и могут вызывать серьёзные побочные эффекты. В этом исследовании рассматривается одна конкретная молекула, производимая паразитом — белок EmCystatin-B — чтобы понять, как она помогает червю уклоняться от защитных механизмов хозяина, и как впоследствии её можно было бы использовать в качестве мишени для новых препаратов.
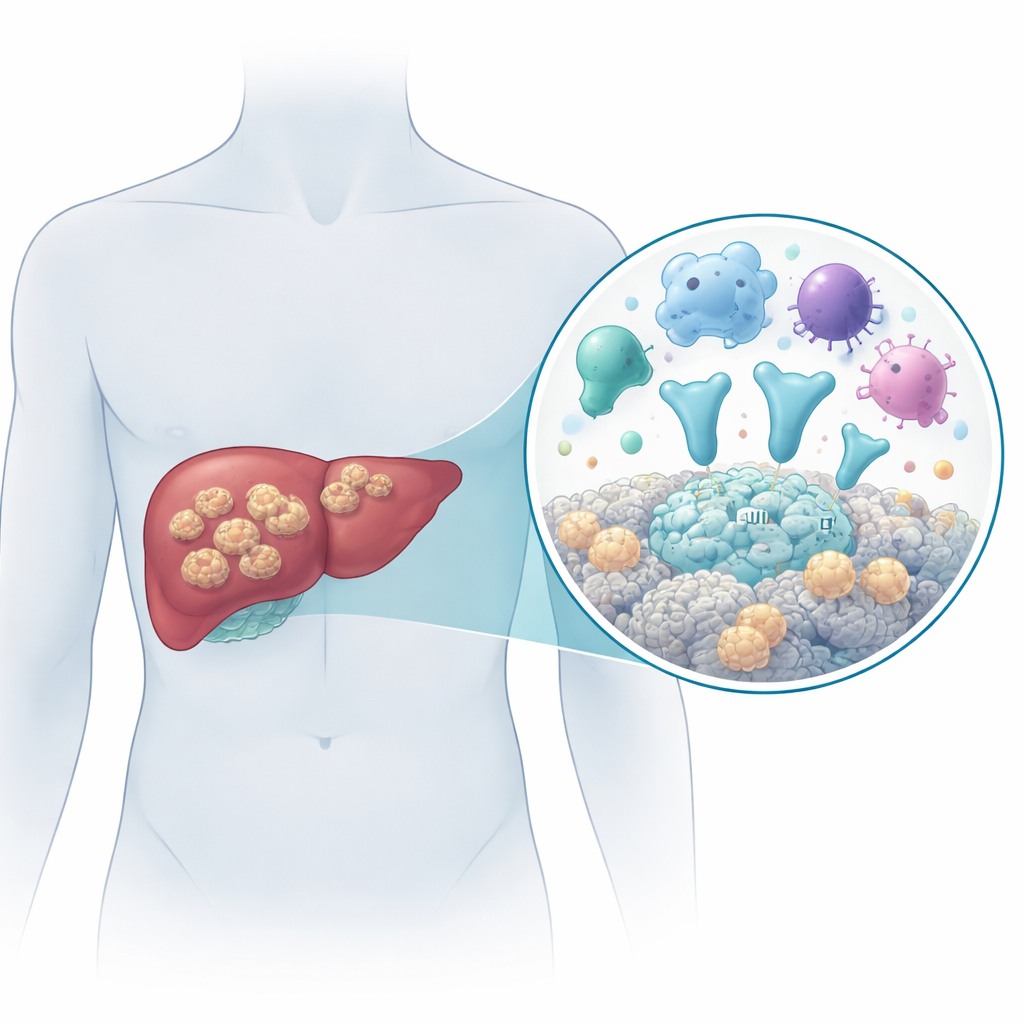
Опасный цепень, растущий как опухоль
Заболевание вызывается личиночной стадией цепня Echinococcus multilocularis. Люди заражаются при случайном проглатывании яиц паразита, например с загрязнённой пищей или водой. Попав в организм, личинки оседают в основном в печени и разрастаются в многочисленные крошечные заполненные жидкостью пузырьки, проникающие в окружающие ткани, распространяющиеся в близлежащие органы, такие как селезёнка, и иногда достигающие отдалённых участков — лёгких или мозга. Без эффективного лечения более 9 из 10 пациентов умирают в течение 10–15 лет. В настоящее время лучшим вариантом является хирургическое вмешательство в сочетании с длительной антипаразитарной терапией, но ранняя диагностика затруднена, а лекарства не дают надёжного излечения. Поэтому крайне важно понимать, как паразит взаимодействует с человеческим организмом на молекулярном уровне.
Паразитический белок, обезвреживающий режущие ферменты
Многие животные, включая человека, производят семейство белков, называемых цистатинами, которые служат предохранителями для мощных пищеварительных ферментов — цистеиновых протеаз. Эти ферменты расщепляют другие белки и важны для процессов вроде удаления старых компонентов клетки и активации иммунного ответа. Паразиты научились синтезировать похожие на цистатины белки, чтобы вмешиваться в работу ферментов и иммунной системы хозяина. В этой работе исследователи идентифицировали цистатиноподобный белок из E. multilocularis и назвали его EmCystatin-B. Они обнаружили, что ген EmCystatin-B значительно активнее в зрелых головках личинок (протосколекусах) по сравнению с тканью кисты, а сам белок присутствует в цитоплазме и ядре клеток паразита, особенно в делящихся «стволоподобных» герминативных клетках. Лабораторные тесты показали, что EmCystatin-B способен сильно блокировать активность человеческой катепсины B — важной цистеиновой протеазы, задействованной в иммунитете и ремоделировании тканей.
Знакомая форма с неожиданным поворотом
Чтобы точно выяснить строение EmCystatin-B, команда кристаллизовала очищенный белок и использовала рентгеновскую кристаллографию для решения его трёхмерной структуры с почти атомным разрешением. Как и другие представители семейства цистатинов, каждый субъединица EmCystatin-B имеет характерную форму: центральный спиральный сегмент, поддерживаемый несколькими плоскими, лентовидными бета-цепями, образующими клин, который обычно входит в активный центр протеазы. По последовательности и отсутствию явного сигнального пептида для секреции EmCystatin-B относится к подгруппе «стефины», которые обычно маленькие внутриклеточные белки и не содержат стабилизирующих дисульфидных связей. Удивительно, но структура показала, что хотя каждая единица EmCystatin-B имеет ожидаемую складку, способ их ассоциации друг с другом необычен и специфичен для вида по сравнению с человеческим аналогом, цистатином B.
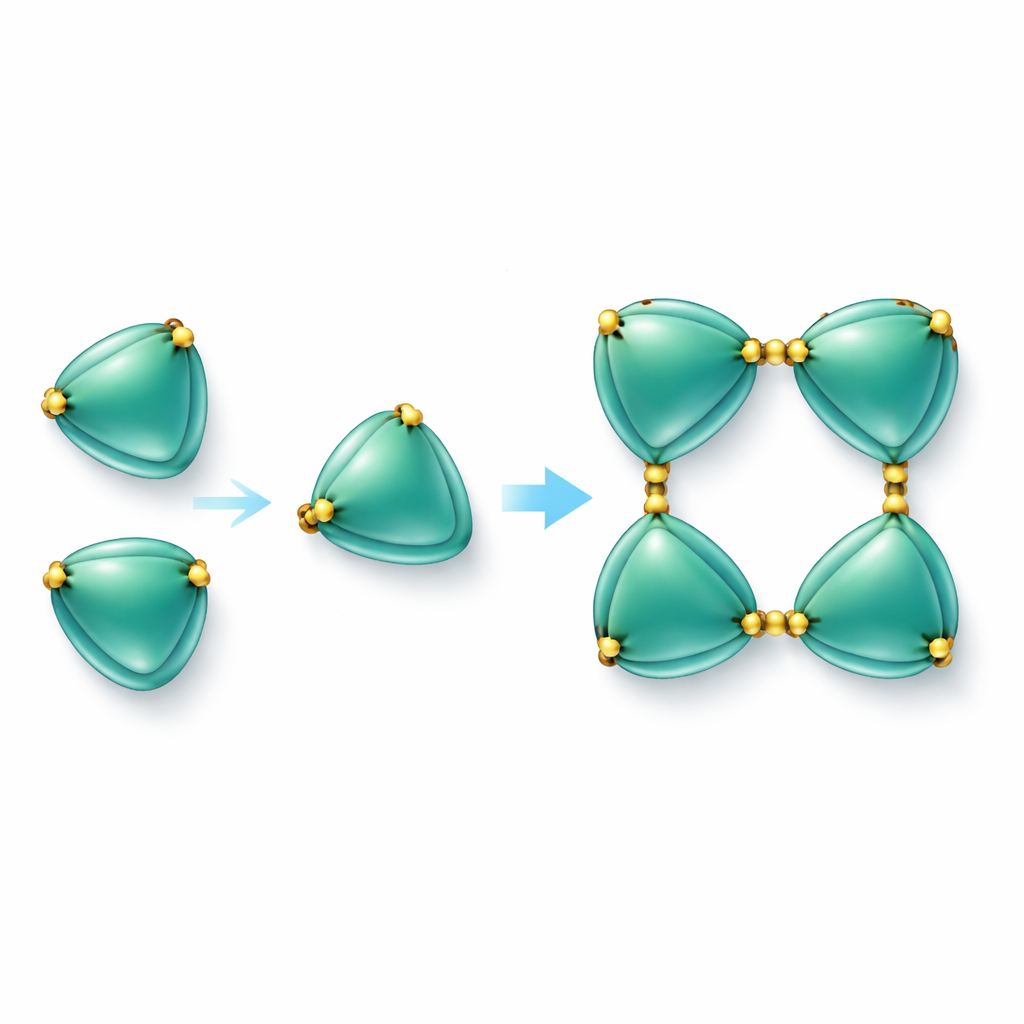
Сборка белковых цепочек с сернистыми связями
Самым поразительным открытием было то, что молекулы EmCystatin-B не существуют просто как отдельные единицы. Вместо этого они могут соединяться поэтапно, формируя димеры (пары), а затем тетрамеры (группы из четырёх). Две разные механики способствуют образованию начальных димеров. В одном случае фрагмент одной молекулы «раскрывается» и дополняет структуру соседней — явление, известное как обмен доменами (domain swapping). В другом случае пары молекул связаны дисульфидными мостиками — прочными химическими связями между серосодержащими аминокислотами (цистеинами). В EmCystatin-B цистеин на позиции 4 одной молекулы связывается с цистеином на позиции 76 партнёра. Четыре таких поперечных связки затем стабилизируют тетрамер. Применение нескольких межмолекулярных дисульфидных мостиков полностью ново для классических стефин, которые обычно лишены таких связей. Когда исследователи заменили эти ключевые цистеины на другую аминокислоту, белок больше не мог эффективно собираться в высокоорганизованные комплексы, и его способность ингибировать катепсин B резко снизилась.
Что это значит для борьбы с инфекцией
Для неспециалиста главный вывод в том, что паразит выработал специально сконструированную версию распространённого семейства белков, используя дополнительные химические «заклёпки» для фиксации нескольких единиц ингибитора вместе. Эта олигомерная форма, по-видимому, важна для подавления фермента хозяина, который в противном случае способствовал бы контролю инфекции. Раскрывая точную архитектуру EmCystatin-B и его уникальные дисульфид-связанные сборки, исследование расширяет наше понимание того, как цистатины могут быть настроены у разных видов. В долгосрочной перспективе эти данные могут помочь в разработке препаратов, которые либо блокируют защитный эффект EmCystatin-B для ослабления паразита, либо имитируют его иммунозатухающее действие для лечения воспалительных заболеваний.
Цитирование: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Ключевые слова: альвеолярный эхинококкоз, Echinococcus multilocularis, цистатин B, структура белка, модуляция иммунитета