Clear Sky Science · ru
Нарушение сборки инфламмасомы NLRP3 через лиганд-индуцируемое ремоделирование интерфейсов пиринового домена
Почему важно усмирять неконтролируемое воспаление
Многие хронические заболевания — от артрита и подагры до сердечно-сосудистых и нейродегенеративных расстройств — подпитываются чрезмерно активной системой иммунного «тревожного сигнала» внутри клеток. Ключевым элементом этого сигнала является инфламмасома NLRP3, которая помогает бороться с инфекциями, но при сбое может вызывать вредное воспаление. В этой работе описана новая малая молекула, названная E9, которая нацелена на ранний этап активации NLRP3, предлагая новый подход к разработке лекарств, способных охлаждать патологическое воспаление, не подавляя полностью иммунную систему.
Клеточная пожарная сигнализация с темной стороной
Когда организм ощущает опасность, иммунные клетки собирают инфламмасому NLRP3 — большой белковый комплекс, действующий как молекулярная пожарная сигнализация. После формирования этот комплекс активирует фермент каспазу-1, которая, в свою очередь, включает мощные провоспалительные медиаторы, включая цитокины IL-1β и IL-18. Эти сигналы необходимы для борьбы с инфекциями и удаления повреждённых тканей. Однако если инфламмасома остаётся активной слишком долго или включается в неподходящее время, она способствует хроническим воспалительным состояниям, поражающим суставы, сосуды, мозг и другие органы. Поэтому учёные по всему миру ищут точные способы контролировать NLRP3, не подавляя при этом иммунитет в целом.
Ищем дальше, чем обычные цели для лекарств
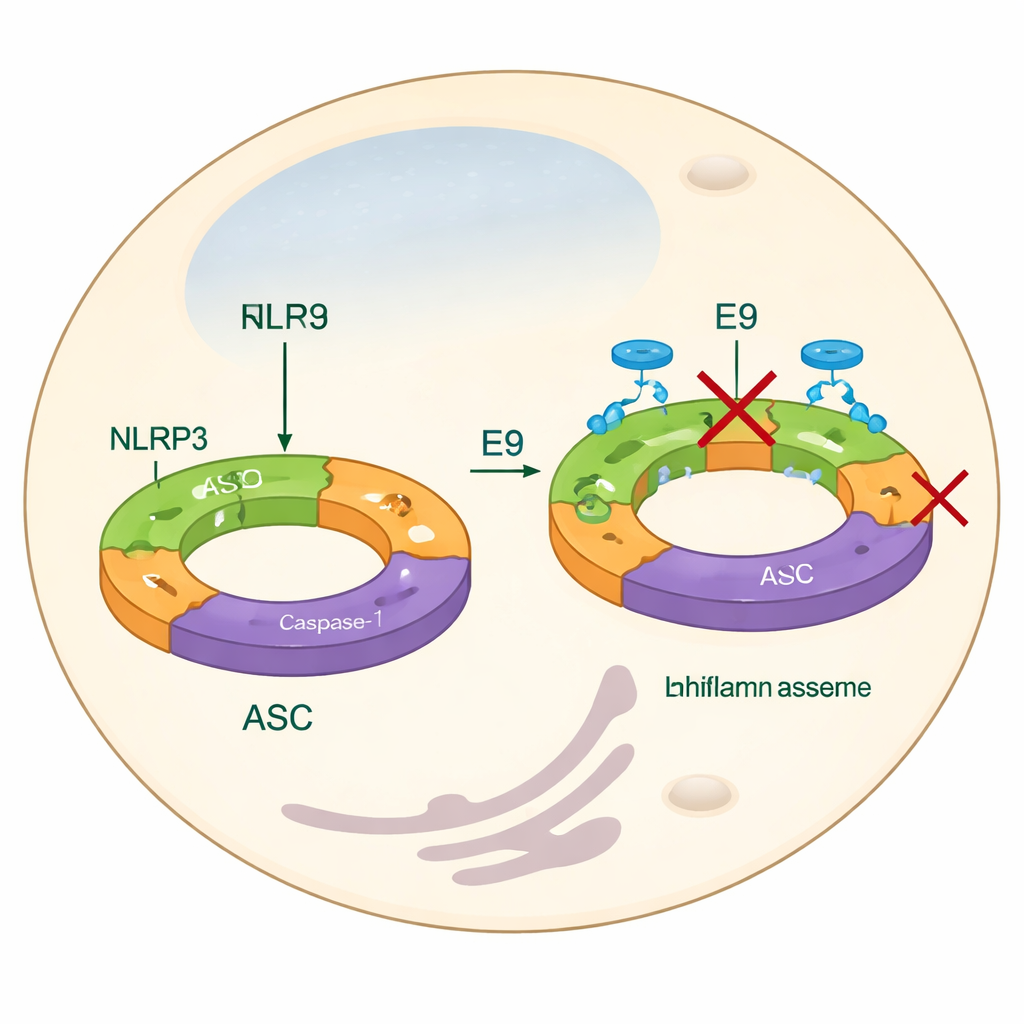
Большинство текущих стратегий по усмирению NLRP3 нацелены на блокирование его конечных продуктов — например, IL-1β — или на вмешательство в центральный домен, использующий энергоносители вроде ATP. Хотя такие подходы могут быть эффективны, они упускают самые ранние этапы сборки и не полностью объясняют, как белки NLRP3 объединяются в функциональную машину. В этой работе авторы сфокусировались на пириновом домене — части NLRP3, которая помогает отдельным субъединицам сцепляться в длинные филаменты. Эти филаменты затем привлекают адаптерный белок ASC, который собирается в яркие «спеки» внутри клеток — визуальный признак активации инфламмасомы. Нахождение соединений, препятствующих правильному сопряжению пириновых доменов, должно помешать образованию инфламмасомы на самых ранних этапах.
Поиск молекулы, разрывающей цепь
Исследователи отскринировали библиотеку из 1500 недавно синтезированных малых молекул с помощью хитрого светочувствительного теста. Они слили разрезанные фрагменты люциферазного фермента с пириновым доменом NLRP3; когда два пириновых домена сближались, фрагменты фермента собирались и излучали свет. Соединения, блокирующие пирин–пириновые контакты, вызывали падение светового сигнала. Из этого скрининга были выделены четыре перспективных кандидата, среди которых одна — E9 — выделялась сильным и стабильным ингибирующим эффектом. Дополнительные измерения, выполненные методом микроскалярной термопорезы, показали, что E9 прочно связывается с пириновым доменом при очень низких (субмикромолярных) концентрациях, что подтверждает, что эффект обусловлен специфическим взаимодействием, а не случайным артефактом.
Наблюдение эффекта в живых клетках
Чтобы проверить, работает ли E9 в живой системе, команда использовала человеческие иммуноподобные клетки, генетически модифицированные для экспрессии флуоресцентной версии ASC. Когда эти клетки стимулируют бактериальными компонентами и вторым триггером, NLRP3 включается, и белки ASC聚集аться в яркие спеки, которые можно посчитать под микроскопом. В присутствии E9 число таких спеках существенно снизилось, сопоставимо или лучше, чем при использовании некоторых известных ингибиторов NLRP3. Это показало, что вмешательство в контакты пириновых доменов достаточно для уменьшения сборки инфламмасомы и ранних этапов воспалительной клеточной смерти, по крайней мере в лабораторных условиях.
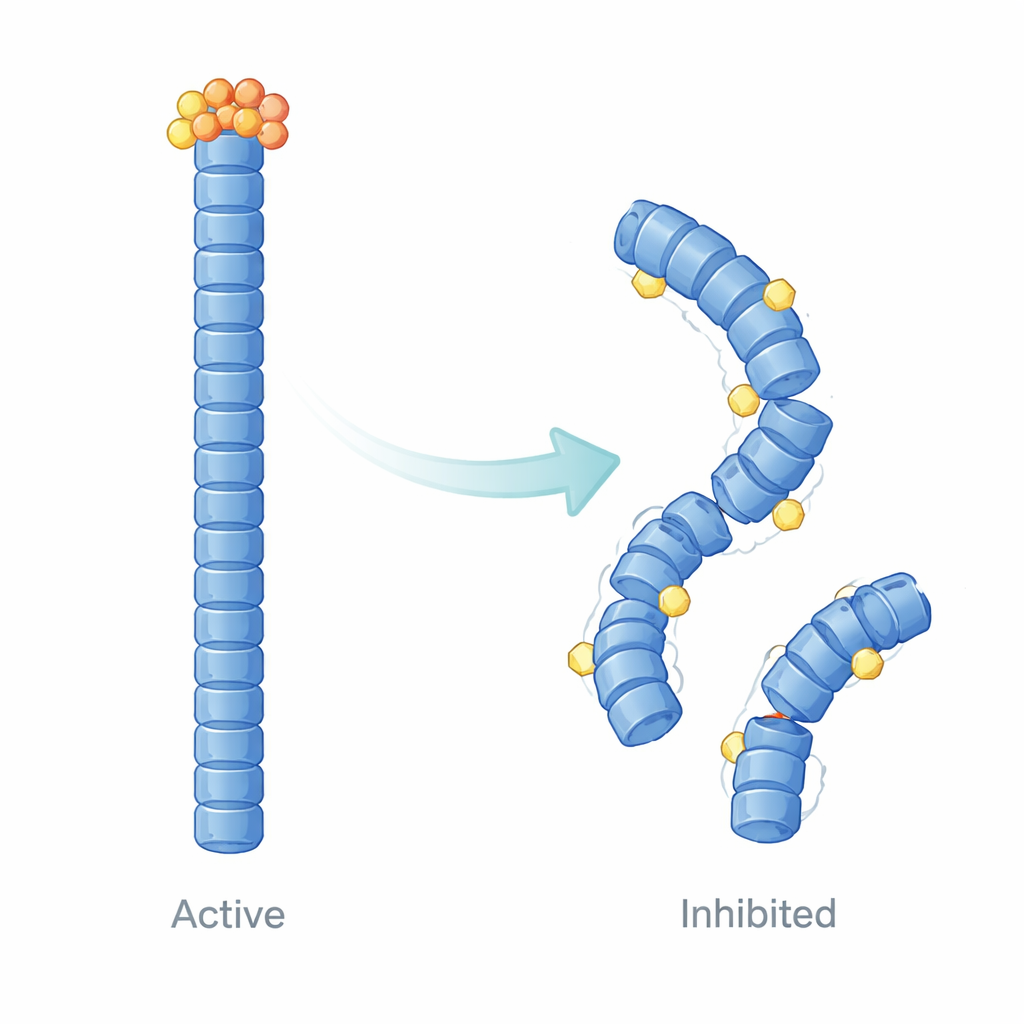
Как E9 преобразует каркас инфламмасомы
Помимо измерения связывания, авторы использовали компьютерное структурное моделирование и молекулярно-динамические симуляции, чтобы визуализировать, как E9 изменяет поведение филаментов NLRP3 с течением времени. Их расчёты указывают, что E9 локализуется на специфических контактных поверхностях между пириновыми доменами, ненавязчиво ослабляя и перестраивая филамент. Вместо однородно стабильной кооперативной структуры филамент становится неравномерным: участки рядом с связанным E9 становятся более гибкими и теряют точную выверенность, тогда как другие части оказываются динамически изолированными. Эти сдвиги ослабляют крупномасштабные движения и плотное взаимодействие, необходимые для эффективного привлечения ASC, предлагая физическое объяснение уменьшения образования спец в клетках.
Что это может значить для будущих терапий
В сумме результаты представляют E9 как прототип нового класса препаратов, нацеленных на инфламмасому путем нарушения интерфейсов между строительными блоками NLRP3, а не через блокирование её энергопотребления или конечных продуктов. Хотя текущая работа ограничена испытаниями в пробирке, компьютерными моделями и культурами клеток — и требуются дальнейшие исследования на животных и людях — она демонстрирует, что тщательно спроектированные малые молекулы могут ремоделировать сам каркас инфламмасомы. Для пациентов с заболеваниями, вызванными неконтролируемым воспалением, такие препараты, нацеленные на интерфейсы, могут в будущем предложить более точный контроль, уменьшая вредную активацию иммунитета при сохранении жизненно важных защитных функций.
Цитирование: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Ключевые слова: инфламмасома NLRP3, пиринный домен, ингибитор малой молекулы, врожденный иммунитет, пироптоз