Clear Sky Science · ru
TTF2 как потенциальный биомаркер и цель иммунотерапии при диагностике и прогнозировании глиомы
Почему это исследование рака мозга важно
Глиомы — опухоли мозга, одни из самых смертоносных злокачественных новообразований, при которых большинство пациентов живут всего несколько лет после постановки диагноза. Врачи срочно нуждаются в более точных способах прогнозирования течения болезни и в поиске новых терапевтических мишеней, особенно для современных иммунных методов лечения. В этом исследовании внимание сосредоточено на малоизвестной молекуле TTF2 и поставлен простой, но значимый вопрос: могут ли уровни TTF2 в опухолях мозга помочь врачам точнее диагностировать глиому, прогнозировать выживаемость и даже направлять будущие подходы иммунотерапии?
Новый сигнал, скрытый в генах опухоли
Глиома — не единое заболевание, а группа различающихся по скорости роста и ответу на лечение опухолей мозга. Нынешние методы, такие как микроскопическое исследование и несколько генетических маркеров, не могут полностью объяснить, почему некоторые пациенты чувствуют себя лучше, а у других состояние быстро ухудшается. Исследователи обратились к крупным общедоступным базам данных геномики рака из США и Китая в поисках дополнительных молекулярных подсказок. Они сосредоточились на TTF2 — белке, участвующем в выключении активности генов, который связывали с несколькими другими типами рака, но который ранее не изучали подробно в глиоме.
Высокий TTF2 — повышенный риск
Сравнив тысячи образцов, команда обнаружила, что уровни TTF2 значительно выше в тканях глиомы по сравнению с нормальным мозгом. Внутри глиом опухоли с наибольшим содержанием TTF2, как правило, были более прогрессирующими, относились к более агрессивным подтипам и встречались у пациентов старшего возраста. При анализе исходов пациентов прослеживалась четкая закономерность: у людей с опухолями, содержащими больше TTF2, как правило, была более короткая общая выживаемость и более частое прогрессирование заболевания. Даже после учета мощных существующих маркеров — таких как степень опухоли, мутация IDH и хромосомное изменение 1p/19q — TTF2 сохранял статус независимого предупреждающего признака. Группа построила прогностическую шкалу, объединяющую TTF2 с этими стандартными факторами, которая тесно соответствовала фактической выживаемости на один, три и пять лет в двух отдельных наборах данных пациентов.
Подсказки из окружения опухоли
Чтобы понять, почему TTF2 может быть связан с плохими исходами, исследователи изучили, какие другие гены коррелируют с ним по экспрессии и какие биологические процессы отражают эти наборы генов. В опухолях с высоким уровнем TTF2 была усилена активность путей, связанных с иммунной сигнальной передачей, производством антител и клеточно‑клеточной коммуникацией, а также знакомых онкологических маршрутов, таких как PI3K–AKT. С помощью вычислительных инструментов, которые по шаблонам экспрессии генов дают оценку состава иммунных клеток, они затем проанализировали микроокружение опухоли. Глиомы с высоким TTF2 также были богаты определенными иммуно-клетками — Th2‑хелперами, макрофагами и нейтрофилами — которые часто ассоциируются с «приглушенным» или подавленным противоопухолевым ответом, и имели меньше плазмоцитоидных дендритных клеток, способных усиливать иммунный ответ.
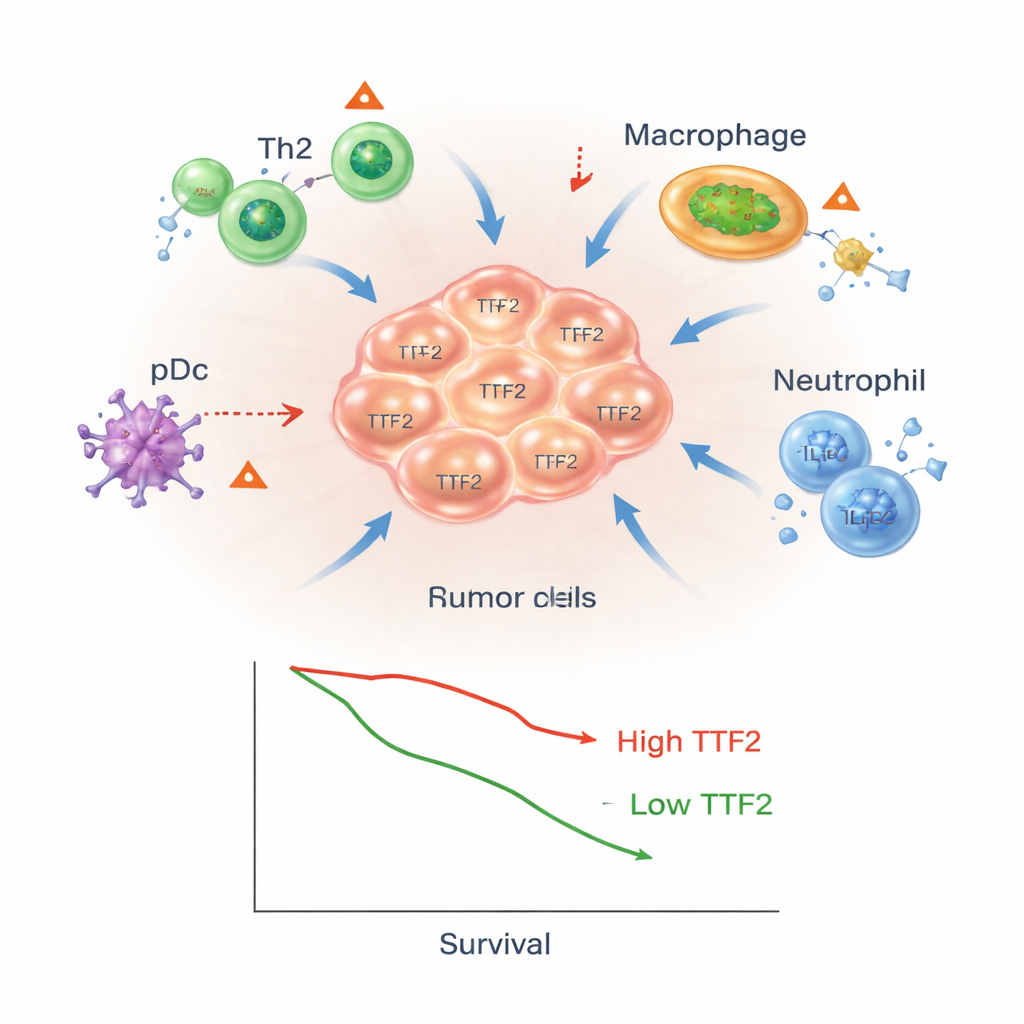
Как TTF2 может помогать опухолям прятаться
Эти результаты указывают на то, что TTF2 делает больше, чем просто отмечает опасные опухоли; он может активно способствовать формированию защитной оболочки вокруг них. Авторы предполагают, что, влияя на механизмы выключения генов, TTF2 может изменять уровни ключевых иммунных медиаторов и хемокинов — молекул, привлекающих или отталкивающих иммунные клетки. Это, в свою очередь, может смещать Т‑клеточный ответ в сторону доминирования Th2, менее эффективного для уничтожения раковых клеток, и содействовать накоплению макрофагов и нейтрофилов, поддерживающих опухоль. Хотя эти идеи основаны на анализе данных, а не на прямой лабораторной модуляции TTF2, они предлагают проверяемую модель того, как эта молекула может способствовать росту опухоли и иммунному уклонению.
Что это значит для пациентов
Авторы заключают, что TTF2 сильно сверхэкспрессирован в глиомах и что более высокие уровни надежно ассоциируются с худшей выживаемостью и более агрессивными чертами болезни. Для пациентов это открывает два обнадеживающих направления. Во‑первых, измерение TTF2 в образцах опухоли может помочь врачам улучшить диагностику и персонализировать оценки риска сверх того, что дают стандартные тесты сегодня. Во‑вторых, если будущие лабораторные исследования подтвердят, что TTF2 помогает опухолям уклоняться от иммунной системы, препараты, блокирующие или модулирующие TTF2 — либо его дальнейшие пути — могут стать частью новых комбинированных терапий, делающих иммунотерапию более эффективной для пациентов с этим разрушительным раком мозга.
Цитирование: Shi, D., Chen, F., Chen , Z. et al. TTF2 as a potential biomarker and immunotherapy target in glioma diagnosis and prognosis. Sci Rep 16, 7653 (2026). https://doi.org/10.1038/s41598-026-35049-9
Ключевые слова: глиома, TTF2, биомаркер опухоли мозга, иммунная микроокружение опухоли, цель иммунотерапии