Clear Sky Science · ru
Структурная основа действия диосгенина как обратного агониста орфанного рецептора, связанного с ретиноевой кислотой γ
Почему важно растение и переключатель иммунитета
Многие хронические заболевания — от аутоиммунных, таких как рассеянный склероз и псориаз, до ожирения и сахарного диабета 2‑го типа — вызваны чрезмерной активностью иммунных сигналов и нарушениями метаболических сигналов. Учёные давно ищут более безопасные препараты, которые могли бы точно регулировать эти сигналы. В этом исследовании показано, как диосгенин, натуральная молекула, содержащаяся в некоторых лекарственных растениях и ямсе, связывается с белком, регулирующим иммунитет, называемым RORγ, и переводит его в менее активное состояние. Понимание этого взаимодействия на атомном уровне может открыть путь к более мягким и целенаправленным терапиям, основанным на знакомом растительном скелете молекулы.
Мастер‑регулятор иммунитета и метаболизма
RORγ относится к большой семье «ядерных рецепторов» — белков внутри клетки, которые включают или выключают гены в ответ на небольшие молекулы. Этот белок является ключевым регулятором группы иммунных клеток, известных как Th17, которые вырабатывают провоспалительный сигнал IL‑17A и связаны с аутоиммунными болезнями, такими как рассеянный склероз, псориаз, ревматоидный артрит и болезнь Крона. RORγ также влияет на развитие жировых клеток и реакцию организма на инсулин, связывая его с ожирением и диабетом. Благодаря такому широкому влиянию RORγ стал привлекательной мишенью для лекарств, однако многие синтетические молекулы, связывающиеся с ним, столкнулись с проблемами безопасности, селективности или эффективности у людей.
Традиционное средство дает перспективный лид
Диосгенин — стероидоподобная молекула, извлекаемая из растений, включая виды Dioscorea (дикой ямс) и несколько традиционных лекарственных трав. Его изучали на предмет противовоспалительного, противоопухолевого, антидиабетического и кардиоваскулярного действия в клеточных и животных моделях. Предыдущие работы предполагали, что диосгенин может влиять на путь RORα/γ и подавлять вредные ответы Th17, но было неясно, взаимодействует ли он напрямую с RORγ и как именно изменяет поведение белка. Чтобы выяснить это, авторы просcreenировали библиотеку природных соединений с помощью чувствительного анализа связывания и идентифицировали диосгенин как сильный лигант, связывающийся с лигандсвязывающим участком RORγ.
Как диосгенин переводит RORγ в обратное состояние
Исследователи изучили, как диосгенин влияет на способность RORγ привлекать вспомогательные белки, которые либо усиливают (коактиваторы), либо ослабляют (корепрессоры) активность генов. Удивительно, но диосгенин способствовал связыванию RORγ с обоими типами партнёров, что отличалось от поведения известного природного антагониста урсоловой кислоты. В клеточных тестах‑репортёрах, отслеживающих переключение генов, диосгенин последовательно снижал активность, управляемую RORγ, в дозозависимой манере с эффективностью в субмикромолярном диапазоне. Такое поведение соответствует профилю «обратного агониста»: соединения, которое не только блокирует базовую активность, но и активно переводит рецептор в выключенное состояние, даже когда он иначе был бы активирован.
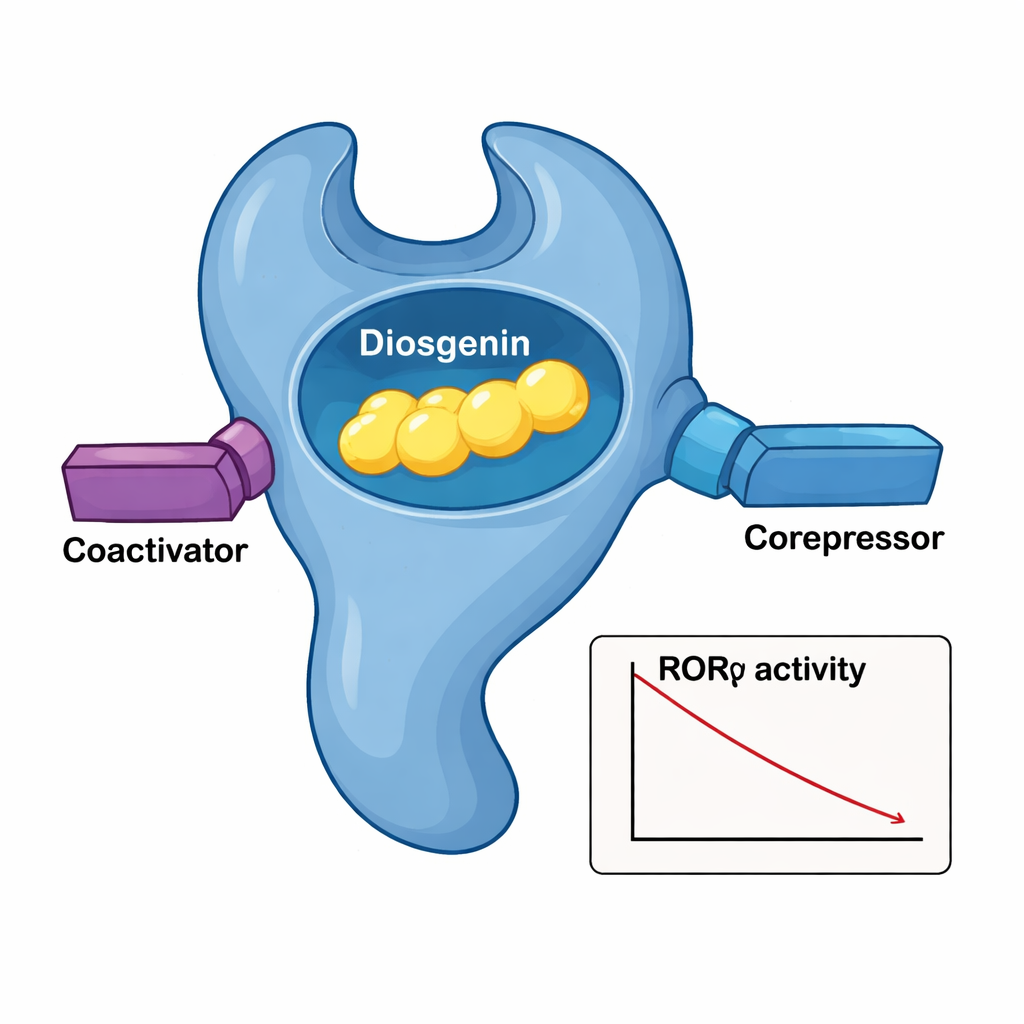
Крупный план молекулярного рукопожатия
Чтобы увидеть, как именно диосгенин помещается в RORγ, команда решила трёхмерную кристаллическую структуру лигандсвязывающего домена белка с диосгенином внутри. Рецептор сворачивается в многослойный пучок спиралей, образуя карман, который охватывает стероидоподобное тело диосгенина. Сеть плотных гидрофобных контактов от нескольких аминокислот действует как подобранная перчатка вокруг скелета молекулы, в то время как критическая гидроксильная группа диосгенина образует водо‑опосредованные водородные связи с двумя остатками аргинина. При поочерёдном изменении этих остатков в кармане способность диосгенина подавлять RORγ снижалась, что подтвердило их важность. Структурное сравнение с комплексом RORγ–урсоловой кислоты показало, что диосгенин удерживает ключевую хвостовую спираль (AF‑2) в «активоподобной» позиции, даже при том что он в целом снижает транскрипционную активность, что объясняет, почему он одновременно привлекает и коактиваторы, и корепрессоры.
От кристаллической структуры к будущим лекарствам
Подробная картина взаимодействия диосгенина с RORγ выделяет два заметных преимущества для дизайна лекарств. Во‑первых, карман рецептора достаточно гибок, чтобы распознавать лигандные формы разной геометрии, что даёт химикам возможность тонко настраивать скелет диосгенина для повышения селективности в отношении RORγ и снижения нежелательного связывания с другими ядерными рецепторами. Во‑вторых, натуральное происхождение диосгенина и известная низкая собственная токсичность в доклинических моделях делают его привлекательной отправной точкой по сравнению с некоторыми полностью синтетическими соединениями, остановившимися в клинических испытаниях. Проще говоря, эта работа показывает, как растительная молекула может сцепиться с центральным иммунным и метаболическим переключателем и перевести его в обратное состояние, предлагая структурный шаблон для разработки более безопасных и эффективных средств от заболеваний, связанных с RORγ.
Цитирование: Chen, S., Tian, S., Liang, J. et al. Structural basis for diosgenin as an inverse agonist of retinoic acid receptor-related orphan receptor γ. Sci Rep 16, 4765 (2026). https://doi.org/10.1038/s41598-026-35006-6
Ключевые слова: ROR gamma, диосгенин, аутоиммунное заболевание, ядерный рецептор, обратный агонист