Clear Sky Science · ru
Феноменологическая модель стабилизации транстиретина
Почему это важно для пациентов и семей
Амилоидоз транстиретина — серьезное состояние, при котором обычный белок крови, транстиретин (ТТР), распадается, и его фрагменты могут образовывать вредные отложения в сердце и нервах. Новые препараты, такие как тафамидис и акорамидис, разработаны, чтобы удерживать этот белок в безопасной четырехсубъединичной форме, и уже улучшили исходы у многих пациентов. Тем не менее врачи наблюдают загадочный эффект у лечащихся пациентов: концентрация ТТР в крови повышается более чем на 30%, и причина этого неочевидна. В этой работе используется упрощенная математическая модель, чтобы исследовать, что может происходить в организме и что это означает для механизма действия этих лекарств. 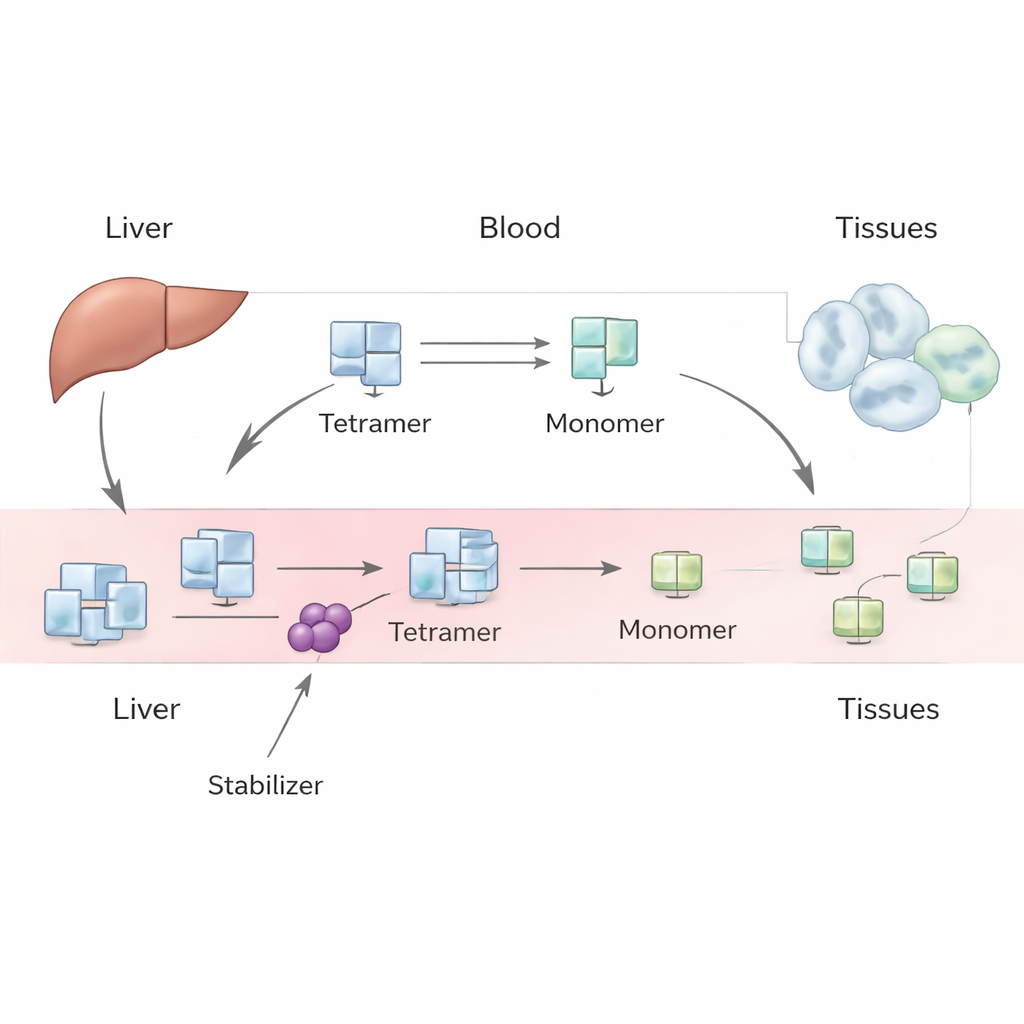
Белок, который может помогать и вредить
ТТР синтезируется преимущественно в печени и обычно циркулирует в крови как стабильный тетрамер — связка из четырех одинаковых субъединиц. Он транспортирует гормон щитовидной железы и витамин A. При определенных условиях, включая старение или наследственные варианты генов, этот тетрамер может распадаться на отдельные субъединицы — мономеры. Мономеры могут неправильно сворачиваться и слипаться в амилоидные фибриллы, повреждающие ткани и приводящие к амилоидозу транстиретина сердца (кардиомиопатии) или нервов (нейропатии). Лекарства вроде тафамидиса и акорамидиса предназначены для связывания тетрамера и повышения его устойчивости к распаду, замедляя прогрессирование болезни. Однако при начале терапии у пациентов измеряемые уровни ТТР в крови надежно повышаются, и это повышение больше, чем ожидалось по простым лабораторным экспериментам.
Построение простой картины сложной системы
Авторы подходят к этой задаче с помощью феноменологической модели — модели, сосредоточенной на общей наблюдаемой динамике, а не на каждой микроскопической детали. В их концепции печень производит тетрамеры ТТР с постоянной скоростью, которые попадают в кровоток. В циркуляции тетрамеры могут диссоциировать на мономеры и снова ассоциироваться, при этом как тетрамеры, так и мономеры могут выводиться из крови путем захвата тканями и разрушения. Записав пару уравнений баланса масс для тетрамеров и мономеров, команда изучает разные сценарии: когда мономеры в основном вновь присоединяются к тетрамерам, когда они быстро удаляются, и промежуточный случай, где важны оба процесса. Для оценки ключевых величин — скорости клиренса тетрамеров, скорости их распада и силы замедления этого распада препаратами — они опираются на исторические исследования с трассерами у людей и современные лабораторные данные.
Почему одной стабилизации тетрамера недостаточно
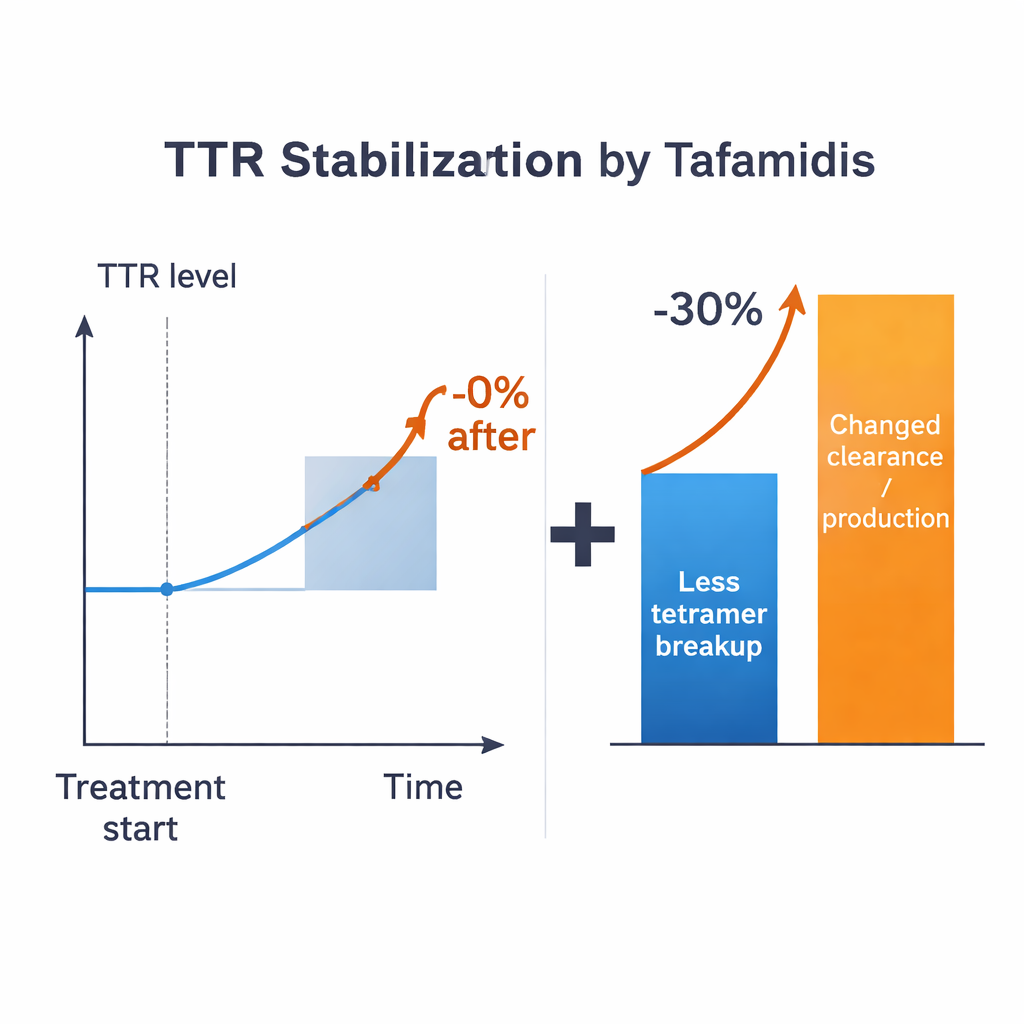
Вооружившись этими оценками, исследователи задают прямой вопрос: если препарат идеально предотвращал бы распад тетрамеров, насколько возрастет уровень ТТР в крови? Во всех правдоподобных режимах ответ скромен — порядка 15% в лучшем случае для типичных параметров и часто меньше, в зависимости от того, как обрабатываются мономеры. Это далеко от наблюдаемого более чем 30% увеличения у пациентов на терапии. Несоответствие сохраняется даже при щедрой учете неопределенностей в известных параметрах. Модель, следовательно, указывает, что простое замедление распада тетрамеров само по себе не может объяснить весь клинический эффект. Должны также изменяться другие процессы, контролирующие скорость синтеза, захвата клетками или разрушения ТТР, когда присутствуют стабилизаторы.
Подсказки от уровней препарата и хитрых экспериментов
Чтобы связать дозу препарата с поведением ТТР, авторы объединяют простую фармакокинетическую модель тафамидиса (как препарат распределяется по организму во времени) с специализированными тестами «обмена субъединиц». В этих экспериментах меченые и немеченые тетрамеры ТТР смешивают в плазме человека, и постепенный обмен субъединицами показывает, как часто тетрамеры распадаются. Измерение этого процесса при разных концентрациях препарата дает прямую, основанную на данных связь между уровнем тафамидиса и эффективной стабильностью тетрамера, без необходимости знать, сколько препарата связано с альбумином или гормоном щитовидной железы. Эта феноменологическая связь вводится в модель и аккуратно обходит многие биохимические неизвестные. Тем не менее даже с этим преимуществом расчеты ограничивают ожидаемый рост ТТР примерно половиной от клинически наблюдаемого увеличения, что усиливает идею о том, что в историю вовлечены изменения клиренса, внутренизации, деградации или даже синтеза.
Что это означает для дальнейших исследований
Для неспециалистов ключевое сообщение таково: эти стабилизаторы, вероятно, делают больше, чем просто «склеивают» тетрамеры ТТР. Они, вероятно, также влияют на то, как организм производит, удаляет или перерабатывает белок. Авторы утверждают, что простые, прозрачные модели, подобные их, ценны, поскольку выявляют пробелы в нашем понимании и указывают на конкретные эксперименты — например, прямое измерение скорости удаления мономеров, скорости захвата разными формами ТТР клетками или выяснение, по-разному ли обрабатывается препарат-связанный ТТР по сравнению с несвязанным белком. Лучшие ответы на эти вопросы не только уточнят лечение амилоидоза транстиретина, но и могут выявить общие правила для других заболеваний, в которых нормальные белки превращаются в вредные агрегаты.
Цитирование: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Ключевые слова: амилоидоз транстиретина, стабилизация белка, тафамидис, моделирование фармакокинетики, амилоидные заболевания