Clear Sky Science · ru
Целенаправленная стабилизация фактора индукции гипоксии 1‑альфа (HIF1A) во время инвитро‑созревания бовинных кумулюс‑ооцитных комплексов повышает уровень бластоцист
Почему важно регулировать чувствительность яйцеклетки к кислороду
Современное разведение крупного рогатого скота в значительной степени опирается на эмбрионы, полученные в лаборатории, но успех далёк от гарантированного: лишь около трети ооцитов достигают ключевой стадии бластоцисты, когда их уже можно переносить в матку. В этом исследовании поставлен на вид казалось бы простой, но важный вопрос для животноводства и вспомогательных репродуктивных технологий: если мы точнее воспроизведём низко‑кислородные условия, в которых ооциты естественно развиваются в яичнике — аккуратно усилив действие ключевого белка, отвечающего за сенсинг кислорода — сможем ли мы помочь большему числу эмбрионов успешно развиться?
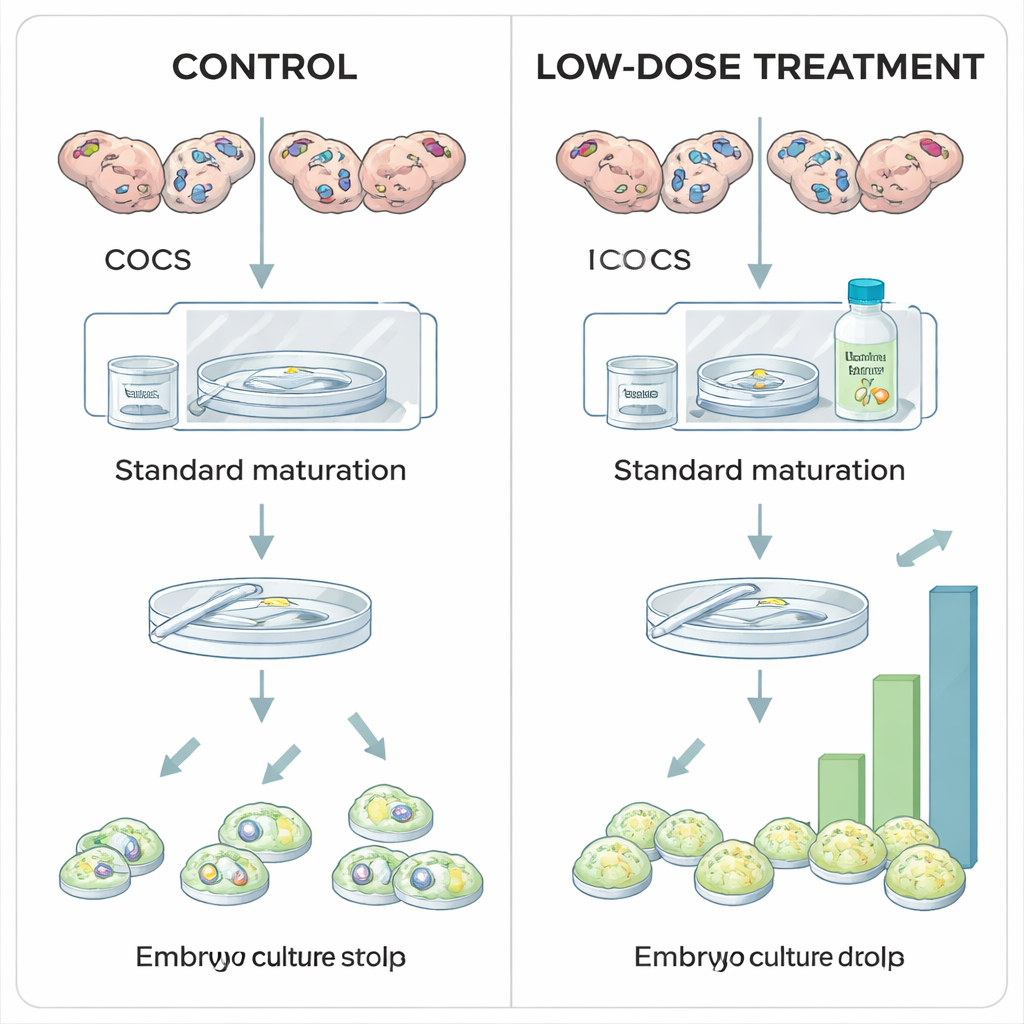
Жизнь начинается в среде с пониженным содержанием кислорода
Внутри яичника каждый развивающийся ооцит окружён поддерживающим скоплением клеток, называемым кумулюсом; вместе они образуют кумулюс–ооцитный комплекс. Хотя по мере роста фолликулов кровоснабжение яичника усиливается, сосуды не проникают в непосредственную близость ооцита. Кислород должен диффундировать, создавая вокруг созревающей яйцеклетки умеренно низко‑кислородную, или гипоксическую, нишу. В этой среде внутриклеточный сенсор HIF1A помогает клеткам адаптироваться, корректируя метаболизм и выработку гормонов. Предыдущие работы показали, что блокирование HIF1A вредно для созревания ооцитов и резко снижает образование эмбрионов, что подчёркивает роль этого белка как центрального координатора компетентности ооцита — способности быть оплодотворённым и развиться в здоровый эмбрион.
Использование препарата для тонкой настройки кислородного сенсора ооцита
Исследователи изучали, может ли умеренная стабилизация HIF1A во время лабораторного созревания бовинных ооцитов повысить выход эмбрионов. В стандартных in vitro протоколах кумулюс–ооцитные комплексы созревают при атмосферном уровне кислорода, в основном по практическим, а не биологическим причинам. В этой работе ооциты, собранные из яичников с убойных пунктов, разделили на группы и в течение 24‑часового периода созревания подвергали разным дозам Роксадустата, препарата, уже применяемого в медицине человека для лечения анемии. Роксадустат действует, блокируя семейство ферментов, называемых пролилгидроксилазами (PHD), которые обычно помечают HIF1A для разрушения при изобилии кислорода. Ингибируя PHD, Роксадустат позволяет белку HIF1A накапливаться даже при более высоком уровне кислорода, частично воссоздавая гипоксический сигнал, который ооцит ощущал бы in vivo.
Больше бластоцист при оптимальной дозе, вред при высоких уровнях
При оценке состояния ооцитов и эмбрионов после лечения выявилась чёткая закономерность. Низкая доза Роксадустата (25 микромолей) не изменила долю ооцитов, завершивших созревание, или долю оплодотворённых ооцитов, начавших деление, но значительно увеличила долю тех, кто достиг стадии бластоцисты. Иными словами, ранние этапы оставались неизменными, однако больше эмбрионов успешно завершали сложный путь до бластоцисты — что указывает на то, что умеренная стабилизация HIF1A улучшает внутреннее качество ооцита. Напротив, самая высокая доза (100 микромолей) снизила процент ооцитов, вообще завершивших созревание, а при применении того же ингибитора позднее, в восьмидневной культуре эмбрионов, высокие дозы резко уменьшали образование бластоцист, не влияя на раннее дробление. Эти данные показывают, что «ровно столько» активности HIF1A во время созревания полезно, тогда как чрезмерная или слишком продолжительная активация вредна.
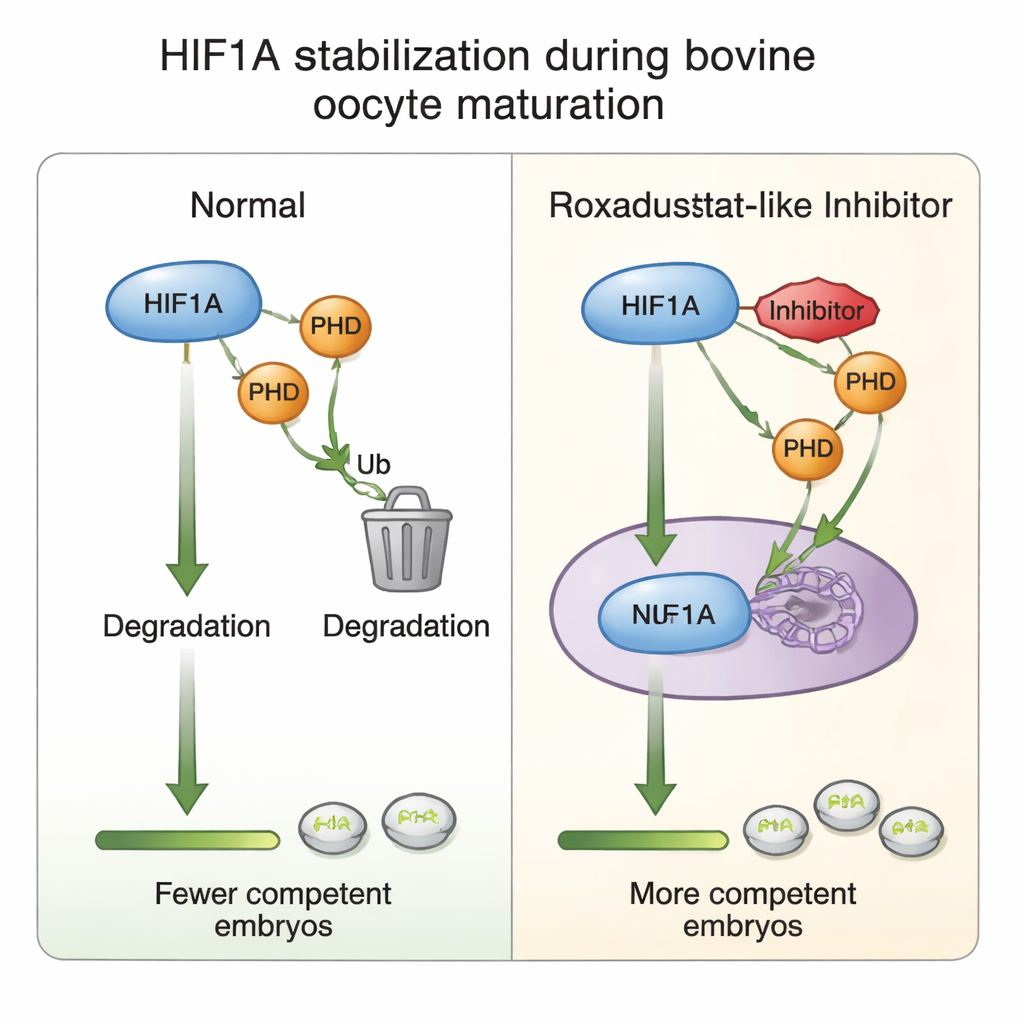
Что происходит в поддерживающих клетках ооцита
Чтобы понять, как действует химическая настройка, авторы исследовали кумулюс‑клетки, окружающие каждый ооцит. Они обнаружили, что само созревание в целом повышает активность генов HIF1A, но добавление Роксадустата парадоксально снижало уровень мРНК HIF1A при сохранении уровня белка HIF1A — намёк на то, что клетки могут уменьшать транскрипцию, когда белок уже стабилизирован, своего рода встроенный тормоз от чрезмерной активации. Уровни PHD2, самой чувствительной к кислороду из ферментов PHD, повышались в ответ на препарат, что усиливает её роль в петле кислородного сенсинга. При более высоких дозах препарата снижались маркёры пролиферации клеток и компоненты адгезивного матрикса, который помогает кумулюс‑клеткам развернуться вокруг ооцита, что согласуется с наблюдаемым падением созревания и образования эмбрионов. Всё это поддерживает идею, что тщательно сбалансированная активность HIF1A тонко настраивает диалог между ооцитом и кумулюс‑клетками, лежащий в основе последующего успешного развития.
Последствия для животноводства и не только
Эта работа демонстрирует, что легкая стабилизация кислородного сенсора ооцита в течение короткого окна in vitro‑созревания может существенно повысить и стабилизировать выход бластоцист у крупного рогатого скота, не меняя оплодотворяемости или раннего дробления. С практической точки зрения это может означать более надёжное производство эмбрионов для племенных программ с использованием целевого препарата вместо грубых изменений уровня кислорода или более токсичных химикатов. Исследование также подчёркивает более общий вывод, важный для лечения бесплодия у человека: имитация тонкой, низко‑кислородной среды яичника — это не просто регулировка уровня кислорода, а уважение к хрупкому балансу сигнальных молекул, таких как HIF1A. Точная настройка этого баланса, а не доведение его до крайностей, может быть ключевым путём к получению более здоровых эмбрионов.
Цитирование: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Ключевые слова: производство эмбрионов in vitro, созревание ооцитов, гипоксическая сигнализация, стабилизация HIF1A, разведение крупного рогатого скота