Clear Sky Science · ru
CMAF-Net: кросс-модальное объединение внимания с информационно-теоретической регуляризацией для несбалансированной гистопатологии рака груди
Почему это исследование важно для помощи при раке груди
Патологи ставят диагноз рака груди, изучая тонкие срезы ткани под микроскопом, но отделить редкие злокачественные участки от моря здоровых клеток — трудоёмкая и несовершенная задача. В этом исследовании предложен CMAF-Net, новый тип компьютерной системы, призванной помогать обнаруживать больше случаев рака на таких изображениях при сохранении невысокого числа ложных тревог, даже когда злокачественные образцы значительно уступают в количестве здоровым. Его достижения могут повысить надёжность автоматизированного скрининга, поддержать перегруженных клиницистов и дать шаблон для выявления многих других редких заболеваний.
Искать иголку в стоге тканевых изображений
В реальных клинических данных большинство образцов ткани груди безвредны, и лишь меньшая часть содержит инвазивную протоковую карциному — наиболее распространённую форму рака груди. Такая несбалансированность заставляет многие системы искусственного интеллекта «учиться» тому, что предсказывать здоровую ткань почти всегда безопасно, из-за чего пропускаются опасные опухоли. При этом признаки злокачественности проявляются на очень разных уровнях увеличения: от искажённых ядер отдельных клеток до нарушенной организации в целом на участках ткани. Традиционные сети анализа изображений хорошо справляются либо с мелкими деталями, либо с крупными паттернами, но редко соединяют оба подхода так, чтобы выделять редкие, потенциально смертельные случаи.
Сочетая крупный план с общей картиной
Чтобы решить эти две задачи, авторы разработали CMAF-Net с двумя дополняющими друг друга «глазами» для каждого изображения. Одна ветвь действует как классический движок распознавания паттернов и специализируется на тонких текстурах, таких как форма и расположение клеток. Вторая ветвь напоминает считыватель глобальной карты и фиксирует более широкую организацию ткани, используя современную архитектуру трансформера. Вместо того чтобы просто складывать эти два представления, система пропускает их через специальный блок слияния, который позволяет ветвям обмениваться информацией по множественным каналам внимания. Этот блок избирательно сохраняет признаки, добавляющие новую информацию, и подавляет дублирующие или отвлекающие сигналы, так что итоговое комбинированное представление остаётся одновременно информативным и компактным. 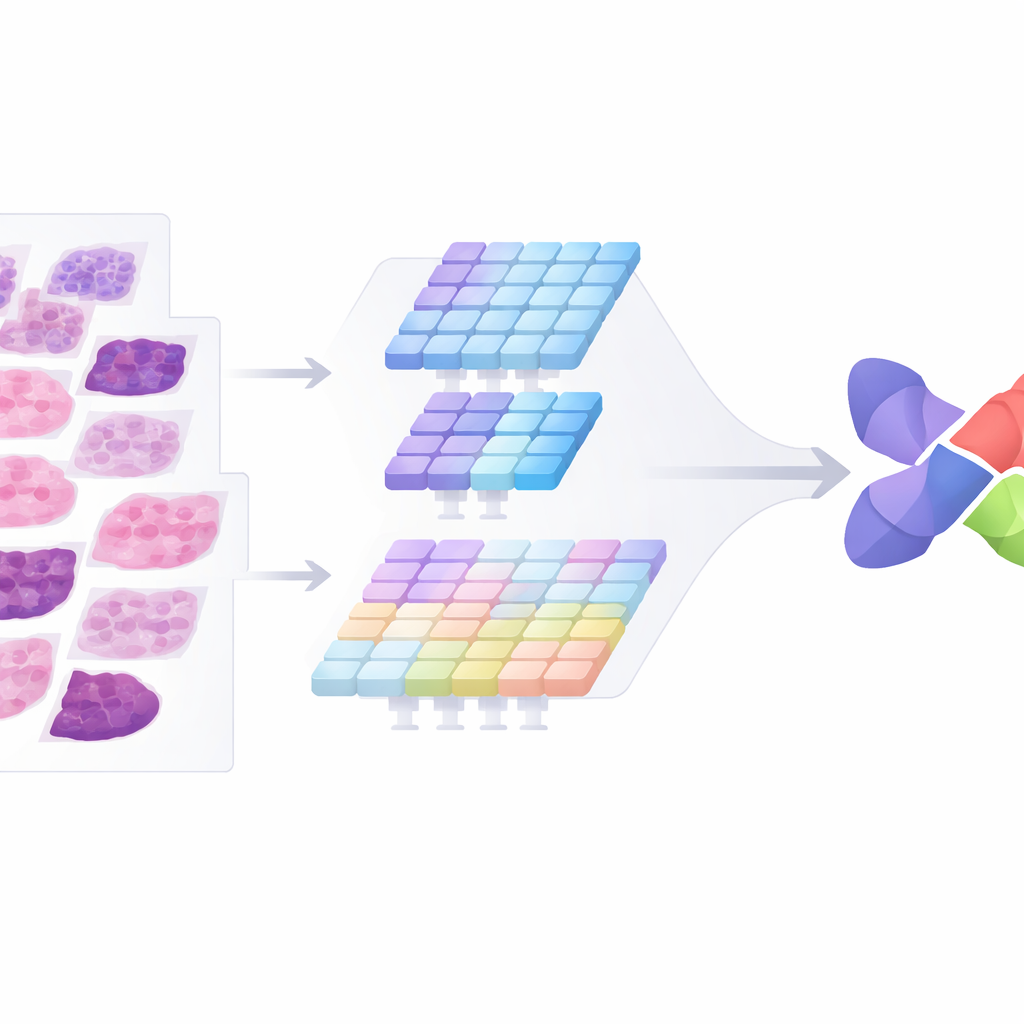
Обучение системе уделять внимание редким случаям рака
Даже продуманная архитектура может по-прежнему отдавать предпочтение мажоритарному классу, поэтому исследователи переработали способ, которым система учится на ошибках. Опираясь на идеи информационной теории и маргинального обучения, они разработали правило обучения, которое прямо стимулирует модель формировать более широкие «зоны безопасности» вокруг миноритарных случаев рака. На практике CMAF-Net сильнее наказывается за пропуск злокачественного участка, чем за ошибочную классификацию доброкачественного, и этот штраф корректируется со временем по мере «созревания» пространства признаков. Сам механизм внимания также настраивается с помощью своего рода контроля «температуры»: острое внимание сохраняет больше информации при необходимости, тогда как более мягкое внимание отфильтровывает шум, давая модели принципиальный способ сжимать данные, не теряя сигналов, отличающих рак от не-рака. 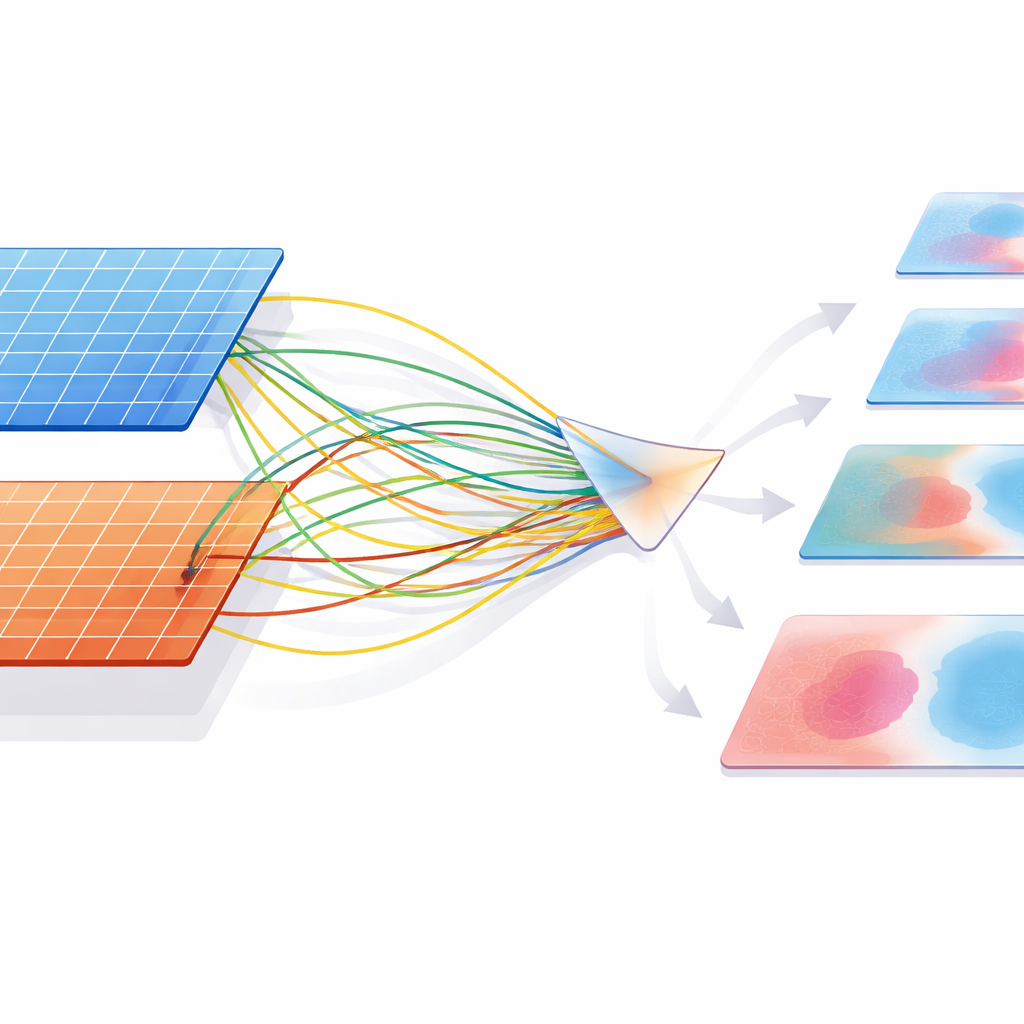
Тестирование метода
Команда оценивала CMAF-Net на большой, естественно несбалансированной выборке патчей ткани груди, где примерно три четверти были доброкачественными, а остальные — злокачественными. По сравнению с рядом сильных базовых систем — включая глубокие свёрточные сети, визуальные трансформеры и предыдущие модели слияния, адаптированные под несбалансированность — новый метод выделялся. Он правильно идентифицировал примерно 95% злокачественных образцов при сохранении сопоставимо высокой специфичности, и делал это с меньшим числом параметров, чем многие конкурирующие модели слияния. Когда авторы ещё сильнее исказили баланс данных — до одного злокачественного патча на девяносто девять доброкачественных — производительность CMAF-Net снижалась постепенно, но оставалась клинически полезной. Другие методы, напротив, теряли большую часть способности распознавать рак в этих экстремальных условиях.
Обобщение между микроскопами и типами опухолей
Чтобы проверить, не запомнила ли модель лишь одну выборку, а действительно ли она усвоила более универсальные закономерности болезни, авторы испытали её на отдельной коллекции изображений опухолей груди, снятых у разных пациентов и на четырёх уровнях увеличения. Без дополнительного дообучения модель сохранила высокую чувствительность на всех уровнях увеличения и превзошла предыдущие подходы как в простой задаче доброкачественное/злокачественное, так и в более сложной восьмиклассовой задаче, охватывающей несколько подтипов опухолей. Примечательно, что наибольшие улучшения CMAF-Net показал на редких категориях опухолей, что указывает на то, что его акцент на информационно-эффективном слиянии и обучении, учитывающем класс, помогает отличать тонкие, нетипичные паттерны, а не только наиболее распространённые случаи.
Что это означает в будущем
Для неспециалистов ключевое сообщение таково: CMAF-Net предлагает более умный способ, которым компьютеры читают патологические слайды — он одновременно смотрит вблизи и в целом, учится уделять дополнительное внимание редким, но опасным признакам рака и продолжает работать даже при дефиците злокачественных примеров. За пределами рака груди те же принципы проектирования могут лечь в основу инструментов для выявления редких заболеваний в самых разных медицинских изображениях, предоставляя врачам более надёжное второе мнение и потенциально обеспечивая более ранние и точные диагнозы пациентам, которые в этом больше всего нуждаются.
Цитирование: Ativi, W.X., Chen, W., Kwao, L. et al. CMAF-Net: cross-modal attention fusion with information-theoretic regularization for imbalanced breast cancer histopathology. Sci Rep 16, 9607 (2026). https://doi.org/10.1038/s41598-025-32794-1
Ключевые слова: рак груди, гистопатология ИИ, несбалансированность классов, глубокое обучение, анализ медицинских изображений