Clear Sky Science · ru
Перепрофилирование природных соединений для спиноцеребеллярной атаксии типа 3 с использованием интегрированной сетевой фармакологии и in silico подходов
Почему это исследование важно для пациентов и семей
Спиноцеребеллярная атаксия типа 3 (SCA3) — редкое наследственное заболевание мозга, которое постепенно лишает людей равновесия, координации и самостоятельности. В настоящий момент нет ни лечения, ни одобренного препарата, способного остановить прогрессирование болезни. В этом исследовании изучают, можно ли разумно «перепрофилировать» соединения, уже встречающиеся в природе — многие из них происходят из традиционной медицины — с помощью мощных компьютерных инструментов, что может обеспечить более быстрый и потенциально безопасный путь к новым терапиям.
Поиск полезных молекул в природе
Исследователи сосредоточились на природных веществах: химических соединениях, обнаруживаемых в растениях и других живых организмах, которые долгие годы служили источником для современных лекарств. Они собрали 15 перспективных природных соединений, ранее показавших смягчение признаков SCA3 в клеточных или животных моделях. С помощью специализированных баз данных предсказали, с какими белками человека каждое соединение может взаимодействовать, и отдельно собрали тысячи генов, связанных с SCA3. Сравнив эти два набора, они выделили 239 общих мишеней — белков, вовлеченных в болезнь и потенциально влияющихся этими природными молекулами. 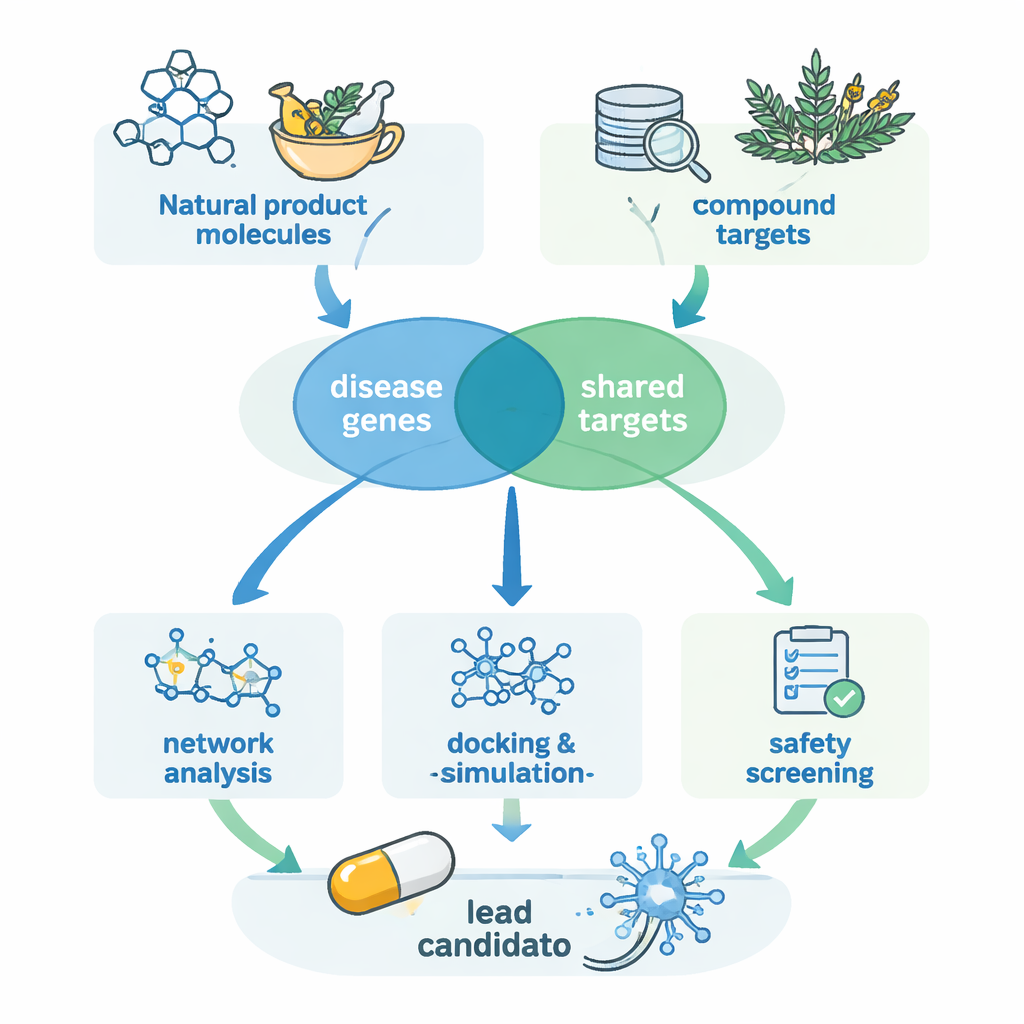
Картирование уязвимых мест болезни
Далее команда построила крупные «карты взаимодействий», показывающие, как эти 239 белков взаимодействуют друг с другом в клетках. На этих картах некоторые белки выступают в роли загруженных узлов транспортной сети, связывая множество путей одновременно. Два таких узла, AKT1 и TP53, оказались особенно центральными. Исследователи затем проанализировали, какие клеточные пути — наборы связанных биохимических реакций — затронуты наиболее сильно. Один путь, известный как MAPK-сигнальный путь, выделился как особенно важный и уже признан влияющим на выживание нейронов, реакции на стресс и дегенерацию. Многие природные соединения, по-видимому, воздействуют на этот путь, что указывает на общий механизм, посредством которого они могут защищать нейроны при SCA3.
Виртуальное изучение кроцина
Из всех протестированных молекул кроцин — ярко-оранжевый пигмент шафрана — показал наибольшее предсказанное сродство к обоим белкам AKT1 и TP53. Для более детального понимания команда применила компьютерное докинг-моделирование, в котором виртуальная копия каждого соединения помещается в 3D-модель белка, как ключ в замок. Кроцин «подошёл» к белкам AKT1 и TP53 лучше, чем референсный экспериментальный препарат трэрилужол (troriluzole), образуя более стабильные контакты и более сильные взаимодействия. Затем учёные выполнили длительные молекулярно-динамические симуляции, имитирующие движение атомов во времени в водной, приближённой к организму, среде. Эти симуляции показали, что комплексы белок—кроцин оставались стабильными, формировали множество водородных связей и переходили в низкоэнергетические устойчивые конфигурации — признаки сильного и надёжного взаимодействия.
Как это может помочь защитить нейроны
AKT1 и TP53 участвуют в решении, восстановится ли напряжённый нейрон или погибнет. При SCA3 дефектные формы белка атаксин-3 нарушают сигнальные сети, в которых участвуют оба этих ключевых регулятора, сдвигая баланс в сторону повреждения и гибели клеток. Компьютерные модели предполагают, что кроцин может связываться с AKT1 в областях, важных для его активности, и с TP53 в области, связывающей ДНК, что тонко меняет поведение этих белков. Ранние лабораторные исследования в других моделях заболеваний мозга показывают, что кроцин может снижать оксидативный стресс, уменьшать воспаление, стабилизировать митохондрии (энергетические станции клетки) и модулировать пути клеточной смерти. В совокупности новые симуляции поддерживают идею о том, что кроцин мог бы помочь восстановить более здоровый баланс выживания и гибели нейронов при SCA3.
От компьютерных предсказаний к реальным терапиям
Хотя предсказанный профиль безопасности кроцина выглядит благоприятным, и его поведение в симуляциях обнадёживает, эта работа пока остаётся на уровне компьютерных моделей. Исследование не тестирует кроцин непосредственно на людях с SCA3. Вместо этого оно предоставляет детальную дорожную карту, указывающую на кроцин как на сильного кандидата для дальнейших лабораторных и животных испытаний, а в перспективе — для тщательно спланированных клинических испытаний. 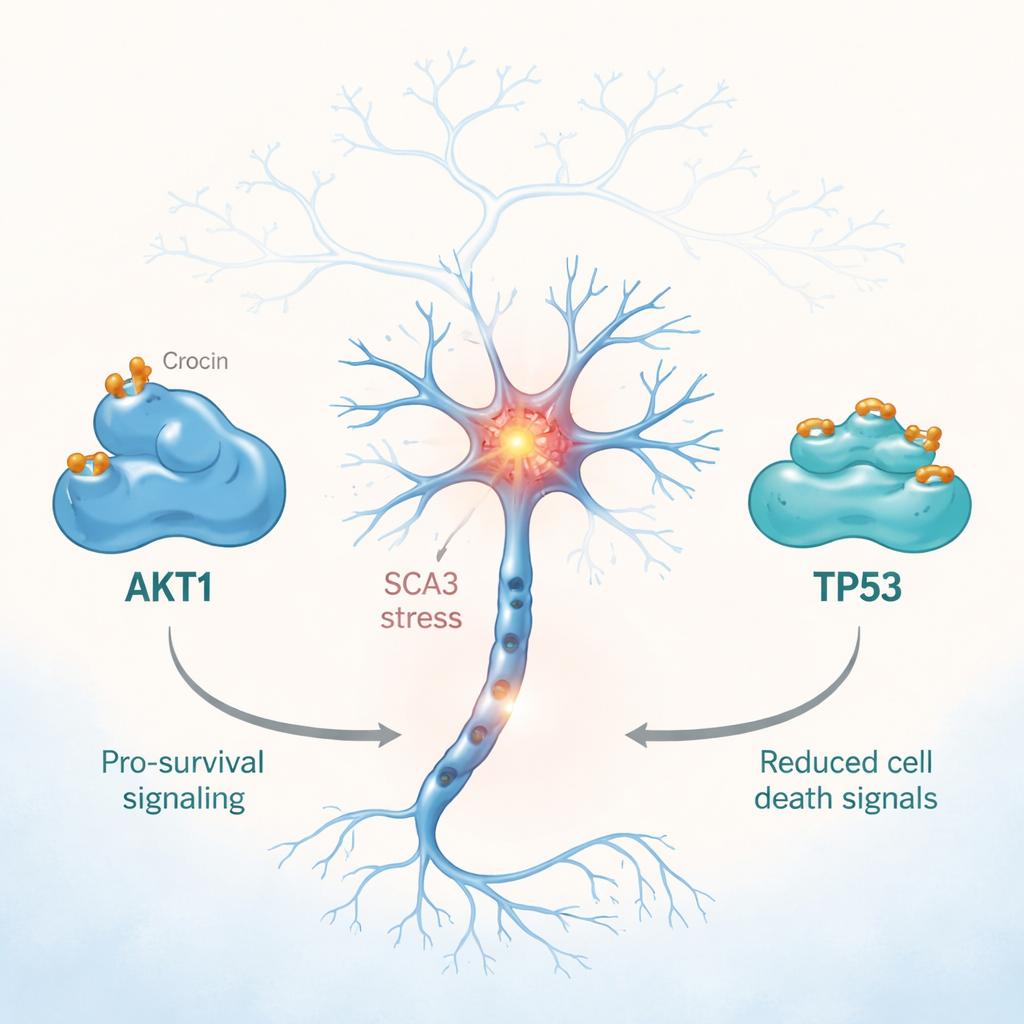
Цитирование: Roney, M., Mohd Hisam, N.S., Uddin, M. et al. Repurposing of natural products for spinocerebellar ataxia type 3 using integrated network pharmacology and in silico approaches. Sci Rep 16, 7332 (2026). https://doi.org/10.1038/s41598-025-30652-8
Ключевые слова: спиноцеребеллярная атаксия типа 3, природные вещества, перепрофилирование лекарств, кроцин, нейродегенерация