Clear Sky Science · ru
Визуализация динамики внеклеточного аденозина в живом сердце и её фармакологическая модуляция в моделях сердечной недостаточности на цефалолеписах
Почему эта история о рыбьем сердце важна
Сердечная недостаточность остаётся одной из ведущих причин смерти в мире, и многие пациенты продолжают ухудшаться, несмотря на современные лекарства. Учёным известно, что стрессированные кардиомиоциты выделяют в окружение химические «сигналы тревоги», но наблюдать эти сигналы в действии внутри бьющегося сердца было трудно. В этом исследовании используют прозрачных зебрафишей, чьи крошечные сердца повторяют ключевые черты человеческого сердца, чтобы следить за этими сигналами в реальном времени и опробовать новый способ их подавления.
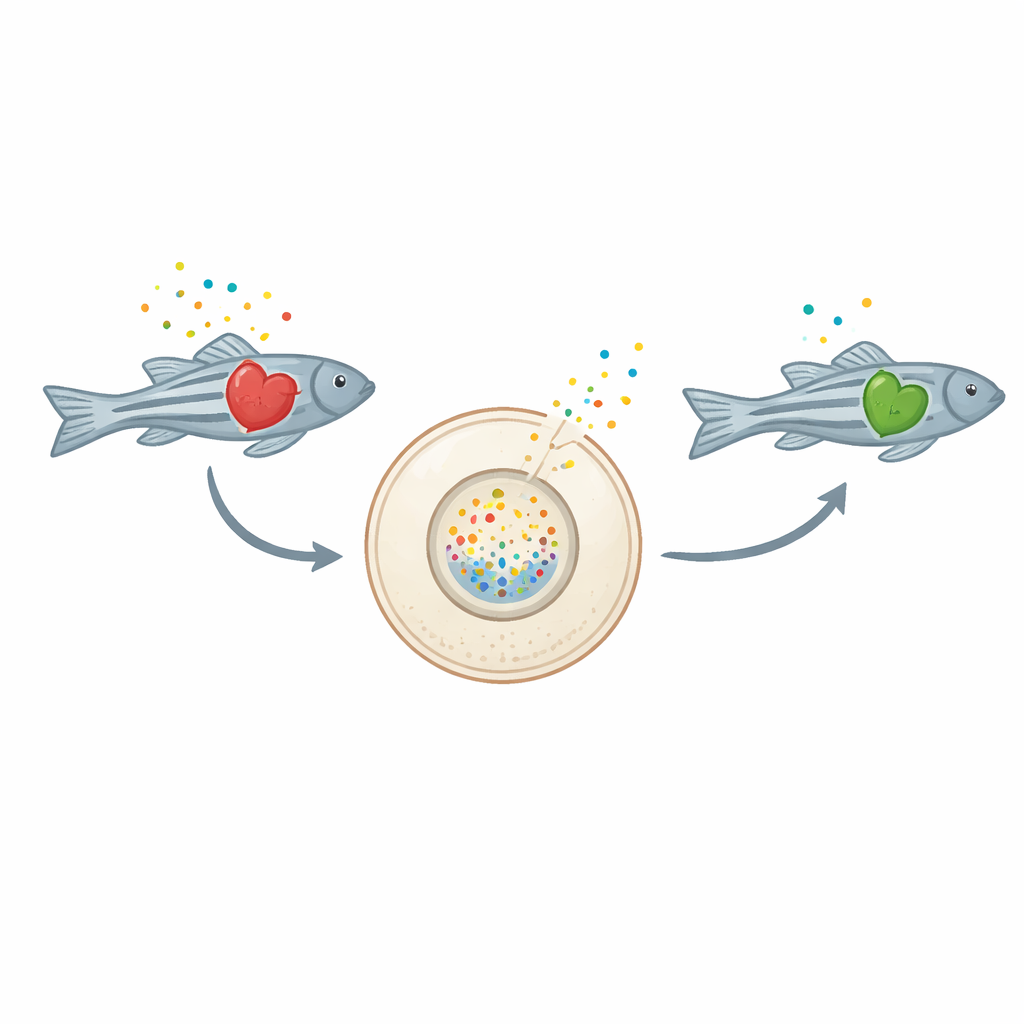
Сигналы от испытывающего трудности сердца
Когда клетки сердца повреждаются, они выделяют молекулы, несущие энергию, такие как АТФ, и его продукт распада — аденозин — в пространство за пределами клетки. Вне клетки эти молекулы перестают служить топливом и вместо этого действуют как срочные сообщения, которые могут разжигать воспаление. При хронической сердечной недостаточности этот воспалительный ответ может становиться чрезмерным и дополнительно повреждать сердце. До сих пор у исследователей не было прямых данных in vivo о том, как эти молекулы ведут себя с течением времени в падающем сердце.
Превращение зебрафишей в живые химические камеры
Команда создала зебрафишей, у которых кардиомиоциты экспрессируют на поверхности специальный флуоресцентный сенсорный белок под названием GRABAdo. Когда аденозин накапливается вне клеток, этот сенсор ярче светится зелёным, фактически превращая каждое крошечное сердце в собственную живую химическую камеру. Исследователи затем вызвали сердечную недостаточность у зебрафишей с помощью терфенадина — препарата, известного тем, что нарушает ритм сердца и ослабляет его сократительную функцию. По мере того как у рыб проявлялись явные признаки сердечной недостаточности — замедление сердцебиения, увеличение и ослабление желудочков, отёк вокруг сердца и снижение способности к плаванию — показатели сенсора в сердце усиливались, показывая заметный рост внеклеточного аденозина. Химические измерения в целом по личинкам подтвердили, что общие уровни аденозина были повышены в поражённых сердцах.
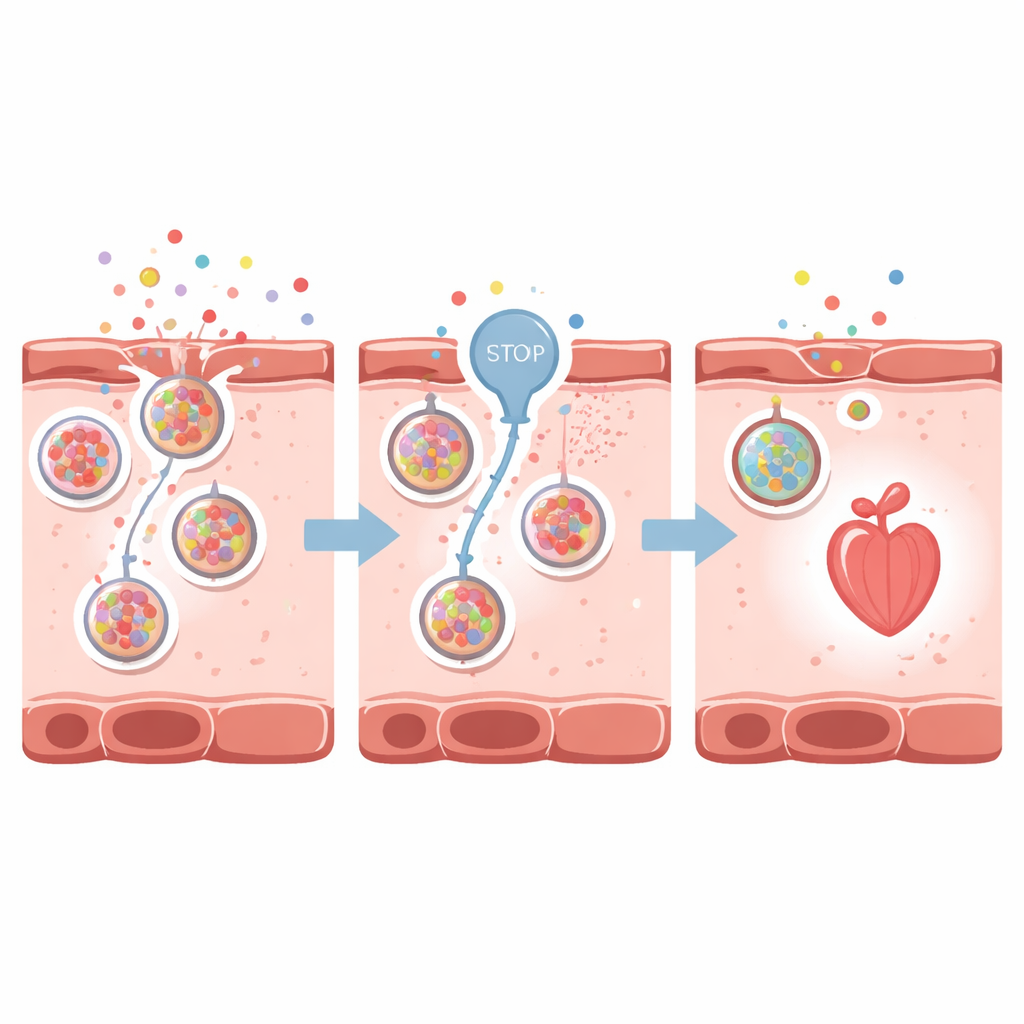
Перекрытие клапана выхода
Затем учёные спросили, может ли ослабление этих сигналов защиты помочь сердцу. Они сфокусировались на VNUT — транспортере, который загружает АТФ в маленькие внутриклеточные пакеты (везикулы) для последующего выделения наружу. Используя клодронат — препарат, блокирующий VNUT, — они уменьшили выделение АТФ и, косвенно, накопление аденозина вокруг кардиомиоцитов. У зебрафишей с индуцированной лекарством сердечной недостаточностью ингибирование VNUT сохраняло форму сердца, сокращало расширение полостей, улучшало частоту и силу сокращений и поддерживало лучший кровоток. Светящийся сенсор аденозина тускнел, показывая, что вне клеток присутствовало меньше сигнала тревоги. Похожие защитные эффекты наблюдались и у взрослых рыб с острой, быстро развивающейся формой сердечной недостаточности.
Несколько защитных рычагов работают вместе
Сердечная недостаточность затрагивает не один путь, поэтому исследователи проверили, как блокада VNUT взаимодействует с другими известными участниками процесса. Препараты, блокирующие определённые аденозиновые рецепторы и рецепторы АТФ, а также соединение, ограничивающее пассивный утек АТФ через мембранные каналы, по отдельности помогали сердцам зебрафишей. В сочетании с ингибированием VNUT многие из этих вмешательств давали аддитивные преимущества, что указывает на то, что ослабление пуриновой сигнализации в нескольких точках может быть особенно эффективно. Блокада VNUT также способствовала восстановлению кальциевого гомеостаза в кардиомиоцитах, что важно для нормального сокращения, и снижала как гибель клеток, так и активность генов, связанных с воспалением. В совокупности эти результаты представляют VNUT как центральный переключатель, связывающий выделение АТФ, воспаление, нарушение кальциевого обмена и прогрессирующее повреждение сердца.
От аквариумов к перспективным терапиям
Для неспециалистов главный вывод в том, что исследование непосредственно визуализирует повышение химического сигнала стресса в падающих сердцах и показывает, что блокада его выделения может защищать сердечную функцию у живого животного. Хотя сердца зебрафишей проще человеческих, у них достаточно сходной биологии, чтобы служить мощной тестовой платформой для новых идей. Выявив VNUT как перспективную мишень на пересечении воспаления и электрической нестабильности, эта работа предполагает, что будущие терапии сердечной недостаточности могут делать не только поддержку кровотока — они могут активно успокаивать вредные клеточные «разговоры», подталкивающие сердце к декомпенсации.
Цитирование: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
Ключевые слова: сердечная недостаточность, аденозиновая сигнальная система, модель на данио (зебра-рыба), воспаление, защита сердца