Clear Sky Science · ru
Крупномасштабный набор гистологических изображений с метаданными для изучения микроокружения колоректального рака
Почему важно картировать скрытое «окружение» рака
Когда врачи рассматривают опухоль толстой кишки под микроскопом, они видят не только раковые клетки; перед ними — оживлённый «район» из жировой ткани, иммунных клеток, соединительной ткани и прочего. Такое сочетание типов клеток, называемое микроокружением опухоли, существенно влияет на ответ пациента на лечение и на прогноз выживания. Тем не менее у компьютеров, которые могли бы помочь врачам интерпретировать эти сложные сцены, была простая преграда: им не хватало хорошо размеченных изображений для обучения. В этом исследовании представлен один из крупнейших и наиболее тщательно аннотированных наборов изображений ткани при колоректальном раке, когда-либо собранных, специально предназначенный для обучения и тестирования современных систем искусственного интеллекта.
Создание масштабной библиотеки изображений опухолей толстой кишки
Исследователи создали ресурс под названием HMU-CRC-Hist550K, собранный из образцов тканей 500 пациентов, лечившихся от колоректального рака в крупном онкологическом центре в Китае. Опухоли каждого пациента фиксировали, окрашивали по стандартной методике, используемой в патологоанатомических лабораториях, и сканировали в виде высокоразрешённого цифрового слайда. Из этих слайдов автоматически вырезали небольшие квадратные фрагменты изображений, примерно такого размера, какой патологоанатом видит одновременно в микроскопе. Всего получилось около 550 000 таких плиток, что даёт моделям ИИ огромный и разнообразный набор примеров для изучения внешнего вида разных тканей.
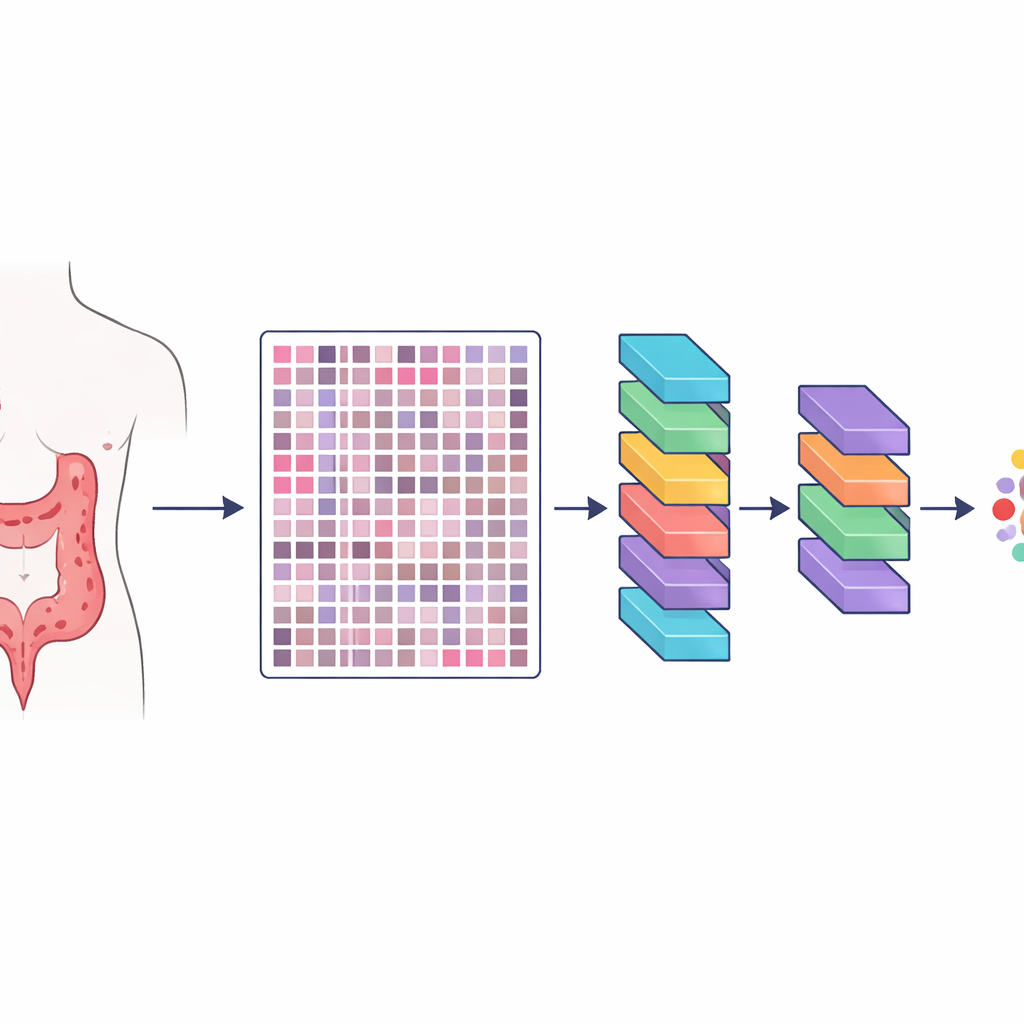
Тщательная ручная разметка ландшафта опухоли
Создание большой библиотеки изображений само по себе недостаточно; изображения нужно ещё и точно размечать. Три опытных патологоанатома совместно провели трёхэтапный процесс, чтобы выделить восемь ключевых компонентов микроокружения опухоли: жировую ткань, клеточный детрит, иммунные клетки — лимфоциты, слизь, гладкую мускулатуру, нормальную слизистую оболочку толстой кишки, окружающую опухоль соединительную ткань и собственно раковые клетки. Два патологоанатома сначала независимо наносили метки на крупных слайдах, затем проверяли работы друг друга. Старший специалист выполнил финальную экспертизу, разрешил разногласия и исключил неясные участки. Такое взаимное контрольное сверение значительно снизило личную предвзятость и обеспечило очень согласованную разметку в деталях, так что каждая плитка связана с конкретным типом ткани в пределах «района» опухоли.
Связывание микроскопических видов с историей пациента
Особую силу этому набору придаёт то, что изображения сопоставлены с богатой клинической информацией по каждому пациенту. Для каждого случая команда собрала базовые сведения, такие как возраст и пол, а также стадию опухоли, её локализацию в толстой или прямой кишке, степень атипии клеток, наличие прорастания нервов или лимфоузлов и продолжительность выживания после лечения. Также были учтены результаты обычных лабораторных тестов, отражающих генетическую и белковую характеристику опухоли. Все персональные идентификаторы были удалены, чтобы исключить возможность опознавания пациентов. Сочетая паттерны ткани с этими клиническими данными, исследователи могут изучать, как конкретные конфигурации микроокружения связаны с реальными исходами, например какие пациенты имеют более благоприятный или неблагоприятный прогноз.
Проверка ИИ на новом наборе данных
Чтобы показать практическую ценность набора данных, учёные обучили три различных модели глубокого обучения — современные системы распознавания образов, отлично справляющиеся с задачами по изображению — распознавать восемь типов тканей на плитках. Они использовали строгие правила разделения пациентов на тренировочную и тестовую группы, чтобы модели оценивались на ранее не встречавшихся пациентах. Модели, включая как классические свёрточные сети, так и более современную архитектуру «vision transformer», показали очень высокую точность, с показателями близкими к идеальным на нескольких тестовых наборах. Команда также сравнила результаты с другими современными методами сегментации изображений и обнаружила сопоставимо высокую эффективность. Визуальные инструменты использовали для подсветки областей ткани, на которые опирались модели, подтверждая, что они фокусируются на медицински значимых регионах, а не на случайных артефактах.
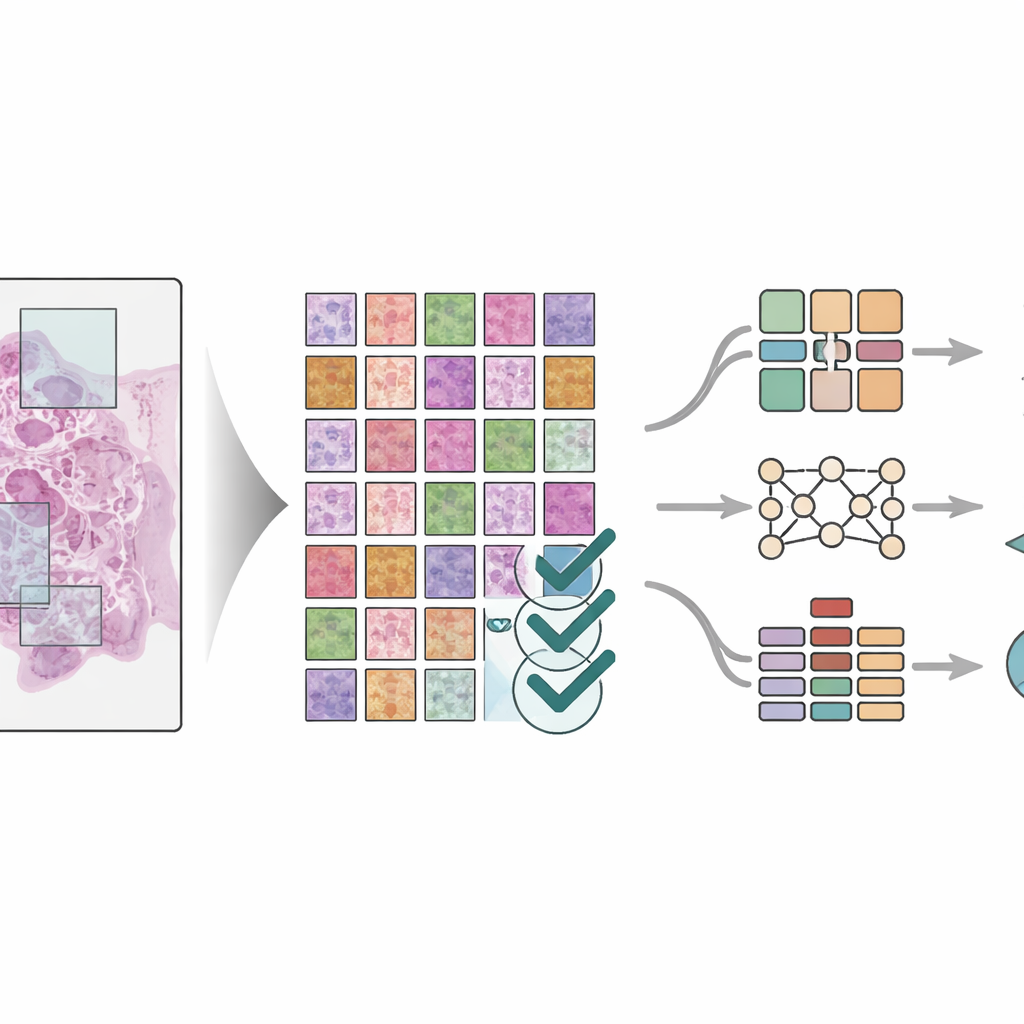
Что это означает для будущей помощи при раке
Для неспециалистов основной вывод заключается в том, что эта работа не представляет собой новое лечение, а создает мощную основу для более умной диагностики и прогнозирования. Публикуя большой, хорошо организованный и открыто доступный набор изображений, связанный с подробными картами пациентов, авторы дают возможность исследователям по всему миру создавать и сравнивать инструменты ИИ на общей, надёжной базе. Такие инструменты в будущем могут помочь патологоанатомам быстрее и стабильнее картировать «окружение» опухоли, прогнозировать, у каких пациентов риск выше, и предлагать более персонализированные стратегии лечения. Хотя текущие данные фиксируют только отдельные моменты времени, а не изменения в течение месяцев или лет, этот ресурс является важным шагом на пути к использованию цифровой патологии и ИИ для лучшего понимания и, в конечном счёте, более эффективного лечения колоректального рака.
Цитирование: Wang, H., Li, H., Xue, J. et al. Large-Scale Histological Image Dataset with Metadata for Colorectal Cancer Microenvironment. Sci Data 13, 431 (2026). https://doi.org/10.1038/s41597-026-06675-9
Ключевые слова: колоректальный рак, микроокружение опухоли, цифровая патология, глубокое обучение, набор медицинских изображений