Clear Sky Science · ru
Курированный ресурс геномов хемолитоавтотрофов и маркерных генов для предсказания путей фиксации CO₂
Микробы, которые помогают уравновесить углеродный бюджет Земли
Скрытые в почвах, океанах и экстремальных средах, некоторые микробы способны строить собственную биомассу, используя диоксид углерода (CO₂) в качестве основного источника углерода. Эти микроскопические «химики» имеют решающее значение для поддержания баланса углеродного цикла Земли и могут послужить вдохновением для новых методов улавливания промышленного CO₂. Однако до сих пор у учёных не было простого и надёжного способа по последовательности ДНК микроорганизма определить, какую стратегию фиксации CO₂ он использует. В этом исследовании представлен курированный каталог генов и новый вычислительный инструмент AutoFixMark, созданный для заполнения этого пробела.
Множество путей превращения воздуха в биомассу
Не все организмы фиксируют CO₂ одинаково. У микроорганизмов эволюционировало как минимум семь природных путей, превращающих CO₂ в органическое вещество. Некоторые, например цикл Калвина–Бенсона–Бассхэма, распространённый у растений и многих бактерий, хорошо знакомы; другие, такие как восстановительный путь глицина, обнаруженный лишь в 2020 году, до сих пор плохо изучены. Эти пути разбросаны по разным ветвям древа жизни и нередко используют схожие ферменты, что затрудняет их различение только по последовательности генома. Существующее программное обеспечение может предсказывать общие метаболические возможности, но оно не было оптимизировано и тщательно протестировано на точное определение конкретных путей фиксации CO₂.
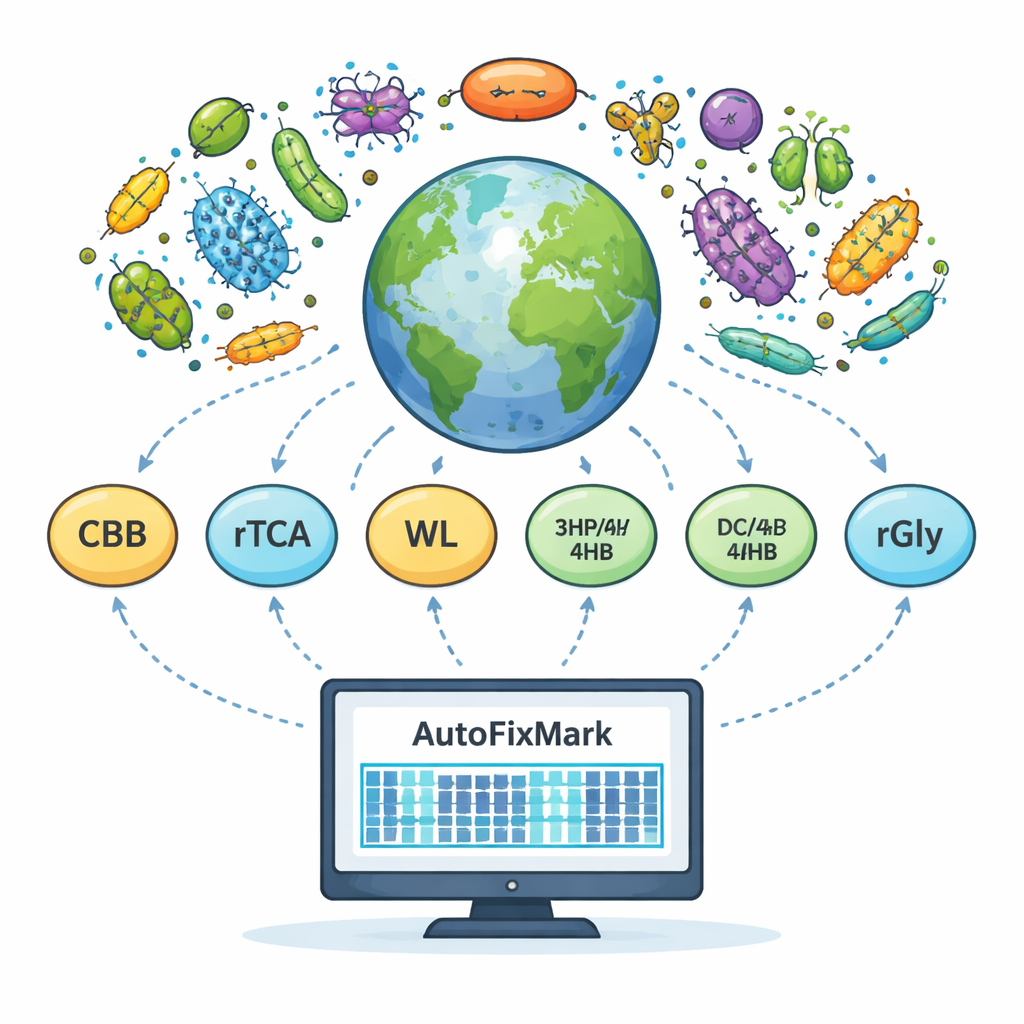
Создание чистой справочной карты микробов, фиксирующих CO₂
Исследователи начали с составления двух тщательно проверенных коллекций геномов. Сначала они отобрали 15 хорошо изученных микроорганизмов, у которых пути фиксации CO₂ проработаны подробно. Эти референсные организмы, представляющие несколько бактериальных и архейных групп, послужили чертежами для определения ключевых ферментов, действительно характерных для каждого пути. Затем они собрали эталонный набор из 347 геномов хемолитоавтотрофов — микробов, получающих энергию из неорганических химикатов и строящих биомассу из CO₂. Каждый геном в этом большем наборе был вручную связаны с конкретными путями фиксации CO₂ на основе литературы, что предоставило надёжный эталон для тестирования предсказаний.
Маркерные гены и простые правила вместо «чёрных ящиков»
Используя 15 референсных геномов, команда идентифицировала «маркерные гены» для каждого из семи путей фиксации CO₂ и сопоставила их со стандартными идентификаторами KEGG Orthology (KO). Вместо опоры на непрозрачные методы машинного обучения они закодировали прозрачные правила о том, как эти маркеры комбинируются. Некоторые реакции могут выполняться любым из нескольких альтернативных ферментов, что реализовано через правило «one_of». Другие требуют мультисубъединичных комплексов и должны иметь «all_of» определённый набор KO. Для восстановительного пути глицина, где не все компоненты полностью понятны, инструмент использует правила «at_least», требующие наличия минимального числа субъединиц. Эти логические правила хранятся в машинно-читаемом JSON-файле, который формирует основную базу знаний для AutoFixMark.
Лёгкий инструмент, который превосходит устоявшееся ПО
Сам AutoFixMark представляет собой небольшой программный продукт на Python, построенный на правилах. На вход он принимает список идентификаторов KO для генов в геноме микроорганизма, обычно получаемый с помощью отдельного инструмента KofamScan, и проверяет, какие маркерные правила выполнены для каждого из семи путей. Авторы сравнили AutoFixMark с двумя широко используемыми инструментами метаболической аннотации — METABOLIC и gapseq — используя их эталонный набор из 347 геномов. Все три инструмента хорошо справлялись с классическими путями, такими как цикл Калвина, восстановительный цикл трикарбоновых кислот и путь Вуда–Люнтхальда. Тем не менее AutoFixMark явно превзошёл остальные при работе с новыми или менее распространёнными путями, такими как цикл 3-гидроксипропионата/4-гидроксибутирата, цикл дикарбоксилата/4-гидроксибутирата и восстановительный путь глицина, некоторые из которых вообще не поддерживаются конкурирующим ПО.
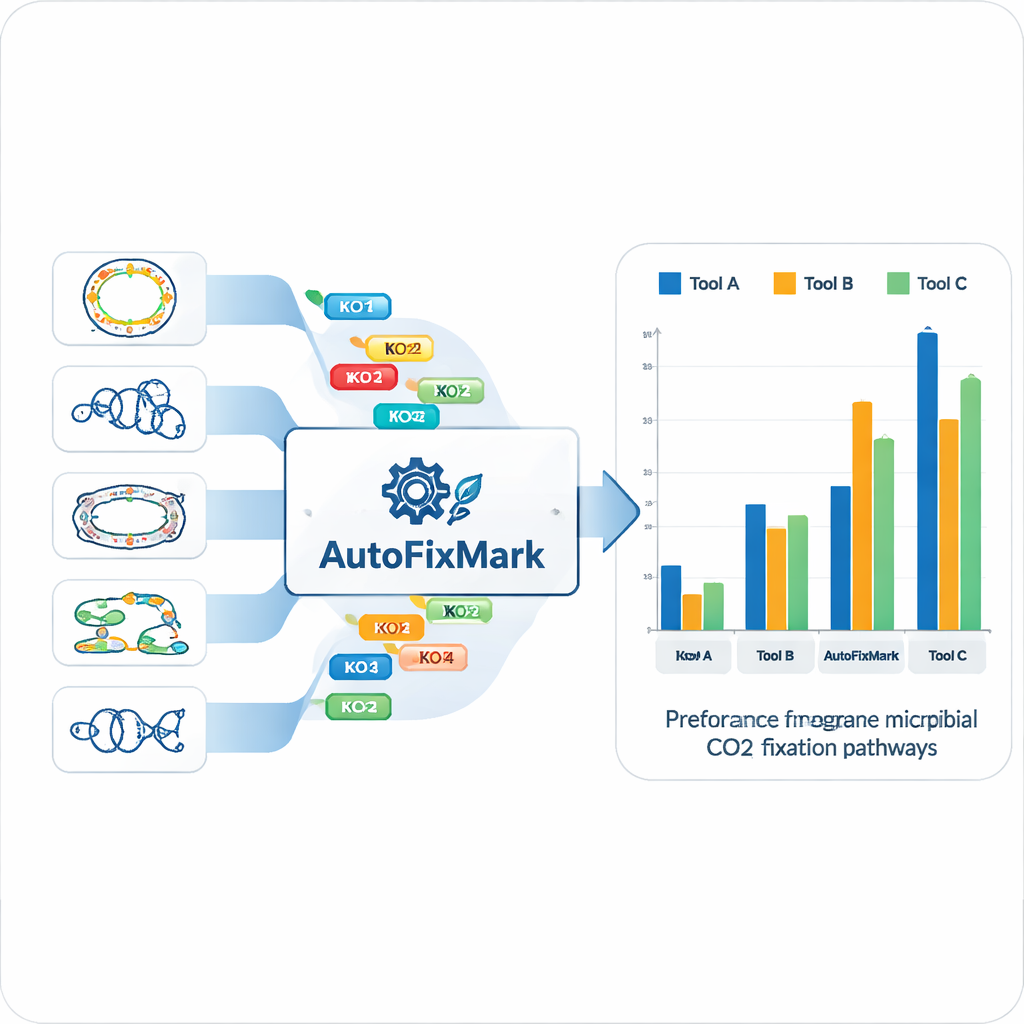
Что эти результаты значат для климатических и экологических исследований
Курированные наборы генов, программа AutoFixMark и полный эталонный набор геномов доступны публично. Это означает, что исследователи теперь могут скринировать как изолированные микроорганизмы, так и геномы, собранные из метагеномов, чтобы определить, какими стратегиями фиксации CO₂ они генетически оснащены. Важно, что авторы подчёркивают: AutoFixMark предсказывает генетический потенциал, а не то, активен ли путь в реальных условиях. Многие из этих биохимических маршрутов могут работать в обратном направлении, в зависимости от энергетического баланса клетки. Тем не менее наличие надёжного и прозрачного способа помечать микробы, фиксирующие CO₂, поможет учёным картировать, где и как жизнь извлекает углерод из атмосферы, направлять эксперименты по новым путям и поддерживать разработку будущих биотехнологий, основанных на CO₂.
Цитирование: Kawashima, S., Okabeppu, Y., Miyazawa, S. et al. A curated resource of chemolithoautotrophic genomes and marker genes for CO₂ fixation pathway prediction. Sci Data 13, 121 (2026). https://doi.org/10.1038/s41597-026-06655-z
Ключевые слова: микробная фиксация углерода, автотрофный метаболизм, аннотация геномов, захват CO2, метагеномика