Clear Sky Science · ru
Комплексный профиль транскриптома спорадических медуллярных раков щитовидной железы
Почему этот редкий рак щитовидной железы важен
Медуллярный рак щитовидной железы — редкая форма рака щитовидной железы, которая ведёт себя более агрессивно, чем большинство опухолей этой локализации, и часто обнаруживается уже на поздних стадиях. Из‑за редкости заболевания у врачей и исследователей было мало данных, чтобы понять, почему одни опухоли растут и метастазируют быстрее других или почему одни пациенты лучше реагируют на лечение. Это исследование закрывает этот пробел, проводя глубокий геномный анализ активности тысяч генов в 72 опухолях и создавая одну из самых полных на сегодня молекулярных «снимков» болезни.
Заглянуть внутрь опухолевой клетки
Вместо того чтобы сосредотачиваться только на ДНК‑мутациях, авторы изучили «транскриптом» опухоли — полный набор РНК‑сообщений, производимых активными генами в раковых клетках. Эти РНК‑сообщения действуют как оперативные отчёты о том, что делает клетка в данный момент. Секвенирование РНК из свежезамороженных образцов позволило увидеть, какие гены включены сильнее, какие — слабее, и как склеиваются транскрипты. Такой подход помогает выявлять скрытые закономерности, которые классические генетические тесты могут пропустить, например изменения в регуляции генов или их объединении.
Кто был исследован и что измеряли
Команда проанализировала опухоли у 72 человек со спорадическим (несемейным) медуллярным раком щитовидной железы. Немного более половины пациентов были женщины, а медианный возраст на момент операции составил 61 год. Примерно в 58% опухолей обнаруживали изменения в гене RET, и около 24% несли мутации в генах семейства RAS — оба фактора известны как драйверы этого рака. Сначала учёные проверили качество образцов и степень смешения с нормальной тканью щитовидной железы или иммунными клетками, оценивая ключевые маркёры — например, кальцитонин, повышенный при этих опухолях, и тиреоглобулин, характерный для нормальных клеток щитовидной железы, который оставался низким. Затем использовали общепринятые вычислительные инструменты для выравнивания ридов РНК по человеческому геному, подсчёта активности генов и поиска различий между клиническими и генетическими группами.
Активность генов связана со стадией и мутациями
При сравнении опухолей ранних стадий (I–II) и более продвинутых (III–IV) исследователи выявили 760 генов, чья активность явно различалась между группами. Это означает, что профиль экспрессии генов несёт сильные подсказки о степени прогрессирования рака. Также они сравнили опухоли с мутациями RET или RAS и те, в которых ни одна из этих мутаций не присутствовала, обнаружив более 1200 генов с изменённой активностью. Отдельный анализ сосредоточился на опухолях с конкретной мутацией RET, называемой M918T, которая давно связана с особенно неблагоприятным прогнозом. В этих опухолях 529 генов показали различную активность по сравнению с RET‑нормальными опухолями, а сам ген RET экспрессировался сильнее, что подчёркивает, насколько существенно одно изменение может перестроить поведение клетки.
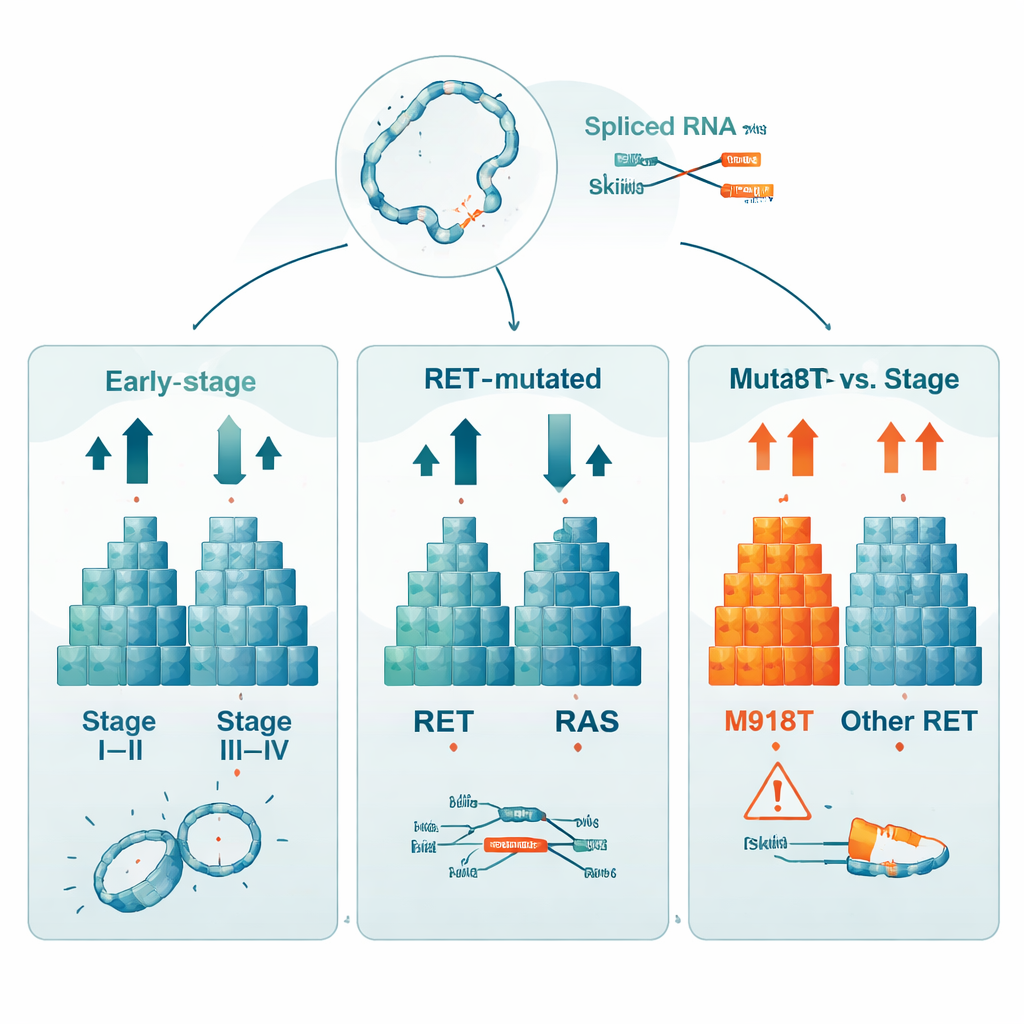
Скрытые перестройки и переработка сообщений
Помимо простых «вкл/выкл» изменений в генах, исследование искало более глубокие формы нарушения РНК. Команда выявила 59 различных транскриптов‑фьюзов, где куски разных генов аномально сшиваются на уровне РНК. Большинство из них были редкими, и самая частая фьюз‑траектория может отражать технический артефакт, но каталог показывает, что такие перестройки можно систематически извлекать из данных. Учёные также зафиксировали тысячи событий альтернативного сплайсинга, когда сегменты транскриптов пропускаются, меняются местами или сохраняются. Хотя в каждом клиническом сравнении (по стадии, типу мутации или статусу M918T) общие числа таких сплайсинговых событий были сопоставимы, конкретные события в основном различались, намекая на множественные, частично независимые пути, которыми опухолевые клетки перенастраивают свои генетические сообщения.
Что этот ресурс даёт пациентам и учёным
Для пациентов эта работа пока не выливается в немедленное появление нового препарата или теста, но она закладывает необходимую основу. Публикуя все обработанные данные секвенирования РНК в открытом доступе, авторы предоставляют богатый ресурс, который другие исследователи могут использовать для поиска новых биомаркёров прогноза, уточнения классификации медуллярных раков щитовидной железы или выявления уязвимостей, нацеливание на которые возможно в будущих терапиях, включая новое поколение селективных ингибиторов RET. Проще говоря, это исследование предлагает детальную «карту активности» генов опухоли на большом наборе реальных случаев, дающую учёным инструменты для лучшего понимания, почему этот редкий рак ведёт себя так по‑разному у разных людей и как в будущем лечение может стать более точечным.
Цитирование: Palumbo, D., Melone, V., Palo, L. et al. Comprehensive Transcriptome Profiling of Sporadic Medullary Thyroid Carcinomas. Sci Data 13, 234 (2026). https://doi.org/10.1038/s41597-026-06550-7
Ключевые слова: медуллярный рак щитовидной железы, геномика рака, секвенирование РНК, мутация RET, персонализированная онкология