Clear Sky Science · ru
Метаболизм витамина B2 повышает стабильность FSP1 для предотвращения ферроптоза
Как обычный витамин помогает клеткам выбирать между жизнью и смертью
Наши клетки постоянно балансируют на грани между выживанием и самоуничтожением. Одна из драматичных форм клеточной гибели — ферроптоз — привлекает внимание, поскольку может избирательно уничтожать раковые клетки, устойчивые к другим методам лечения. В этом исследовании показано, что повседневный нутриент — витамин B2, или рибофлавин — тихо смещает равновесие, стабилизируя ключевой белок защиты. Понимание этой скрытой связи между питанием, клеточным метаболизмом и гибелью раковых клеток может помочь учёным разработать более умные терапии и уточнить будущие рекомендации по питанию.
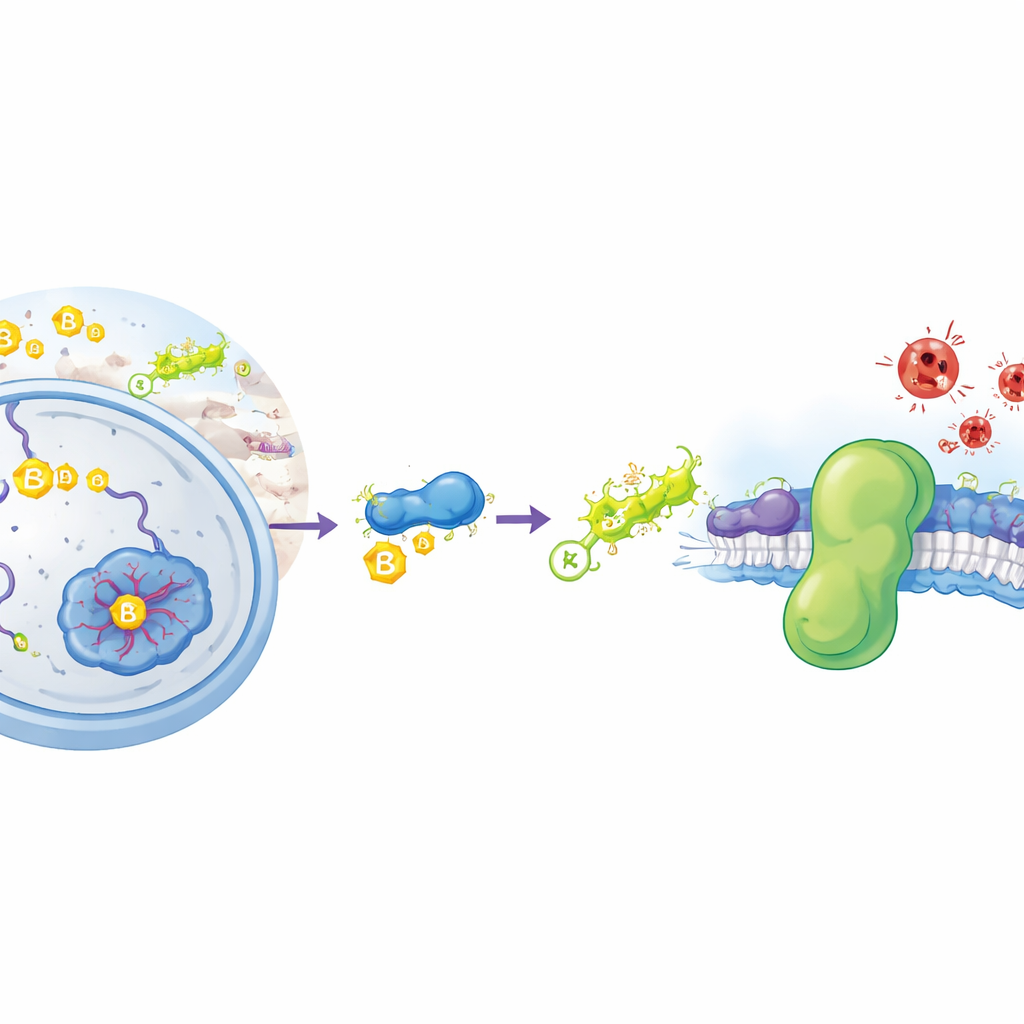
Особый вид «ржавчины» внутри клеток
Ферроптоз — это тип клеточной смерти, вызванный химическим процессом, сходным с ржавлением металла: неконтролируемым окислением липидов в мембранах клеток. Когда эти жиры разрушаются, мембраны теряют целостность и клетки разрушаются. Клетки обычно используют несколько защит, чтобы этого не допустить. Одним из основных щитов является фермент GPX4, который при помощи небольшого молекулярного антиоксиданта глутатиона детоксифицирует вредные липидные перекиси. Второй, параллельный, щит — белок FSP1, расположенный на клеточных мембранах, который использует малые липидоподобные молекулы, чтобы перехватывать разрушительные радикалы прежде, чем те распространится. Раковые клетки часто повышают уровень FSP1, чтобы избежать ферроптоза, что делает этот белок важной мишенью для новых противораковых препаратов. До настоящего времени учёным было неясно, как именно клетки контролируют синтез и продолжительность жизни FSP1.
Создание клеточного «указателя топлива» для блокировщика смерти
Чтобы обнаружить скрытых регуляторов FSP1, исследователи сначала создали в человеческих остеосаркомных клетках флуоресцентный репортер. Они пометили естественный белок FSP1 зелёным светом и добавили синий сигнал, сообщающий о количестве его матричной РНК. Эта хитрая конструкция позволила отделить изменения активности гена (синий) от изменений стабильности белка (зелёный). С помощью этой двухцветной системы они затем использовали CRISPR–Cas9, чтобы систематически нарушить практически каждый ген в геноме, и отбирали клетки с высоким или низким уровнем FSP1. Сравнивая, какие направляющие РНК обогащались в каждой группе, они составили карту сотен генов, которые либо повышают, либо понижают уровень FSP1, действуя на уровне регуляции гена или распада белка.
Скрытая роль витамина B2: создание стабилизирующей рукояти
Среди наиболее заметных попаданий оказались два фермента — рибофлавин-киназа (RFK) и синтаза FAD (FLAD1), которые превращают витамин B2 в кофактор FAD. FSP1 является флавопротеином, который обычно плотно связывает FAD для выполнения своих химических реакций. Когда RFK или FLAD1 были удалены, или когда клетки выращивали в среде, лишённой витамина B2, уровни белка FSP1 резко падали, хотя активность его гена оставалась примерно прежней. Команда показала, что эта потеря делала клетки гораздо уязвимее к ферроптозу при блокировке GPX4. Важно, что сам витамин B2 не действовал как классический антиоксидант: в чувствительном тесте in vitro он не остановил окисление липидов, в отличие от витамина E. Вместо этого добавление FAD (и частично его предшественника FMN) к дефицитным клеткам восстанавливало как уровни FSP1, так и устойчивость к ферроптотической гибели, тогда как простой избыток витамина B2 не помогал, если отсутствовали ферменты его обработки.
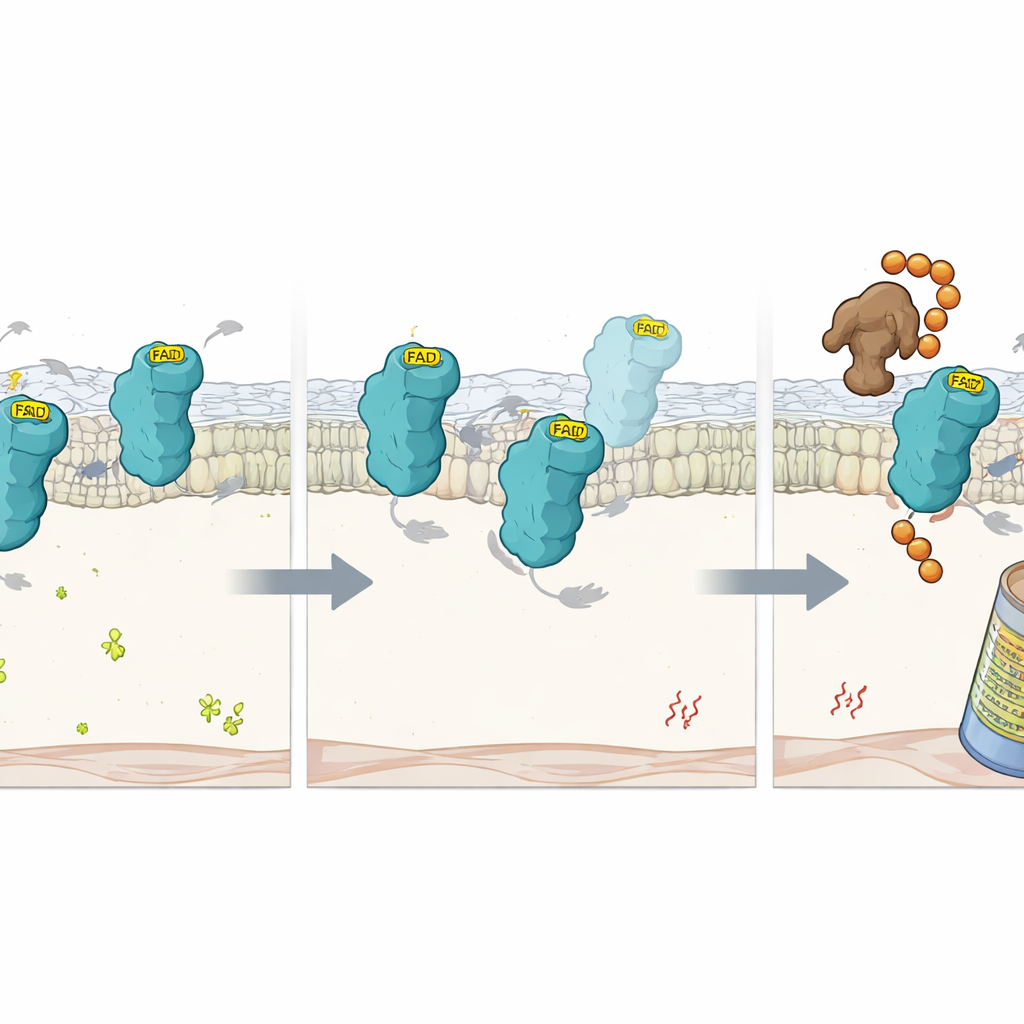
Что происходит, когда кофактора не хватает
Чтобы рассмотреть процесс подробнее, учёные изучили точечные мутации в FSP1, которые лишают его способности удерживать FAD. Эти мутантные белки всё ещё складывались в в основном нормальные конформации, но теряли FAD и каталитическую активность. Внутри клетки они распадались гораздо быстрее, чем нормальный FSP1, если только не блокировать протеасому — машину клетки по разборке белков. Это позволило предположить, что связывание FAD само по себе действует как стабилизирующая рукоять, защищающая FSP1 от маркировки как дефектного. Используя ещё один целевой CRISPR-скрин при низком уровне FAD, команда выявила E3-лигазу RNF8 как ключевой фактор, распознающий FAD-свободный FSP1. При удалении RFK RNF8 присоединял цепочки убиквитиновых меток к «пустому» белку, направляя его на уничтожение протеасомой. Удаление RNF8 замедляло распад FSP1 в бедных на FAD клетках, хотя не могло восстановить утраченные защитные функции без кофактора.
От молекулярной схемы к идеям противораковой терапии
Собрав эти куски вместе, авторы предлагают простую, но мощную модель. Витамин B2, после превращения в FAD при участии RFK и FLAD1, связывается с FSP1 и необходим как для его биохимической активности, так и для его долговечности. Когда поставка витамина B2 или его обработка нарушается, вновь синтезированный FSP1 не может захватить FAD, помечается RNF8 и быстро разрушается протеасомой, оставляя клетки более уязвимыми к ферроптотическому повреждению. Данные по раку указывают на то, что опухоли с повышенной экспрессией RFK более устойчивы к препаратам, индуцирующим ферроптоз, что подчёркивает практическую значимость этого пути. Для неспециалистов ключевое сообщение таково: знакомый витамин выполняет гораздо более тонкую роль, чем просто выступает в роли антиоксиданта — он помогает решать, будет ли мощный белок-противодействие смерти стоять на страже или будет сметён прочь. Путём регулировки метаболизма витамина B2 или стабильности FSP1 будущие методы лечения могут лучше использовать ферроптоз для уничтожения раковых клеток, при этом щадя здоровую ткань.
Цитирование: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Ключевые слова: ферроптоз, витамин B2, FSP1, гибель раковых клеток, клеточный метаболизм