Clear Sky Science · ru
Картография химер транposable element–гены: происхождение и роль в повышении пластичности транскриптома
Скрытые пассажиры в нашей ДНК
Значительная часть нашей ДНК состоит из древних вирусных пришельцев — транспозируемых элементов, фрагментов генетического кода, которые некогда «перепрыгивали» по геномам, как паразитирующие попутчики. В этом исследовании показано, что эти древние вирусные фрагменты — не просто молчаливый мусор: они могут встраиваться в наши собственные гены, создавая гибридные сообщения, помогать клеткам адаптироваться к меняющимся условиям и иногда способствовать развитию заболеваний. Проследив эти гибриды в процессе развития, старения и при раке, авторы выявляют неожиданный способ, которым вирусная ДНК продолжает формировать биологию человека и сегодня.
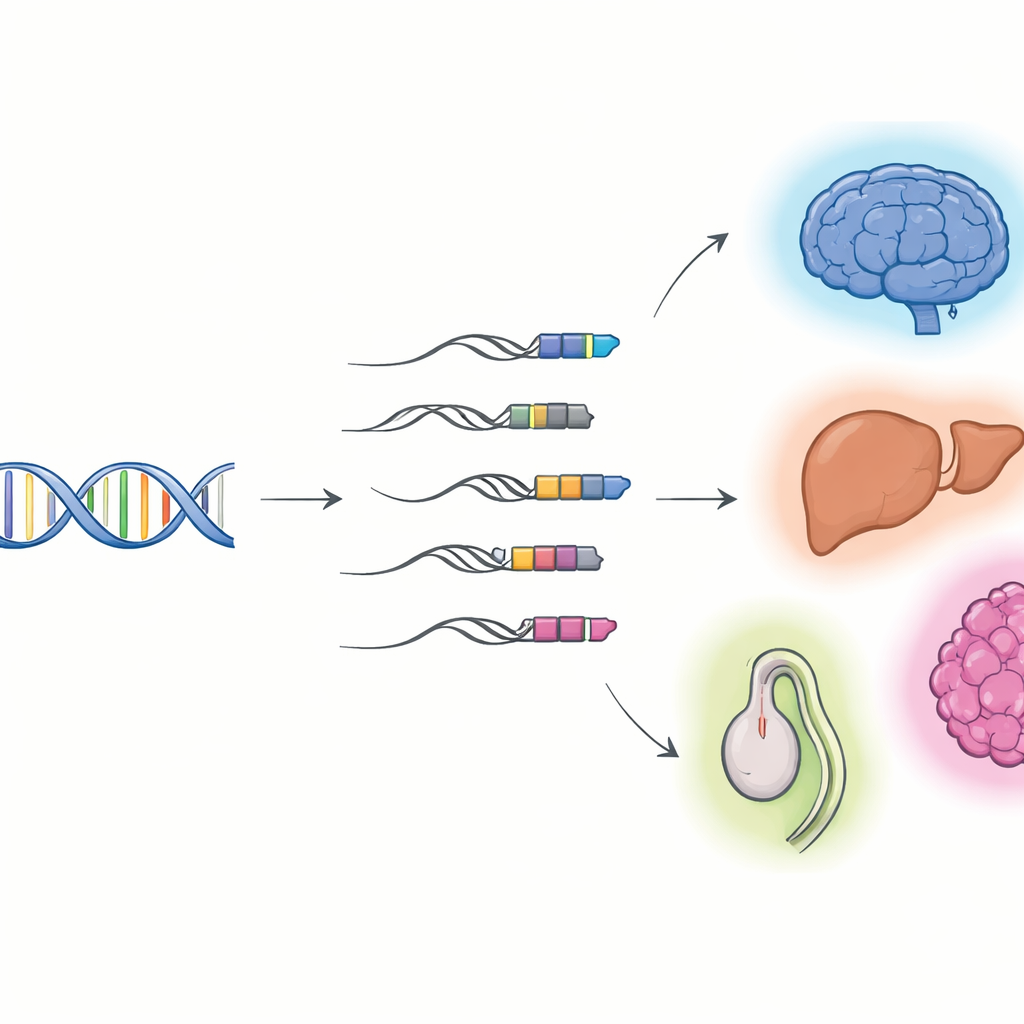
Когда вирусная ДНК становится частью наших генов
Исследователи сосредоточились на «TE–gene химерах»: молекулах РНК, которые начинаются в транспозируемом элементе, а затем продолжаются в хозяевом гене. Используя долгочитабельное секвенирование, способное захватить полную молекулу РНК «от конца до конца», в сочетании со стандартным короткочитабельным секвенированием, они составили подробные каталоги этих гибридов в клетках и органах мыши и человека. Было обнаружено тысячи ранее неизвестных химерных транскриптов, большинство из которых представляют собой некодирующие РНК, а не шаблоны для белков. Многие начинаются в классе вирусных рудиментов, называемых длинными терминальными повторами (LTR), которые часто находятся в начале генов и могут действовать как альтернативные выключатели. Разные ткани и органы используют разные наборы таких химер, особенно высокая активность отмечена в мозге, печени и семенниках, а их использование меняется по мере развития тканей от фетальных к взрослым стадиям.
Химеры при старении и раке
Чтобы понять, как эти вирусно-хозяевые гибриды ведут себя в реальных популяциях, команда проанализировала большие человеческие наборы данных, охватывающие десятки тканей от сотен людей, а также образцы опухолей. Они идентифицировали несколько сотен надежных химер, которые повторяются у разных людей. Их экспрессия варьирует не только между органами, но и с возрастом: в таких тканях, как кровь и мозг, некоторые LTR-инициируемые химеры снижаются у пожилых людей, тогда как в отдельных периферических тканях они увеличиваются. Во многих типах рака эти LTR-основанные гибриды в целом повышены в опухолях по сравнению с прилежащей нормальной тканью, и у пациентов, чьи опухоли экспрессируют больше таких транскриптов, прогноз обычно хуже. В наборах данных от людей, устойчивых к химио- или иммунотерапии, гены, затронутые новыми LTR-опосредованными экзонами, часто участвуют в путях, связанных с действием этих препаратов, что предполагает, что TE-химеры могут помогать опухолям перестраиваться под давлением лечения.
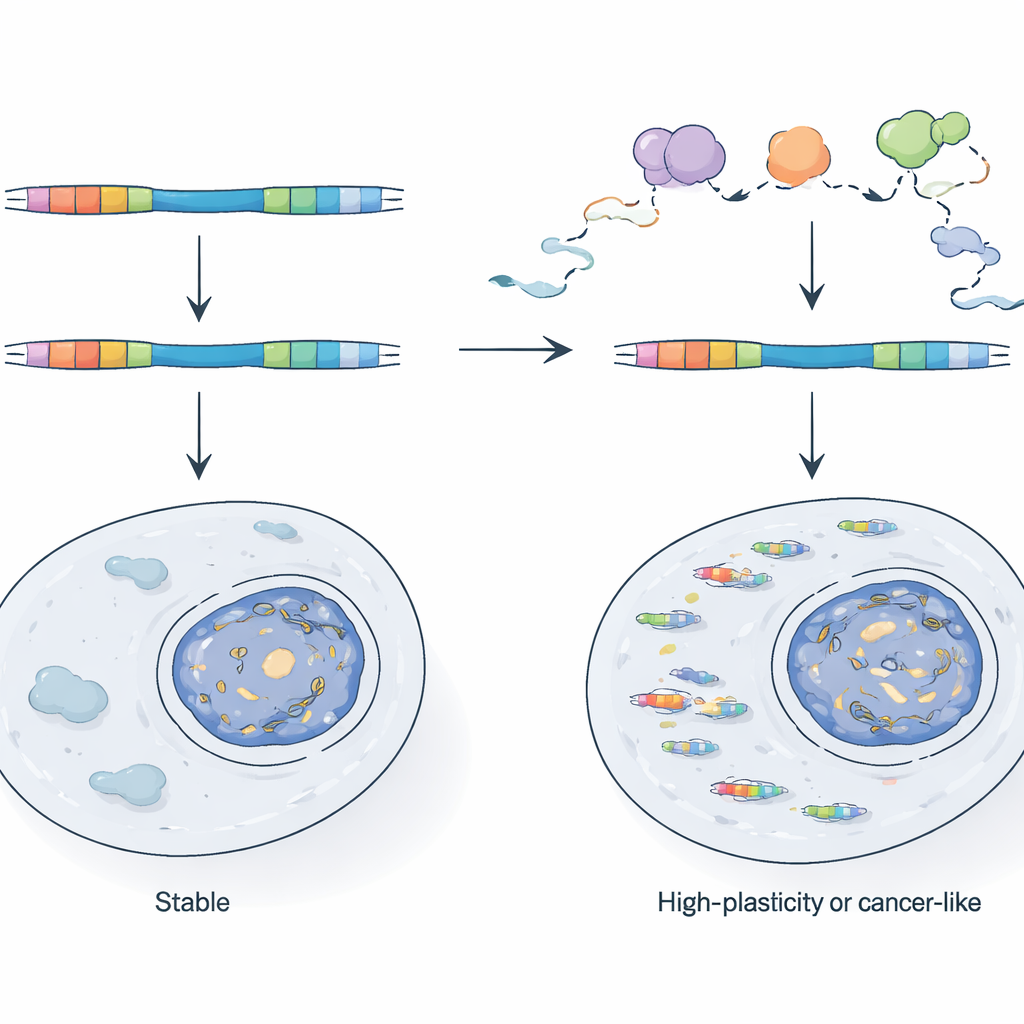
Как клетки сдерживают вирусные гибриды
Учитывая их потенциал, почему TE-химеры не захватывают клетки? Авторы показывают, что клетки полагаются на систему контроля качества РНК, центром которой является ядерный экзосомный комплекс, чтобы патрулировать и уничтожать многие из этих транскриптов по мере их синтеза. Когда они генетически нарушают ключевой компонент экзосомы в стволовых клетках мыши, промотеры, инициируемые LTR, становятся гораздо более активными, и поток химерных РНК резко возрастает. Сравнивая недавно синтезированную РНК со стабильной РНК, они демонстрируют, что одни LTR обычно удерживаются под контролем потому, что их транскрипты быстро разрушаются, тогда как другие регулируются на уровне частоты запуска транскрипции. Эти активные LTR, как правило, локализованы в участках генома, которые уже доступны и часто транскрибируются, что указывает на то, что простое соседство с активным геном или антисмысловой транскрипцией может помочь вирусному фрагменту уйти от традиционного эпигенетического подавления.
Сплайсинг, пластичность стволовых клеток и вирусный «главный переключатель»
Ситуация усложняется, когда нарушается машинерия сплайсинга клетки. Авторы подавляют несколько ключевых факторов сплайсинга или химически ингибируют сплайсосому и наблюдают тот же результат, что и при потере экзосомы: сильное усиление LTR-инициируемых химер и коротких, бедных интронами генов. Среди «победителей» — MERVL, эндогенный ретровирус, активный в очень ранних эмбрионах мыши. Когда внутренняя последовательность MERVL и связанные с ней факторы транскрипции повышаются в активности, стволовые клетки смещаются в более «тотипотентное» состояние, напоминающее ранние эмбриональные клетки, способные образовать все ткани. Наоборот, деградация MERVL-РНК с помощью антисмысловых олигонуклеотидов ослабляет этот сдвиг и снижает активность LTR-промотеров, что указывает на то, что MERVL действует как главный переключатель, способный запустить более широкую сеть TE-химер и пластичности клеточных состояний.
Вирусные инновации в ходе эволюции
Просматривая множество млекопитающих геномов, команда отследила, когда различные семейства TE начали жертвовать экзонами для генов хозяина. И у человека, и у мыши относительно молодые семейства LTR особенно склонны формировать химеры в «сенс»-ориентации, которую можно прочесть как часть транскриптов хозяина. Эта картина предполагает, что новые волны вставок TE неоднократно поставляли сырой материал в сети регуляции генов в ходе эволюции. Вместо того чтобы быть исключительно вредоносными, эти вставки могут испытываться транскрипционной и деградационной машинерией клетки: большинство из них подавляется или разрушается, но меньшинство оказывается в правильном месте и контексте, чтобы быть заимствованным в качестве полезных регуляторных элементов или новых стартов генов.
Почему эти вирусные реликты важны
Для неспециалиста эта работа показывает, что большая и когда-то отвергнутая часть нашего генома активно формирует то, как читаются гены, как клетки меняют свою идентичность и как прогрессируют заболевания. Древние вирусные последовательности могут превращаться в альтернативные «входные двери» генов, порождая гибридные РНК, которые обычно контролируются клеточными системами очистки. Когда этот контроль или нормальный сплайсинг дают сбой, эти гибриды могут вспыхивать, подталкивая стволовые клетки к более гибким состояниям или помогая опухолям адаптироваться и приобретать резистентность к терапии. На протяжении миллионов лет эволюция многократно экспериментировала с этими вирусными фрагментами, превращая многие из них из геномных паразитов в строительные блоки регуляторной сложности — и оставив нам транскриптом, куда более пластичный и динамичный, чем простое перечисление генов.
Цитирование: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Ключевые слова: транспозируемые элементы, химерные транскрипты, контроль качества РНК, пластичность стволовых клеток, эволюция рака