Clear Sky Science · ru
Адаптация митохондриального импорта белков к стрессу через деградацию DNAJC15, опосредованную OMA1
Как клетки справляются, когда их «электростанции» испытывают стресс
Каждая клетка вашего тела зависит от крошечных структур — митохондрий — которые превращают питательные вещества в доступную энергию. Подобно миниатюрным фабрикам, митохондрии постоянно импортируют новые детали — белки, синтезированные в других частях клетки — чтобы поддерживать свою работу. В этой статье показано, что при стрессе или повреждении митохондрий клетки целенаправленно замедляют поток такого импорта белков. Это защищает их от перегрузки и координирует более широкий стрессовый ответ, вовлекающий не только митохондрии, но и другой важный компартмент — эндоплазматический ретикулум.
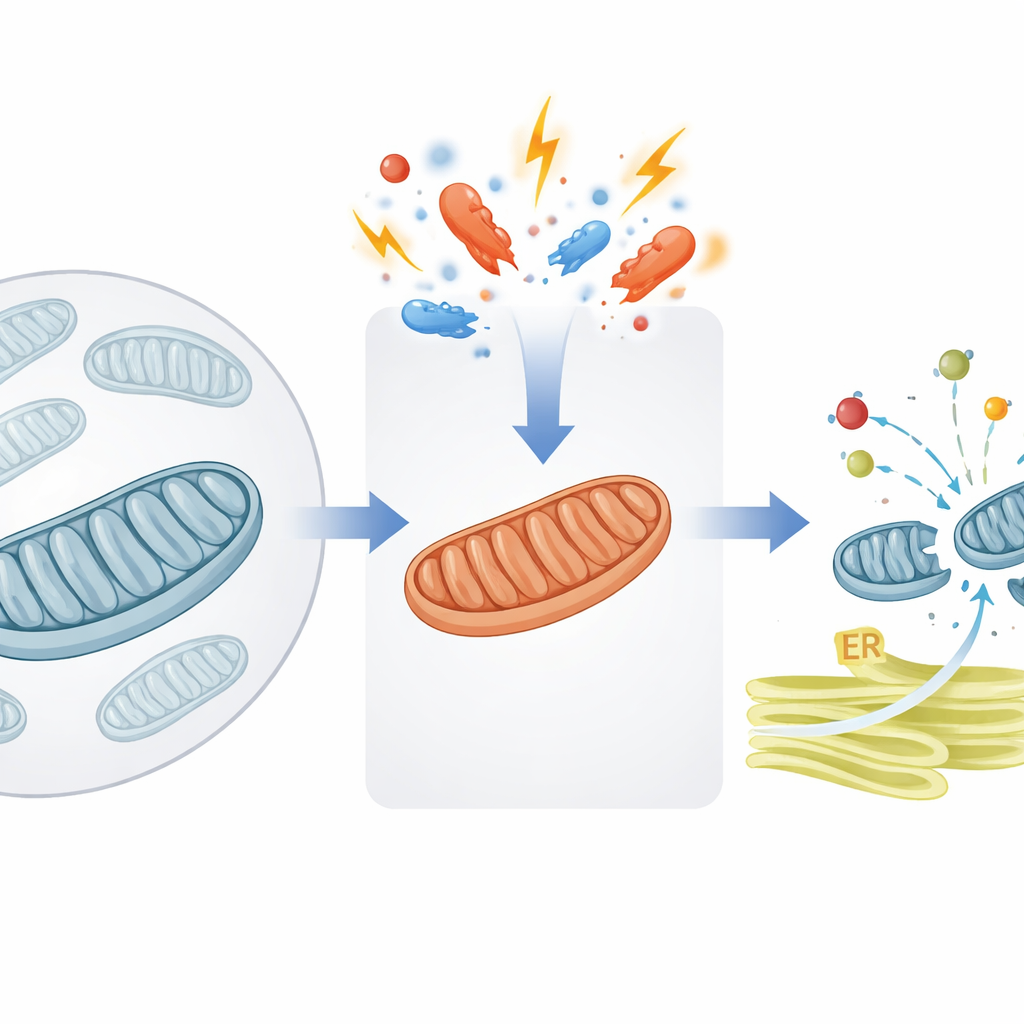
Предохранительный клапан для движения белков в митохондриях
Митохондрии зависят от тысяч белков, которые сначала построены в общем веществе клетки, а затем доставляются внутрь органеллы. Авторы сосредотачиваются на важном шлюзе во внутренней мембране митохондрий, поддерживаемом вспомогательным белком DNAJC15. В нормальных условиях DNAJC15 помогает протянуть новые «пакеты» белков через импортный канал и доставить их в митохондриальный матрикс, где многие из них становятся частью энергообразующего механизма, известного как окислительное фосфорилирование (OXPHOS). Исследование показывает, что при митохондриальном стрессе — например, при нарушении выработки энергии или изменении свойств мембраны — клетка включает молекулярный переключатель, уменьшающий объём белкового импорта в органеллу.
OMA1: фермент, активируемый при стрессе
В основе этого переключателя лежит чувствительный к стрессу фермент OMA1, расположенный во внутренней митохондриальной мембране. Когда митохондрии испытывают проблемы, OMA1 активируется и отрезает DNAJC15 в определённой позиции рядом с его N‑концом. Этот разрез порождает укороченную версию DNAJC15, которая быстро расщепляется другим митохондриальным протеазным комплексом — m‑AAA. В результате полного, пригодного для импорта вида DNAJC15 становится меньше. Авторы показывают, что клетки, лишённые DNAJC15 или в которых DNAJC15 быстро уничтожается после активации OMA1, хуже импортируют новые белки в митохондрии, особенно те, что необходимы для сборки и поддержания комплексов OXPHOS.
Замедление сборки энергоагрегатов в соответствии со состоянием митохондрий
С помощью крупномасштабных измерений белков и тестов импорта команда установила, что DNAJC15 особенно важен для доставки в митохондрии белков, участвующих в экспрессии генов и сборке дыхательной цепи. При отсутствии DNAJC15 эти белки медленнее накапливаются внутри митохондрий, а способность органелл потреблять кислород и обеспечивать выработку энергии — по данным изолированных митохондрий — снижается, особенно в отношении комплекса I дыхательной цепи. Другой компонент импортного канала, TIMM17A, действует совместно с DNAJC15: потеря обоих приводит к особенно сильным нарушениям в уровнях митохондриальных рибосомальных белков и компонентов OXPHOS. В совокупности эти данные указывают, что опосредованная OMA1 деградация DNAJC15 служит способом временно приостановить строительство новой энергетической аппаратуры до восстановления органеллы.
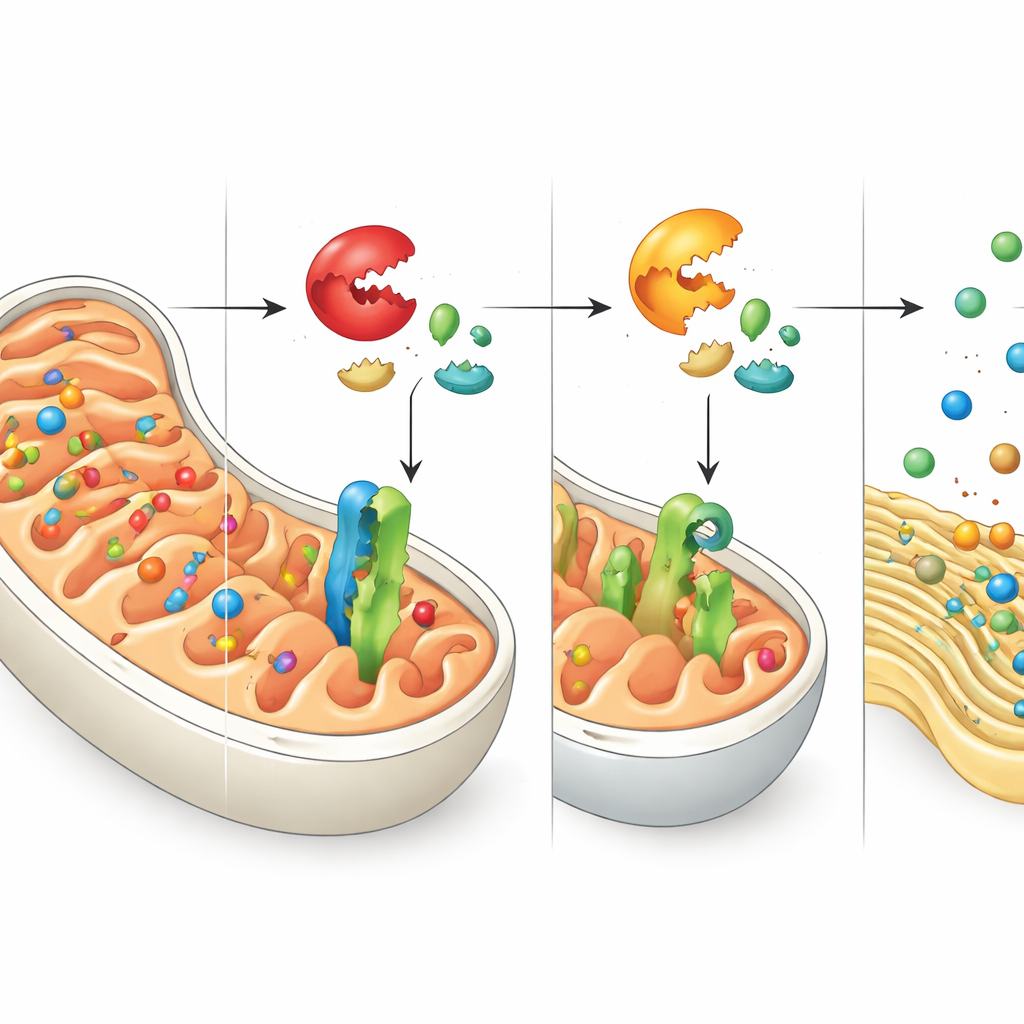
Неправильно доставленные «посылки» и сигнал о помощи в сторону ЭР
Отключение DNAJC15 не прекращает синтез митохондриальных белков — в основном это препятствует их достижению назначенного места. Авторы проследили, куда попадают эти заблокированные белки, и обнаружили, что многие оказываются в эндоплазматическом ретикулуме (ЭР), сети мембран, которая обычно помогает сворачивать и обрабатывать другие наборы белков. Эти «заблудшие» митохондриальные белки встраиваются в мембраны ЭР, нарушая собственный контроль качества ЭР. В ответ клетка запускает защитную программу, известную как ответ на накопление несвёрнутых белков, в частности через ветвь, контролируемую сенсором ATF6. Этот ответ повышает способность ЭР справляться с неправильносвёрнутыми или неправильно направленными белками, открывая тесную координацию между системами стресса митохондрий и ЭР.
Координированное замедление во имя защиты клетки
Вместе исследование рисует картину встроенной тормозной системы для биогенеза митохондрий. При стрессе митохондрий OMA1 обрезает и косвенно уничтожает DNAJC15, уменьшая поток новых энергоотносящихся белков в скомпрометированные органеллы. Часть этих белков временно буферизуется в ЭР, которое разворачивает собственную защитную программу. Связывая способность импорта митохондрий с состоянием органелл и привлекая ЭР как запасное хранилище для избытка белков, клетки избегают засорения повреждённых митохондрий и выигрывают время, чтобы либо отремонтировать их, либо удалить. Для непрофессионального наблюдателя эта работа демонстрирует, насколько глубоко интегрированы наши клеточные системы контроля качества: даже самые незначительные сбои в одном компартменте ощущаются и уравновешиваются другими, чтобы поддерживать выработку энергии — и жизнь в целом.
Цитирование: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Ключевые слова: митохондриальный стресс, импорт белков, клеточный контроль качества, окислительное фосфорилирование, эндоплазматический ретикулум