Clear Sky Science · ru
Структура и функция сверхкомплекса SEAC–EGOC у дрожжей, чувствительного к аминокислотам
Как клетки решают, когда расти
Каждая клетка постоянно принимает решение: может ли она позволить себе рост или лучше беречь ресурсы. Это решение во многом зависит от аминокислот — строительных блоков белков и важного источника азота. В статье подробно показано, как дрожжевые клетки с помощью гигантского молекулярного комплекса оценивают доступность аминокислот и включают или выключают главный регулятор роста TORC1. Поскольку аналогичная схема сохраняется в клетках человека и связана с раком и метаболизмом, выводы, сделанные на дрожжах, дают представление о том, как наши клетки решают, подходят ли условия для роста.
Тонкий узел на «перерабатывающем» органоиде клетки
У дрожжей центральный комплекс принятия решений, называемый SEAC, располагается на мембране вакуоли — органеллы, выполняющей функцию перерабатывающего центра клетки. Там он взаимодействует с другим комплексом, EGOC, который передаёт информацию об уровне аминокислот. Вместе они передают сигналы в TORC1, главный переключатель роста. SEAC состоит из двух функциональных половин: SEACIT, который может выключать TORC1, и SEACAT, долгое время считавшийся фактором, сдерживающим SEACIT. Авторы использовали крио-электронную микроскопию высокого разрешения, чтобы визуализировать полный комплекс SEAC в связке с EGOC, зафиксировав этот молекулярный узел прямо там, где происходит сигнализация — на поверхности вакуоли. 
Рассматривая молекулярную архитектуру вблизи
Структура показывает SEAC как крупное ядро, состоящее из субъединиц SEACAT, от которого расходятся две гибкие «крыловидные» части SEACIT. Каждое «крыло» может связать один комплекс EGOC, то есть один SEAC способен одновременно принимать два входных сигнала. Удивительно, что EGOC присоединяется только к крыльям, а не к ядру, и общая форма SEAC почти не меняется при присутствии EGOC. Это указывает на то, что SEACAT не физически блокирует активный сайт SEACIT и не препятствует связыванию EGOC. Ориентация комплекса на мембране вакуоли также оставляет ядро SEAC обращённым в цитоплазму, где оно может взаимодействовать с дополнительными регуляторами, в то время как крылья расположены близко к мембране и оптимально ориентированы для контакта с EGOC и другими мембраносвязанными партнёрами.
Как SEAC выбирает правильный сигнал
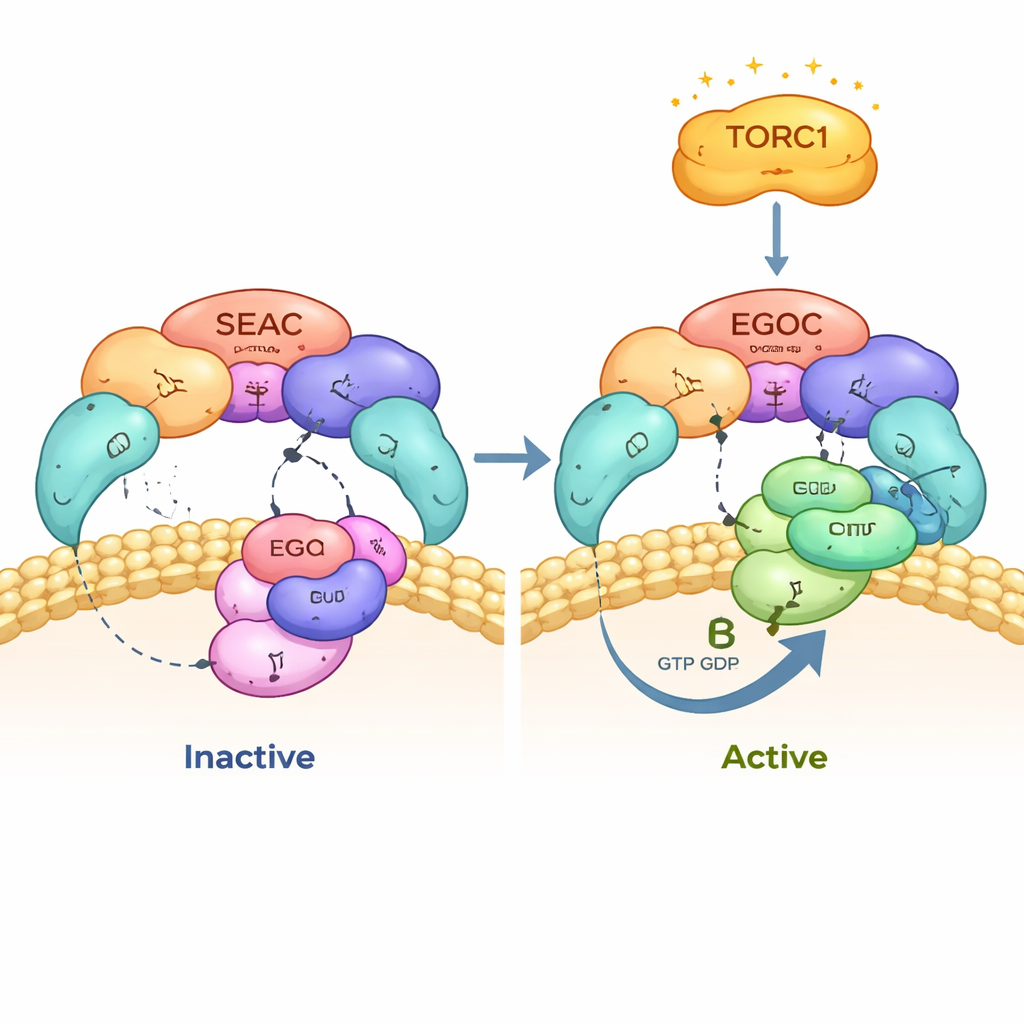
Авторы внимательно изучили контакты между SEAC и EGOC и обнаружили, что SEAC распознаёт только «активную» форму EGOC, в которой один из его малых GTP-аз, Gtr1, несёт гуанозинтрифосфатоподобный нуклеотид (GTP), а партнёр Gtr2 содержит GDP. SEACIT предоставляет каталитический «палец», который достаёт до нуклеотидного кармана Gtr1 и ускоряет гидролиз GTP, переводя EGOC из активного состояния в неактивное. Подробные карты крио-ЭМ и результаты мутационных экспериментов показывают, что этот каталитический «палец» и соседний вспомогательный остаток критически важны для взаимодействия и для правильного считывания нуклеотидного состояния. Когда авторы изменяли эти ключевые остатки, SEAC переставал правильно локализоваться на вакуоли, и EGOC не мог эффективно взаимодействовать.
Быстрый и медленный контроль переключателя роста
Чтобы понять значение этих наблюдений для живой клетки, исследователи отслеживали активность TORC1 во времени при удалении аминокислот и последующем их возвращении. В нормальных клетках TORC1 быстро выключается в течение нескольких минут при недостатке азота и столь же быстро включается при возвращении аминокислот. Когда каталитический «палец» SEACIT был инактивирован или субъединицы SEACIT удалены, TORC1 практически не реагировал в этом раннем временном окне. То же наблюдалось при удалении и Gtr1, и Gtr2, что показывает: пара SEAC–EGOC является доминирующим быстрым путём регуляции TORC1 в ответ на аминокислоты. Однако в более поздние моменты — примерно через полчаса — активность TORC1 медленно адаптировалась даже в этих мутантах, что указывает на существование отдельного, более медленного пути регуляции TORC1, независимого от этой системы GTPаз.
Неожиданная роль удалённой субъединицы
Особенно любопытный результат касается Sea2 — компонента SEACAT с гибким доменом «пропеллера», выступающим из ядра. Удаление Sea2 или лишь его пропеллера приводило к нарушениям сигнализации, почти идентичным тем, что наблюдались при потере каталитической активности SEAC: TORC1 вялo реагировал как на лишение аминокислот, так и на их возвращение. При этом Sea2 находится далеко от каталитического сайта и не контактирует напрямую с крылом SEACIT, поэтому простая блокирующая модель вряд ли объясняет эффект. Генетические эксперименты с комбинацией утраты Sea2 и каталитически неактивного варианта SEAC показали, что полная фиксация GAP-активности в положении «включено» или «выключено» нарушает быстрый отклик, тогда как требуется промежуточная регуляция. Авторы предлагают, что пропеллер Sea2 служит докинговой платформой для неизвестного фактора, который смягчает активность SEACIT, позволяя клеткам тонко регулировать TORC1, а не просто окончательно выключать его.
Что это значит для решений о росте клетки
В целом исследование переосмысляет SEAC не как два противопоставленных комплекса, а как единый интегрированный механизм, где каталитическое крыло (SEACIT) и структурное ядро (SEACAT) работают вместе, чтобы распознавать аминокислоты и оперативно регулировать переключатель роста TORC1. Каталитическое действие SEACIT на EGOC обеспечивает быстрый и точный контроль, в то время как пропеллер Sea2, вероятно, привлекает регуляторы, смягчающие эту активность. Параллельно более медленные пути гарантируют, что TORC1 в конечном итоге отражает состояние питания, даже если основной сенсор нарушен. Поскольку сходные комплексы выполняют ту же функцию в клетках человека, эти наблюдения на дрожжах проливают свет на то, как наши собственные клетки балансируют рост и доступность питательных веществ, что важно для понимания заболеваний, связанных с нарушением сигнализации TORC1.
Цитирование: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Ключевые слова: распознавание аминокислот, сигнализация TORC1, комплекс SEAC GATOR, контроль роста клеток, криоэлектронная микроскопия