Clear Sky Science · ru
Механизм и восстановление циркадной транскрипции у цианобактерий
Почему биологические часы важны — даже для бактерий
Все живые существа, от человека до крошечных микробов, ведут отсчет времени. Эти внутренние часы помогают организмам предвидеть рассвет и закат, планируя такие процессы, как питание, восстановление и рост. В статье исследуется, как простая фотосинтезирующая бактерия Synechococcus elongatus использует белковый механизм, чтобы включать и выключать гены с поразительной точностью в течение 24‑часового цикла. Воссоздав эту систему времени в пробирке, исследователи показали упрощенную версию биологических часов, которая может вдохновить новые инструменты для биотехнологии и синтетической биологии.
Крошечные часы, работающие на химии
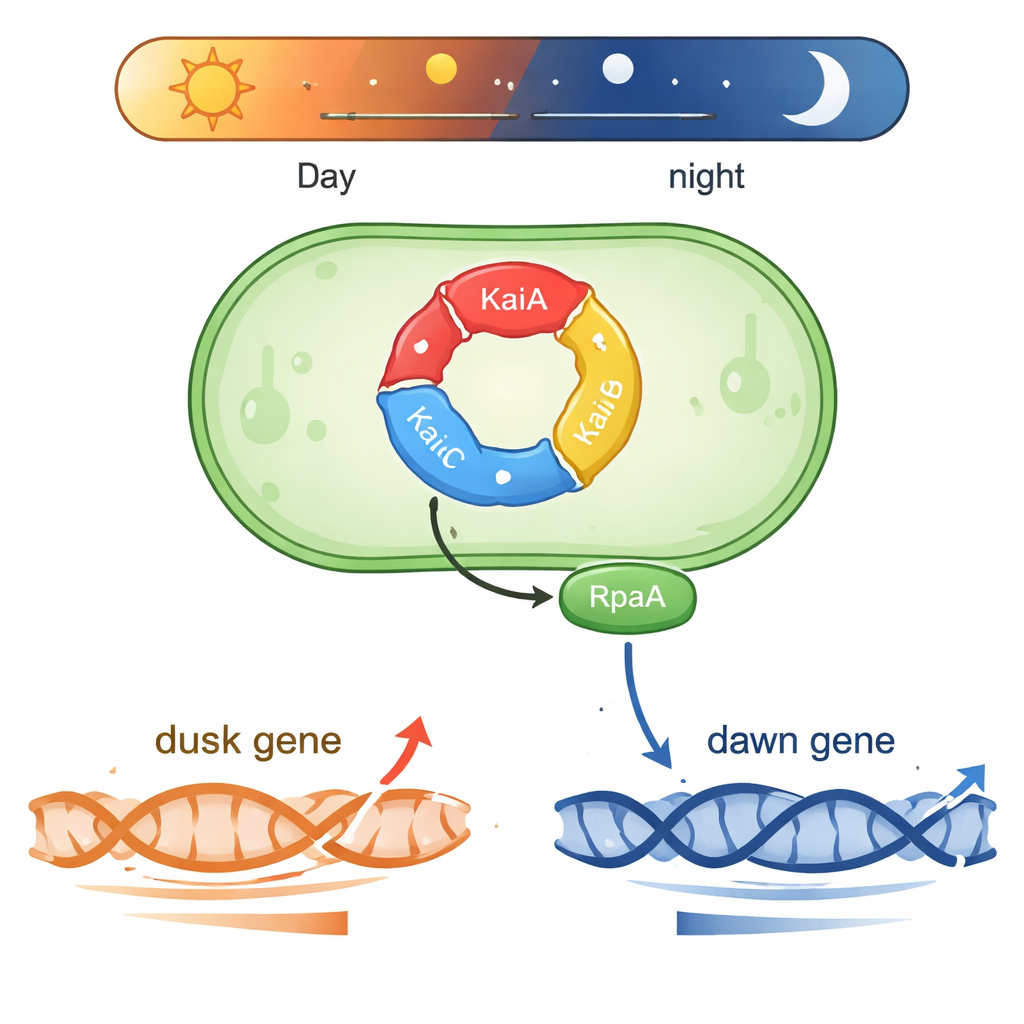
Synechococcus обитает в освещенных слоях воды и должен предсказывать суточные изменения света. В основе лежит трехкомпонентный белковый механизм из KaiA, KaiB и KaiC. Эти белки передают фосфатные группы по циклу с периодом примерно 24 часа, образуя биохимический «передаточный механизм», который сохраняет время даже за пределами клетки. Два других белка, SasA и CikA, считывают состояние фосфорилирования KaiC и используют эту информацию для управления белком RpaA. Когда RpaA фосфорилирован, он связывается с ДНК и действует как главный переключатель для сотен генов, активность которых повышается и понижается либо около субъективного «рассвета», либо «заката» при постоянном освещении.
Один белок — два противоположных режима генов
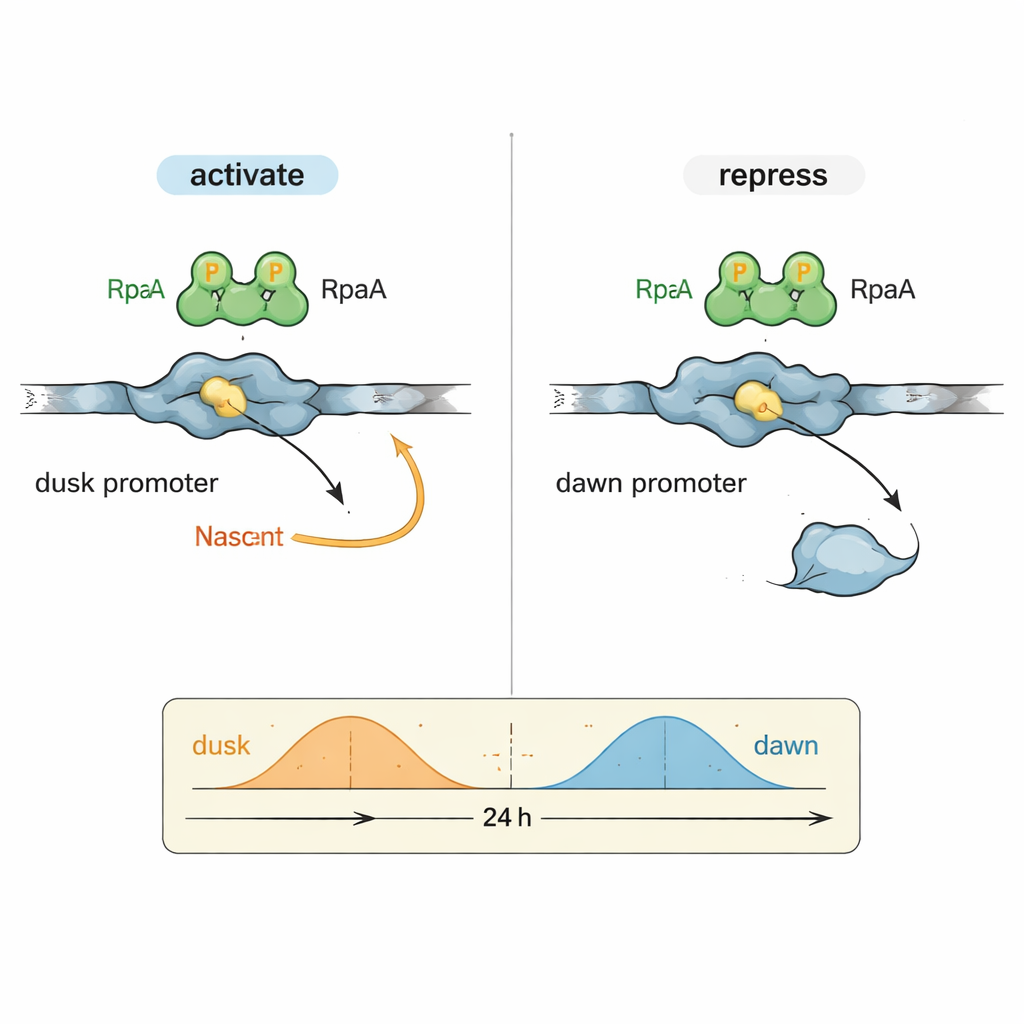
Загадкой в циркадной биологии было то, как один выходной фактор, RpaA, может координировать гены, пиковая активность которых приходится на совершенно разное время суток. Авторы сосредоточились на двух типичных областях управления ДНК (промоторах): kaiBC, который наиболее активен к закату, и purF, пик которого приходится на рассвет. В контролируемых реакциях с очищенной РНК‑полимеразой цианобактерий и RpaA они показали, что фосфорилированный RpaA усиливает транскрипцию с промотора kaiBC и одновременно ослабляет транскрипцию с промотора purF. Подробные эксперименты по картированию подошвы (footprinting) точно определили места связывания RpaA на каждой последовательности ДНК, показав, что его позиция относительно стандартных элементов промотора определяет, действует ли он как ускоритель или тормоз.
Наблюдая переключатель часов в атомных деталях
Чтобы понять это двойственное поведение на молекулярном уровне, команда использовала крио‑электронную микроскопию высокого разрешения, чтобы зафиксировать структуру RpaA, связанного с промотором kaiBC вместе с РНК‑полимеразой. Снимки показывают, как RpaA охватывает ДНК как асимметричная пара и контактирует с двумя ключевыми частями фермента: хвостом альфа‑субъединицы и участком сигма‑фактора, который обычно распознает промоторные последовательности. Эти контакты изгибают ДНК и помогают правильно позиционировать РНК‑полимеразу у слегка смещенной точки старта транскрипции. Тщательно подобранные мутации, ослабляющие любой из этих контактных пунктов, снижают или уничтожают активацию kaiBC как in vitro, так и в живых клетках, подтверждая, что физическое привлечение РНК‑полимеразы лежит в основе включения генов в фазе заката.
Создание гена, управляемого часами, с нуля
Поскольку нативная РНК‑полимераза цианобактерий сложна и трудно сохраняет активность в течение нескольких дней, исследователи обратились к гораздо более простой полимеразе бактериофага T7, широко используемой в лабораториях. RpaA не способен рекрутировать этот несвязанный фермент, но он по‑прежнему может блокировать его, занимая участок ДНК. Команда спроектировала синтетический шаблон ДНК, где промотор T7 запускает флуоресцентный РНК‑репортер «Broccoli», а сайт связывания RpaA размещен ниже по течению. Когда они совместили этот шаблон с часами KaiA–KaiB–KaiC, киназой/фосфатазой CikA, RpaA и полимеразой T7 в одном оптимизированном буфере, были наблюдаемы колебания скорости транскрипции с периодом около 24 часов. Ритм можно было сбросить изменением соотношения ATP к ADP, и он сохранял почти тот же период в широком диапазоне температур — классические признаки истинных циркадных часов.
От простых часов к инженерному учету времени
Исследование показывает, что всего шесть белков достаточно, чтобы связать химический камертон с ритмичным считыванием генов: три белка Kai, CikA, RpaA и РНК‑полимераза. Изменяя место нахождения RpaA на ДНК, тот же молекула может делать так, чтобы одни гены пиковали к закату, а другие — к рассвету, что помогает объяснить сложные волны генетической активности, наблюдаемые у цианобактерий. Поскольку дизайн на основе репрессии работает даже с чужеродной полимеразой, такой как T7, станет возможным трансплантировать этот минимальный модуль часов в другие микроорганизмы или клеточно‑свободные системы, позволяя ученым программировать включение и выключение генов по суточному ритму для исследований, промышленного производства или будущих терапевтических приложений.
Цитирование: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Ключевые слова: циркадные часы, цианобактерии, регуляция транскрипции, RpaA, синтетическая биология