Clear Sky Science · ru
Цереблон вызывает деградацию неосубстрата G3BP2 с помощью имитации молекулярной поверхности
Преобразование клеточной уборки в систему умной нацеленности
Современная медицина всё чаще пытается лечить болезни не просто блокируя вредные белки, а полностью избавляясь от них. В этой работе изучается хитрый способ перенастроить один из внутриклеточных «уборочных» механизмов так, чтобы при участии малой молекулы он узнал и уничтожил белок, связанный с раком и другими нарушениями. Исследование показывает неожиданный трюк: уборочный комплекс перестраивает часть своей поверхности, имитируя естественного партнёра белка, что позволяет ему прикрепиться и направить белок на утилизацию.
Клеточный сборщик мусора с скрытой гибкостью
Наши клетки постоянно помечают изношенные или нежелательные белки для разрушения с помощью системы, основанной на E3-лигазах — крупных белковых комплексов, которые решают, что следует утилизировать. Один из таких комплексов опирается на компонент под названием цереблон, выполняющий роль сенсора, распознающего конкретные признаки («дегроны») на других белках. Некоторые одобренные препараты уже используют цереблон в роли «молекулярного клея»: они связываются с цереблоном и создают новую посадочную поверхность, которая притягивает болезнетворные белки, после чего те помечаются для деградации. До сих пор большинство известных мишеней имели определённый структурный паттерн, из‑за чего казалось, что спектр белков, поддающихся такому удалению, ограничен.
Открытие новой мишени вне старых правил
В новом исследовании авторы просеяли коллекцию молекулярных клеев, ориентированных на цереблон, в клетках человека и обнаружили соединение MRT-5702. Эта малая молекула вызывала быструю потерю белка G3BP2, который участвует в управлении РНК и входит в состав стресс-гранул — образований, связанных с раком, сердечными проблемами и нейродегенеративными заболеваниями. Важно, что G3BP2 не содержит привычного дегронного мотива, который распознаёт цереблон. Последующие клеточные эксперименты, включая чувствительные световые методы для оценки близости белков, подтвердили, что MRT-5702 сближает цереблон и G3BP2 в трёхкомпонентный комплекс, приводящий к деградации G3BP2, при этом близкий по составу белок‑сиблинт G3BP1 остаётся нетронутым, если только у него не заменить ключевой домен.
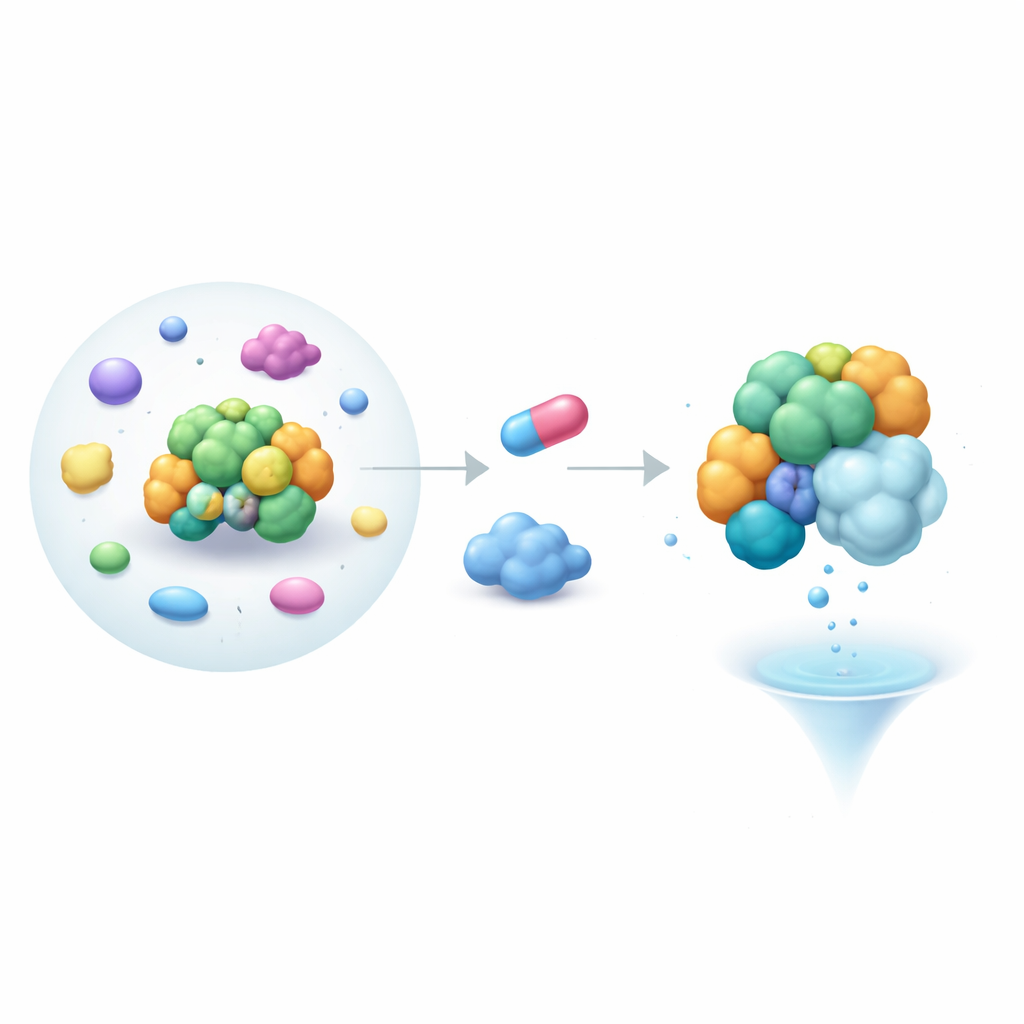
Имитация как стратегия связывания
Углубляясь, исследователи задали вопрос, как G3BP2 может связываться с цереблоном без стандартного мотива распознавания. Вместо того чтобы искать сходства между G3BP2 и известными мишенями цереблона, они перевернули задачу: не может ли цереблон напоминать одного из обычных партнёров G3BP2? Белки G3BP обычно взаимодействуют с другими молекулами через «горячую точку» в области, называемой NTF2‑подобным доменом, который обычно распознаёт короткие последовательные мотивы. Используя модель структуры естественного партнёра G3BP2 — USP10, команда вычислительно просканировала поверхность цереблона и нашла участок в менее изученной области, LON‑домене, который в форме и химии близко имитирует мотив связывания USP10. Замены всего нескольких ключевых аминокислот на этом участке или в «горячей точке» G3BP2 ослабляли трёхкомпонентный комплекс, что свидетельствует о том, что цереблон фактически выдаёт себя за USP10, чтобы прикрепиться к G3BP2.
Запечатление нового интерфейса в атомных деталях
Чтобы визуализировать это нетипичное взаимодействие, команда использовала крио‑электронную микроскопию высокого разрешения и решила структуру комплекса, содержащего цереблон, другой основной компонент лигазы, MRT-5702 и NTF2‑подобный домен G3BP2. Снимки показали, что гибкая петля в LON‑домене цереблона сгибается и изменяет форму, формируя почти половину контактной поверхности с G3BP2. Активная зеркальная форма MRT-5702 располагается в обычной карманной зоне связывания цереблона, но вместе с петлёй помогает создать широкую «площадку», которая удерживает одну половину димера G3BP2. Поразительно, что такая укладка почти не задействует каноническое место цереблона, ответственное за предыдущие клеевые мишени, показывая, что цереблон способен взаимодействовать с очень разными участками своей поверхности в зависимости от клея и вовлечённого белка. Одновременно нетронутая половина димера G3BP2 остаётся доступной для связывания с другими партнёрами, что даёт правдоподобный механизм «побочной» деградации белков, случайно присоединённых к комплексу.
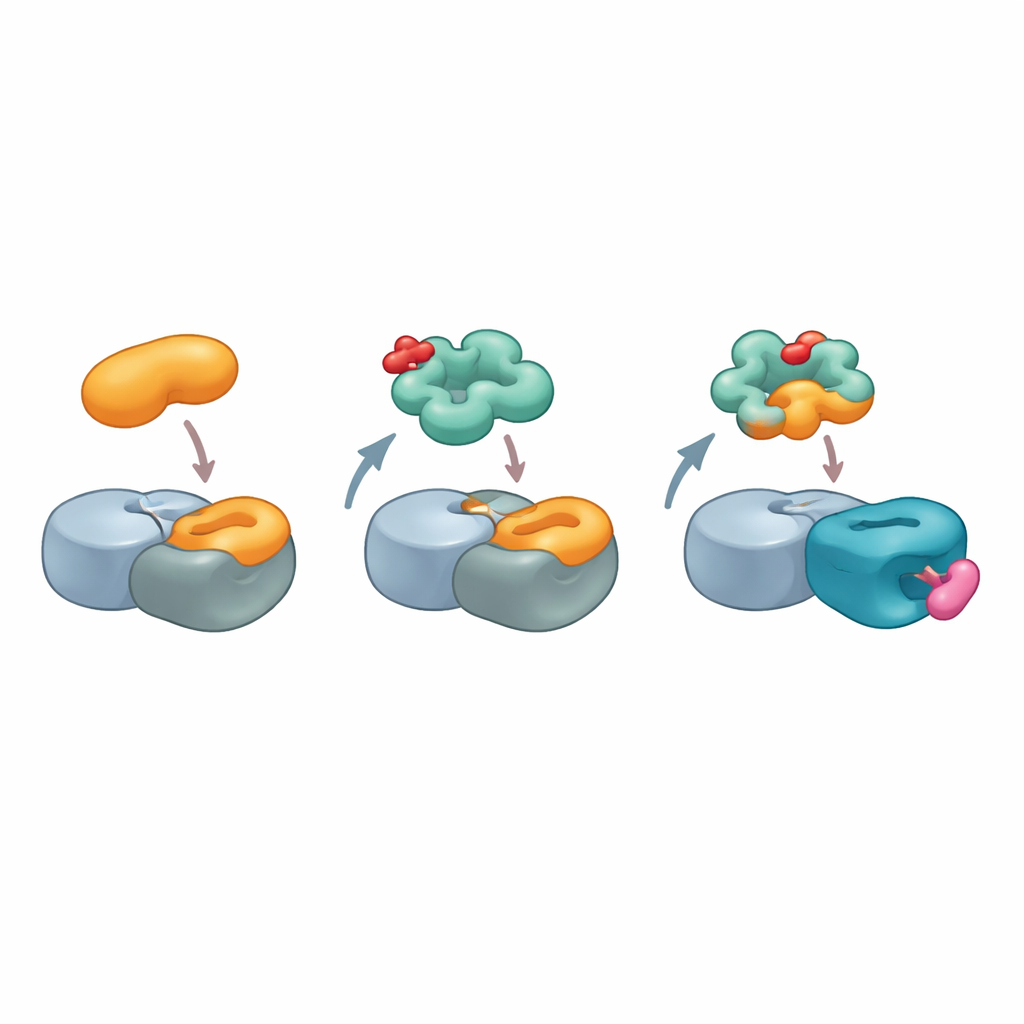
«Отпечатки клея» для будущей разработки лекарств
В совокупности результаты рисуют цереблон как гораздо более универсального сватовника, чем считалось ранее. Вместо того чтобы требовать от мишеней наличия одного типа дегрона, цереблон может, вооружённый подходящим молекулярным клеем, сформировать составную поверхность, имитирующую натуральные белок–белковые контакты в клетке. Авторы предлагают, что такие комбинированные поверхности белка и клея, которые они называют «glueprints» (отпечатки клея), можно картировать и проектировать для имитации существующих контактных «горячих точек» на многих белках, связанных с болезнями. Для непрофессионального читателя ключевая мысль такова: разработчикам лекарств, возможно, не потребуется открывать новые карманы связывания на проблемных белках; вместо этого они могут научить внутриклеточный «мусоропровод» распознавать эти белки, хитро копируя формы их обычных партнёров, что значительно расширяет перечень мишеней, которые можно безопасно и выборочно удалить.
Цитирование: Annunziato, S., Quan, C., Donckele, E.J. et al. Cereblon induces G3BP2 neosubstrate degradation using molecular surface mimicry. Nat Struct Mol Biol 33, 479–487 (2026). https://doi.org/10.1038/s41594-025-01738-8
Ключевые слова: молекулярные клеи-деградеры, цереблон, таргетированная деградация белков, G3BP2, взаимодействия белок–белок