Clear Sky Science · ru
Сигнальная передача TGFβ обеспечивает устойчивость микроглии к пространственно‑временно ограниченной дегенерации миелина
Почему проводку мозга нужно обслуживать
С возрастом «изоляция» вокруг наших нервных волокон — миелин — естественно изнашивается. Эта изоляция жизненно важна для быстрой и надежной коммуникации между мозгом и телом. В новом исследовании рассматривается, почему одно конкретное «шоссе» нервных волокон в спинном мозге, дорсальный столб, особенно уязвимо к этому износу, и как встроенный тормоз иммунной системы — сигнальный путь TGFβ — препятствует разрастанию повреждений. Понимание этого скрытого защитного механизма важно, так как его сбой может помочь объяснить некоторые расстройства спинного мозга и повлиять на подходы к лечению заболеваний мозга и рака у пожилых пациентов.
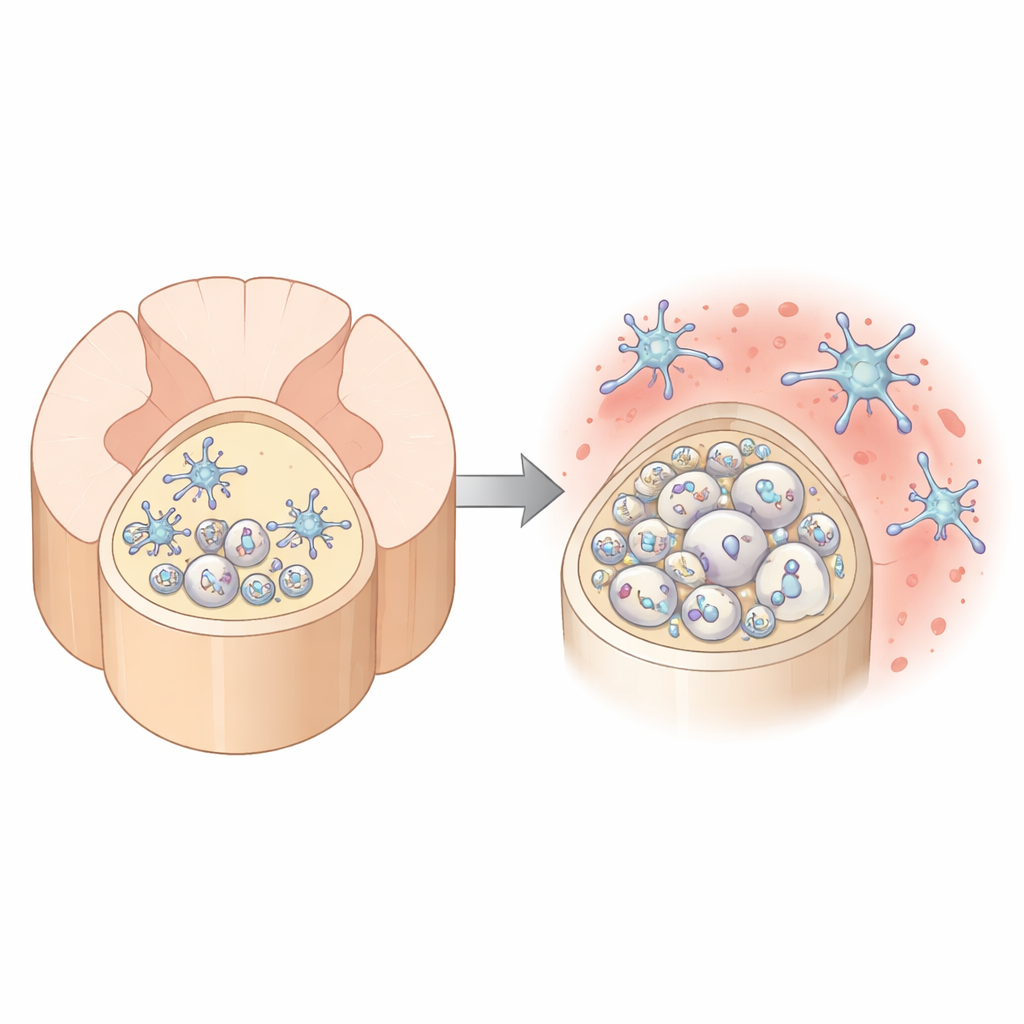
Где старение ударяет по «супершоссе» спинного мозга сильнее всего
Авторы сначала сравнили два основных пути белого вещества в спинном мозге мыши: дорсальный столб сзади и вентральный столб спереди. С помощью высокоразрешающей электронной микроскопии они обнаружили, что с возрастом миелин в дорсальном столбе становится все более искажённым. Обычно плотные обёртки вокруг волокон ослабляются, выпячиваются или отстают, оставляя увеличенные пространства между волокном и изоляцией и увеличивая число случаев явного распада миелина. Для контраста, вентральный столб остаётся относительно стабильным. В дорсальном регионе также сосредоточено гораздо больше, но тоньше́ных аксонов, что создаёт особенно большую нагрузку на клетки, строящие и поддерживающие миелин.
Иммунные сторожа под растущим давлением
Вокруг этих волокон находятся микроглия — резидентные иммунные клетки мозга и спинного мозга. Они постоянно патрулируют ткани, удаляют мусор и тонко настраивают связи. По мере дегенерации миелина в дорсальном столбе с возрастом микроглия начинает выглядеть и вести себя иначе: они повышают экспрессию генов, связанных с иммунной активацией, накапливают внутри маслянистые капли и проявляют признаки того, что поглотили больше повреждённого миелина. В то же время тканевая среда в дорсальном столбе становится сильно обогащённой TGFβ1 — сигнальным молекулой, известной своей ролью в сдерживании микроглии в состоянии, защищающем гомеостаз. Сами микроглиальные клетки являются основным источником этого TGFβ1, что свидетельствует о попытке удержать себя под контролем даже по мере нарастания стрессовых сигналов.
Что происходит, когда срабатывает отказ предохранителя
Чтобы выяснить, насколько важен этот тормоз, исследователи генетически инактивировали передачу сигналов TGFβ специально в микроглии взрослых мышей: либо удаляя рецептор, с помощью которого клетки чувствуют TGFβ, либо предотвращая синтез TGFβ1. В обоих случаях результат оказался поразительно схожим и строго локализованным: микроглия в дорсальном столбе становилась чрезмерно многочисленной, сильно активированной и принимала «пенной» внешность, наполненную поглощённым миелином. В этом регионе миелин сдирался, аксоны демонстрировали признаки дегенерации, а у мышей развивались ухудшение движений и координации, особенно с возрастом. Другие области спинного мозга были значительно меньше затронуты, что выявляет зависимость, специфичную для региона.
Особый подтип микроглии и напряжённые производители миелина
Секвенирование одиночных ядер РНК позволило команде каталогизировать отдельные типы клеток по мере развития болезни. Они обнаружили отдельный подтип микроглии — названный чувствительной к TGFβ микроглией — который резко расширялся при удалении сигнальной передачи TGFβ. Эти клетки выражали высокие уровни генов, связанных с сильными воспалительными ответами, активным поеданием миелина и обработкой липидов, и были сосредоточены в дорсальном столбе. Одновременно популяция зрелых клеток, формирующих миелин — олигодендроцитов — сменилась: здоровые субтипы сократились, тогда как «ассоциированная с болезнью» группа олигодендроцитов увеличилась в поражённом дорсальном столбе, но не смогла восстановить функциональный миелин, оставив аксоны оголёнными, несмотря на видимые попытки ремонта.
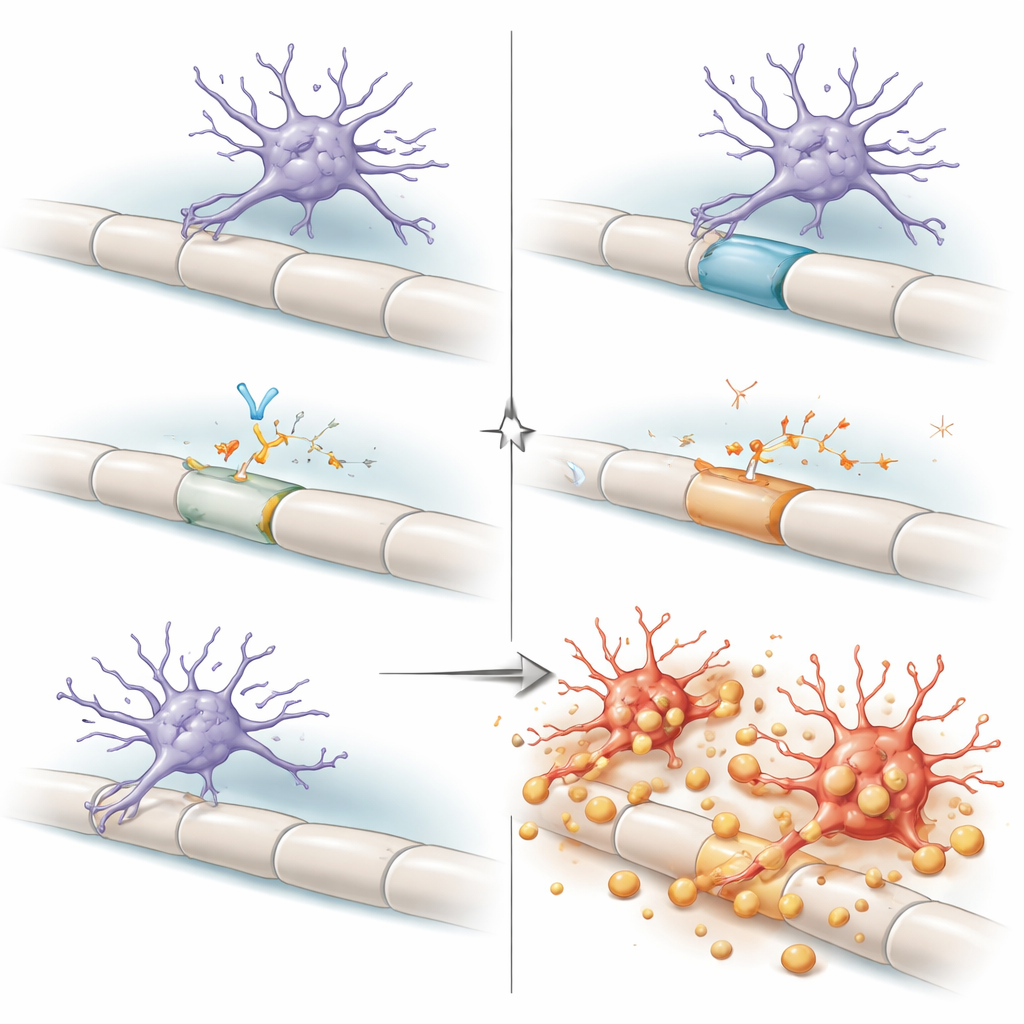
Последствия для старения и будущих терапий
В совокупности результаты рисуют дорсальный столб как район с высокой нагрузкой, где стареющий миелин и перегруженные вспомогательные клетки подталкивают микроглию к критической грани. При нормальных условиях аутокринная петля — когда микроглия производит и ощущает собственный TGFβ1 — удерживает её в «готовом, но устойчивом» состоянии, способном справляться с текущим мусором, не атакуя относительно сохранный миелин. Когда эта петля разрушается, микроглия переходит в неадаптивный режим, агрессивно снимая миелин и приводя к неврологическому упадку. Для неспециализированной аудитории ключевая мысль такова: иммунные клетки мозга не просто «хорошие» или «плохие»; их поведение сильно зависит от локальных требований проводки и от молекулярных тормозов, таких как TGFβ. Поскольку разрабатываются препараты, блокирующие TGFβ для лечения рака и некоторых заболеваний мозга, эта работа вносит важное предупреждение: нарушение этого пути, особенно у пожилых людей, может непреднамеренно повредить уязвимые участки спинного мозга, развязав микроглию на той самой изоляции, которая необходима нашим нервам для нормальной работы.
Цитирование: Zhu, K., Liu, Y., Min, JH. et al. TGFβ signaling mediates microglial resilience to spatiotemporally restricted myelin degeneration. Nat Neurosci 29, 617–631 (2026). https://doi.org/10.1038/s41593-025-02161-4
Ключевые слова: микроглия, старение миелина, дорсальный столб спинного мозга, сигналы TGF бета, нейровоспаление