Clear Sky Science · ru
Многомодальный антигенный уход от GPRC5D-направленных связывающих Т‑клетки препаратов при множественной миеломе
Когда рак перехитрит точную иммунотерапию
Мощные новые препараты на основе иммунной системы меняют подход к лечению множественной миеломы — гемоболезни, которая для большинства пациентов по‑прежнему остается неизлечимой. Эти терапии перенаправляют собственные Т‑клетки организма на уничтожение опухолевых клеток, помеченных определёнными «флагами» на поверхности. Одним из перспективных флагов является молекула GPRC5D. Однако, как и при многих таргетных методах лечения, опухоли могут эволюционировать и ускользать от воздействия. В этом исследовании подробно раскрыто, как клетки миеломы изменяют или скрывают флаг GPRC5D, чтобы избежать действия высокоэффективных препаратов, привлекающих Т‑клетки.
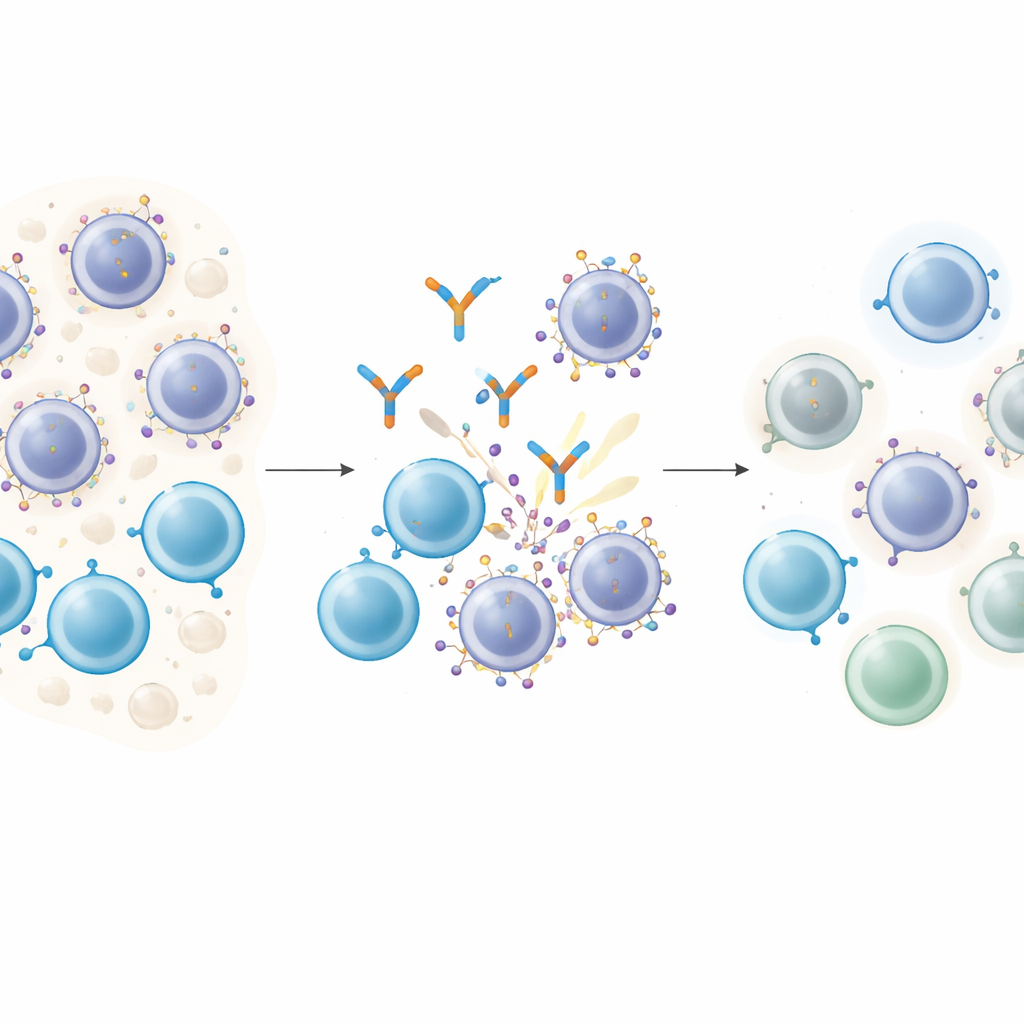
Как «умные» препараты цепляются за раковые клетки
Антитела‑связыватели Т‑клеток действуют как молекулярные сваховники: один конец захватывает Т‑клетку, другой прикрепляется к мишени на раковой клетке, сближая их, чтобы Т‑клетка могла убить цель. При множественной миеломе GPRC5D привлекателен как мишень, потому что он обилен на злокачественных плазматических клетках и редок на большинстве нормальных тканей. Пациенты, получавшие препарат, направленный на GPRC5D, под названием талкетамаб, зачастую испытывают глубокие ремиссии. Тем не менее почти все в конце концов рецидивируют, что поднимает важный вопрос: не изменяют ли раковые клетки ту самую мишень, от которой зависят эти препараты?
Отслеживание эволюции опухоли в реальном времени
Исследователи наблюдали за 21 пациентом с труднолечимой миеломой, получавшим талкетамаб. У некоторых пациентов брали образцы костного мозга до начала лечения и снова при рецидиве, затем использовали многослойный анализ ДНК, РНК и хроматина для изучения опухолевых клеток. Этот сверхдетализированный взгляд показал, что примерно у двух третей пациентов с рецидивом опухоль модифицировала GPRC5D такими способами, которые ослабляют или блокируют действие препарата. Поразительно, что несколько различных резистентных субклонов — генетически отличающихся ответвлений опухоли — часто сосуществовали в одном пациенте, показывая, что эволюция в направлении ухода может идти по нескольким путям одновременно.
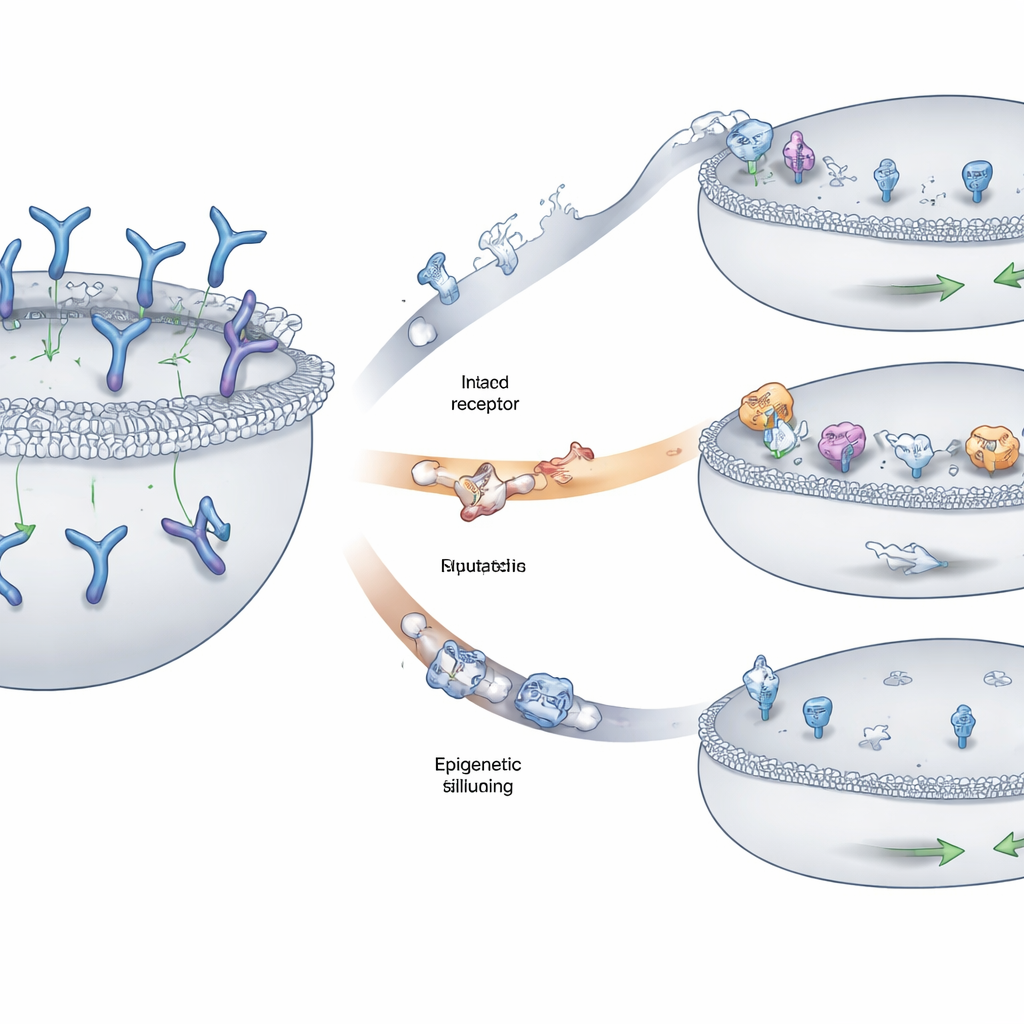
Три основных способа, которыми опухоли скрывают мишень
Команда выявила три повторяющиеся закономерности уклонения миеломных клеток от распознавания. У некоторых пациентов фрагменты хромосомы, несущей ген GPRC5D, были удалены в обеих аллелях, полностью стирая флаг с поверхности клетки. У других мелкие изменения — замены одной буквы в ДНК или крошечные вставки и делеции — искажали ключевые участки белка GPRC5D. Многие из этих изменений нарушали участки белка, необходимые для правильного транспорта внутрь клетки к наружной мембране, что приводило к тому, что GPRC5D застревал во внутренних компартментах вместо того, чтобы отображаться там, где препарат мог бы его увидеть. Третий путь включал эпигенетическое выключение: окружающая ген GPRC5D ДНК становилась плотно упакованной и химически маркированной так, что ген почти не считывался, хотя его последовательность в основном оставалась неповреждённой. Клетки опухоли, использовавшие эту стратегию, вырабатывали очень мало или совсем не вырабатывали GPRC5D.
Когда флаг есть, но замок больше не подходит
Не все пути ухода удаляли GPRC5D с поверхности клетки. В некоторых случаях белок выглядел нормальным в стандартных лабораторных тестах, но больше не подходил препарату как ключ к замку. Исследователи воссоздали конкретные мутации, обнаруженные у пациентов, в лабораторных клеточных линиях и проверили, насколько разные антитела, нацеленные на GPRC5D, могут связываться и убивать эти клетки. Одна мутация тонко изменила точную область, где талкетамаб захватывает рецептор, резко снижая способность препарата связываться и вызывать гибель клетки, хотя рецептор по‑прежнему был видим при рутинном окрашивании. Интригующе, другой препарат, направленный на GPRC5D, который фиксируется за рецептор в двух точках, оставался эффективным против нескольких таких мутантов, что подчёркивает, как дизайн препарата — например мультивалентное или многоэпитопное связывание — может влиять на выживаемость резистентных клонов.
Кроме мишени: другие ограничения для иммунной атаки
Хотя у большинства пациентов с рецидивом наблюдалась та или иная форма потери или изменения GPRC5D, у меньшинства пациентов рецидив наступал без очевидных изменений самой мишени. В таких случаях проблема, по‑видимому, заключалась в Т‑клетках: они были менее жизнеспособны и хуже убивали раковые клетки в лабораторных тестах, что указывает на то, что длительное непрерывное воздействие терапии‑привлекателя может истощать иммунную систему. Исследование также показало, что определённый генетический подтип миеломы (с хромосомной перестановкой t(11;14)) естественным образом поддерживает ген GPRC5D в более «закрытом» состоянии хроматина с более низкой исходной экспрессией. Это наводит на мысль, что некоторые пациенты могут быть предрасположены к худшим ответам, потому что их опухоли изначально имеют сниженные уровни мишени.
Что это значит для пациентов и будущих методов лечения
Для пациентов и врачей эта работа объясняет, почему даже высокоактивные препараты, нацеленные на GPRC5D, пока не являются лечением: клетки миеломы могут удалять, перестраивать, неправильно маршрутизировать или выключать тот самый флаг, от которого зависят эти препараты, и они часто делают это несколькими путями одновременно. Полученные данные указывают на то, что мониторинг опухолевой ДНК, а не только измерение уровня белка, будет важен для выявления возникающих мутаций ухода, которые стандартные лабораторные тесты могут пропускать. Они также намекают на стратегии следующего поколения — например препараты, которые связывают GPRC5D более прочно в нескольких точках, комбинации, которые поражают более одной мишени одновременно, или агенты, «открывающие» замолчанные гены — чтобы опережать эволюцию опухоли. По сути, это исследование картирует маршруты ухода, которые использует миелома, чтобы будущие терапии могли быть спроектированы с учётом их блокировки и продлевали эффективность средств, основанных на Т‑клетках.
Цитирование: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Ключевые слова: множественная миелома, связывающие Т‑клетки, GPRC5D, антигенный уход, раковая иммунотерапия