Clear Sky Science · ru
Линавонкибарт и пембролизумаб при солидных опухолях с устойчивостью к ингибиторам иммунных контрольных точек: фаза 1
Почему упорные формы рака важны для всех нас
Лекарства-иммунотерапии, которые «снимают тормоза» с иммунной системы, изменили подход к лечению многих видов рака, но большинство пациентов либо изначально не получают от них пользы, либо со временем вновь наблюдают рост опухолей. В этом исследовании проверяется новый антительный препарат линавонкибарт, разработанный для нейтрализации мощного щита, которым опухоли прикрываются от атаки иммунитета, и сочетается он с уже существующей иммунотерапией — пембролизумабом. Результаты дают раннее представление о том, что даже у пациентов, чьи опухоли уже перестали реагировать на препараты, блокирующие контрольные точки, возможно восстановить иммунный контроль при приемлемом уровне побочных эффектов.
Скрытый щит вокруг опухолей
Многие современные иммунотерапевтические препараты действуют, блокируя так называемые молекулы контрольных точек, такие как PD-1, которые в норме сдерживают Т-клетки. Когда эти «тормоза» снимаются, иммунные клетки могут сильнее атаковать рак. Но опухоли часто приспосабливаются, создавая в своем окружении враждебную среду, которая не пускает цитотоксические Т-клетки или ослабляет их функции, если они проникают внутрь. Ключевым архитектором этой защитной «пузыри» является сигнальный белок TGFβ1, который вырабатывают как раковые клетки, так и соседние поддерживающие клетки. Ранние попытки блокировать всю семью TGFβ показали обнадеживающие результаты, но столкнулись с серьезными проблемами с сердцем и кровотечениями, поскольку другие члены семейства важны для нормальных тканей. Линавонкибарт был создан так, чтобы решить эту задачу выборочно: он нейтрализует только латентную, неактивную форму TGFβ1 до её активации, оставляя близкие молекулы, необходимые организму, нетронутыми.
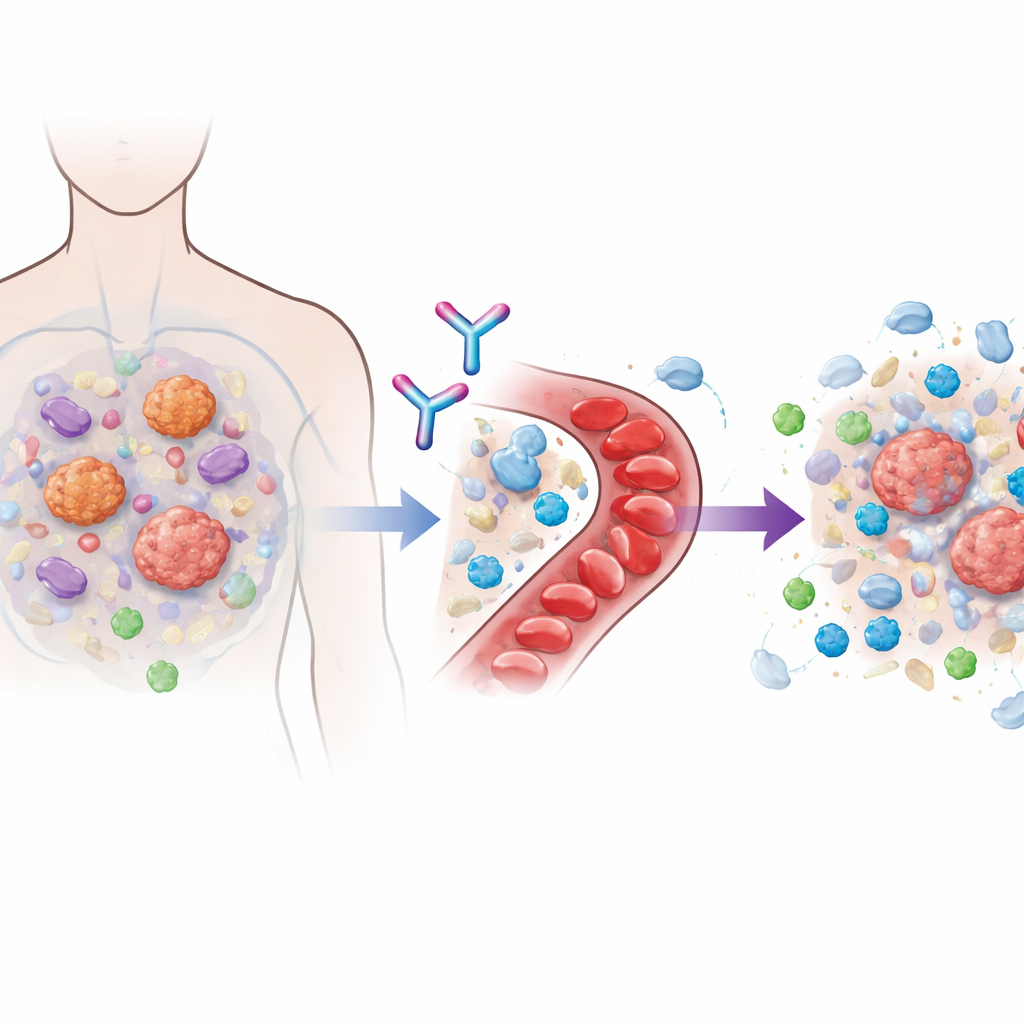
Проектирование осторожного первого в человеке исследования
Исследование DRAGON было многоцентровым испытанием фазы 1, проведенным в 22 больницах в США и Южной Корее. В нем участвовали 112 взрослых с распространенными солидными опухолями, у всех которых были ограниченные варианты лечения. В первой части исследования линавонкибарт вводили отдельно в постепенно увеличивающихся дозах небольшим группам пациентов либо в сочетании с их предыдущим препаратом на основе PD‑1. Такой поэтапный подход использовали для оценки безопасности, фармакокинетики — как препарат распределяется и сохраняется в крови — и для выбора дозы для более широкого тестирования. Во второй части 78 пациентов с опухолями, уже резистентными к по крайней мере одному курсу иммунотерапии PD‑1, получили фиксированную дозу линавонкибарта совместно с пембролизумабом. У этих пациентов были труднолечимые опухоли, включая почечно-клеточный рак, меланому, рак головы и шеи, уротелиальный (мочевой пузырь) рак и рак легких, и большинство из них ранее получало несколько линий терапии.
Прежде всего — безопасность: что случилось с пациентами
Главной целью этого раннего этапа было оценить безопасность, и линавонкибарт на этом фронте показал обнадеживающие результаты. По всем уровням доз максимальная переносимая доза не была достигнута, не выявлено дозовых ограничивающих или летальных побочных эффектов, связанных с препаратом. При сочетании линавонкибарта с пембролизумабом на дозе фазы 2 примерно у трех четвертей пациентов возникали побочные явления, связанные с лечением, что сопоставимо с тем, что часто наблюдается при иммунотерапии в целом. Высыпания и зуд были наиболее частыми дополнительными проблемами, у небольшого числа пациентов развивались более серьезные воспаления кожи или легких. Важно, что опасная гиперактивация иммунитета — синдром высвобождения цитокинов, который иногда возникает при некоторых антителах — не наблюдалась, и общий профиль безопасности в основном напоминал таковой у пембролизумаба в монорежиме.
Признаки того, что иммунную систему можно разбудить вновь
Хотя это не было крупным подтверждающим исследованием эффективности, несколько признаков указывали, что подавление TGFβ1 может помочь возобновить ответы на блокаду PD‑1. На стадии расширения комбинированная терапия линавонкибарт–пембролизумаб уменьшала измеримые опухоли у заметной доли пациентов, ранее переставших получать пользу от препаратов PD‑1. Подтвержденные показатели ответа составили 20 % при почечно-клеточном раке, 18,2 % при меланоме и чуть более 9 % при раке головы и шеи и уротелиальном раке; у одного пациента с раком почки наблюдалось полное исчезновение визуально определяемой болезни. Многие из этих ответов длились несколько месяцев, и ответившие пациенты в целом дольше получали комбинированную терапию по сравнению с предыдущим лечением PD‑1. Биопсии до и после лечения дали биологическое объяснение: опухоли демонстрировали более выраженную инфильтрацию CD8 «киллерных» Т-клеток, повышенные уровни активированных Т-клеток, меньше супрессивных регуляторных Т-клеток и миелоидных клеток, а также общее смещение в сторону более воспаленной, подготовленной к атаке микросреды.
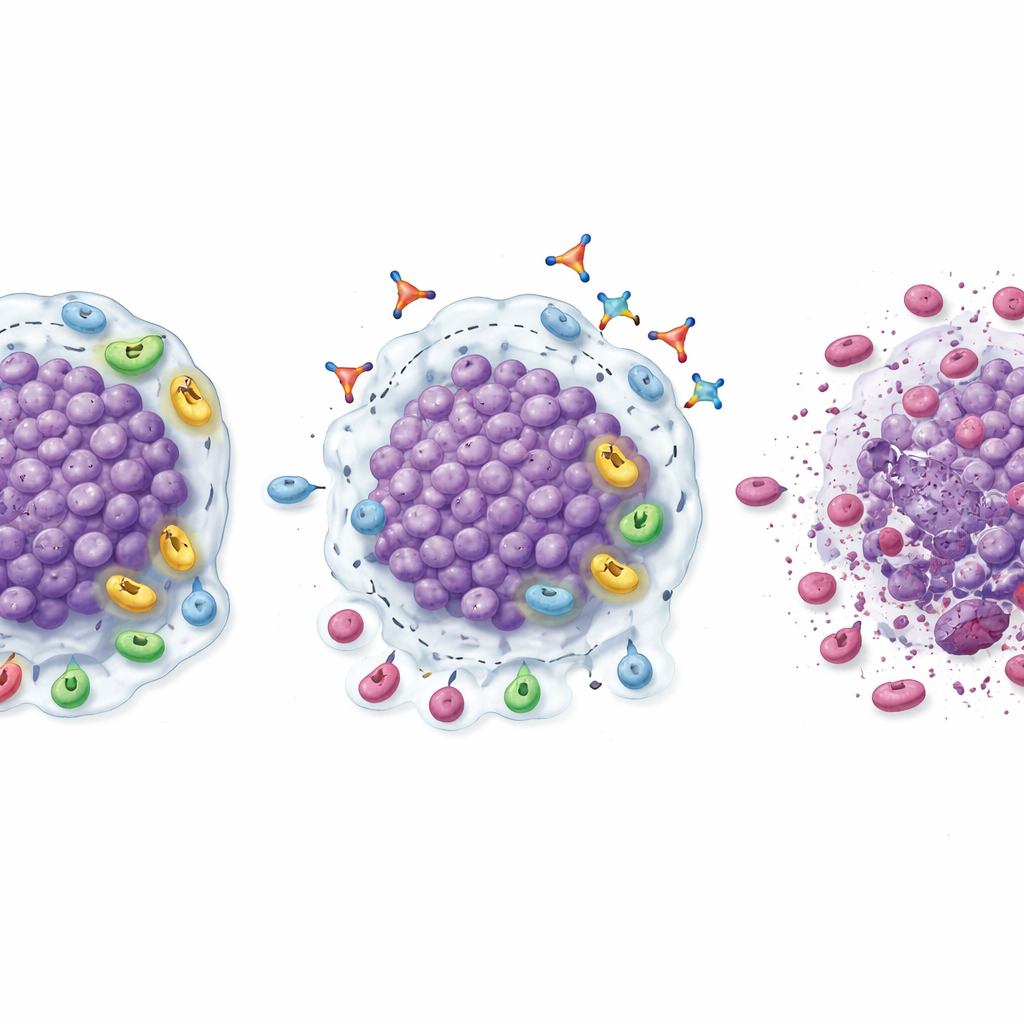
Как найти тех, кто может получить наибольшую пользу
Исследователи также изучали, какие пациенты особенно вероятно отреагируют. При почечно‑клеточном раке опухоли, которые изначально содержали много CD8‑Т-клеток, но одновременно были богаты регуляторными Т-клетками и экспрессировали высокие уровни TGFβ1, с большей вероятностью уменьшались при комбинированной терапии. У таких пациентов показатели ответа и выживания без прогрессирования были существенно выше, чем в более широкой группе больных с раком почки. Этот паттерн указывает на «сладкое место»: опухоли, в которых присутствует достаточное количество иммунных «солдат», но которые сдерживаются подавлением, опосредованным TGFβ1, могут быть идеальными кандидатами для линавонкибарта в сочетании с блокадой PD‑1. Если это подтвердят более крупные исследования, простые тканевые тесты на эти маркеры могут помочь врачам выбрать пациентов с наибольшей вероятностью пользы.
Что это означает в дальнейшем
Для людей с продвинутыми опухолями, уже резистентными к иммунотерапии, перспектива вновь активировать собственный иммунитет без значительного увеличения токсичности выглядит многообещающе. Это первое в человеке исследование дает ранние доказательства того, что селективное отключение щита TGFβ1 с помощью линавонкибарта можно выполнить безопасно и что это может восстановить значимый контроль над опухолью в сочетании с ингибитором PD‑1, особенно при некоторых формах рака почки. Поскольку исследование было небольшим и нерандомизированным, требуются более крупные фазы 2 для подтверждения. Если будущие работы подтвердят эти результаты, подход может расширить круг пациентов, которым доступна иммунотерапия, превращая некоторые ныне упорные опухоли в вновь уязвимые для собственных защит организма.
Цитирование: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
Ключевые слова: иммунотерапия рака, ингибирование TGFβ1, устойчивость к ингибиторам контрольных точек, почечно-клеточный рак, опухолевая микросреда