Clear Sky Science · ru
Интерпретируемая панорама воспаления циркулирующих иммунных клеток
Почему воспаление в крови важно для вас
Воспаление лежит в основе многих заболеваний — от артрита и астмы до COVID-19 и рака. Тем не менее врачам по-прежнему трудно интерпретировать воспалительные сигналы организма так, чтобы ясно понять, что именно нарушено и какое лечение сработает лучше всего. В этом исследовании создана большая «карта» иммунных клеток, циркулирующих в крови, и показано, как эти клетки могут выступать живыми, легко доступными биомаркерами для классификации широкого круга воспалительных заболеваний.
Создание гигантской карты иммунных клеток
Чтобы проложить этот ландшафт, исследователи проанализировали более 6,5 миллиона иммунных клеток, взятых из крови 1 047 человек. Волонтеры представляли 19 состояний, включая аутоиммунные заболевания, такие как волчанка и ревматоидный артрит, хронические заболевания легких (астма и ХОБЛ), инфекции (COVID-19 и ВИЧ), несколько видов рака, а также здоровых доноров. С помощью секвенирования РНК по одной клетке они измеряли, какие гены активны в каждой отдельной клетке, затем применяли продвинутые статистические методы для коррекции технических различий между исследованиями и группировали клетки в 64 различных состояния иммунных клеток. Этот «Атлас воспаления» включает как хорошо знакомых участников — например, Т-клетки, В-клетки и моноциты — так и более специализированные подтипы, которые меняются в зависимости от болезни.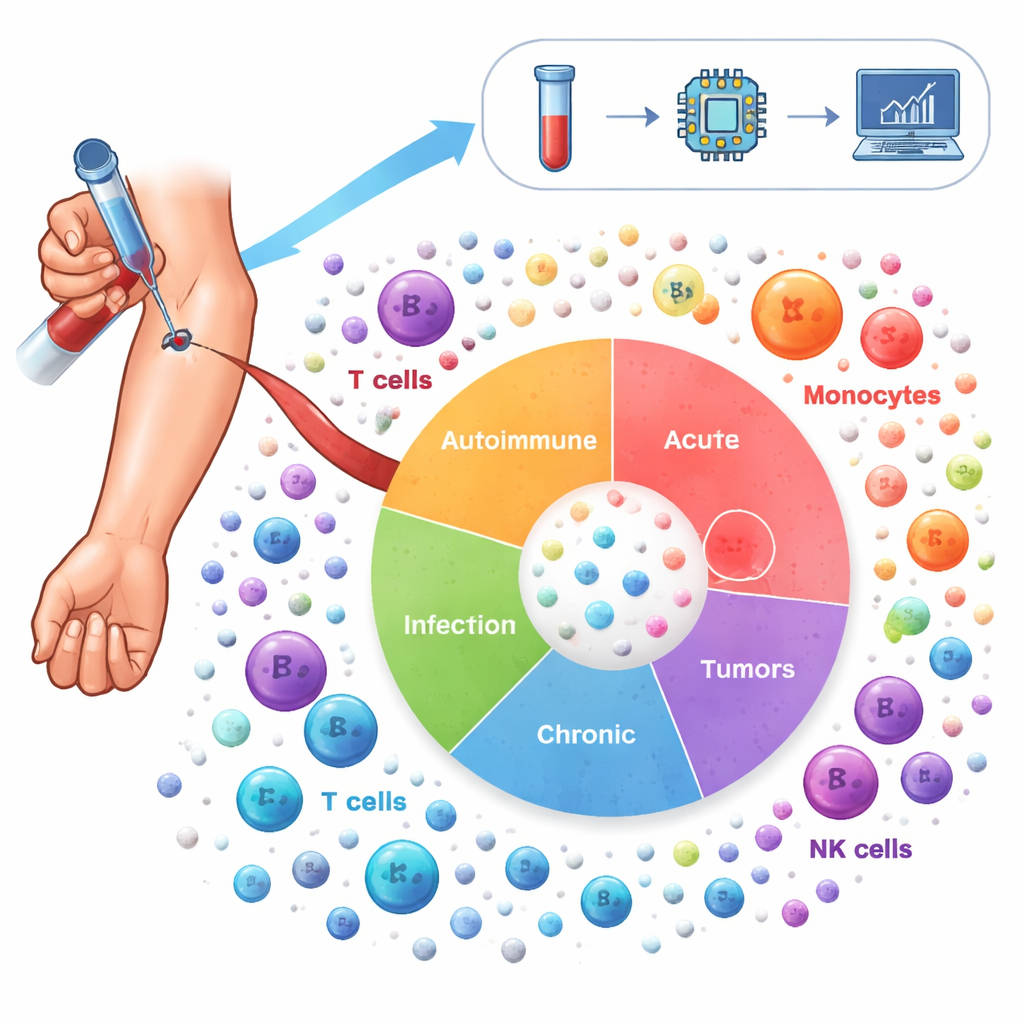
Чтение воспалительных сигнатур организма
Далее команда сосредоточилась на генах, контролирующих активацию иммунных клеток, их перемещение по организму, презентацию антигенов и отклик на сигнальные молекулы, такие как интерфероны и фактор некроза опухоли. Они сгруппировали эти гены в 21 биологическую «сигнатуру» и уточнили их для каждого основного типа клеток. Сравнивая пациентов со здоровыми донорами, исследователи могли видеть, какие сигнатуры усиливаются или подавляются при разных заболеваниях. Например, многие иммунно-опосредованные воспалительные заболевания демонстрировали повышенную активность молекул адгезии и механизмов презентации антигенов, тогда как ответы, индуцированные интерфероном, были снижены в большинстве типов клеток, но повышены в определенных CD8 Т-клетках. Вирусные инфекции, такие как грипп и COVID-19, усиливали интерферон-индуцированные программы, тогда как хронические инфекции, такие как ВИЧ и вирусный гепатит B, их ослабляли.
Углубление в ключевые гены и управляющие переключатели
Поскольку широкие сигнатуры по-прежнему скрывают важные подробности, исследователи углубились до отдельных генов и их регуляторов. В ненивных CD8 Т-клетках они обнаружили, что два гена, FGFBP2 и GZMB, особенно активны в специфических субтипах эффекторной памяти, особенно при язвенном колите. Эти гены связывают с повреждением эпителиальных поверхностей, и их сильный сигнал в крови предполагает, что эти агрессивные клетки уже находятся в состоянии подготовки до проникновения в ткани. Отдельный анализ сетей регуляции генов выделил два транскрипционных фактора, STAT1 и SP1, как центральных контроллера интерферон-индуцированных программ. Их образцы активности различались между болезнями и типами клеток — например, противоположное поведение в моноцитах и CD8 Т-клетках при волчанке, а также изменения между фазами обострения и ремиссии — что указывает на то, как одни и те же пути в одном контексте могут быть защитными, а в другом — вредными.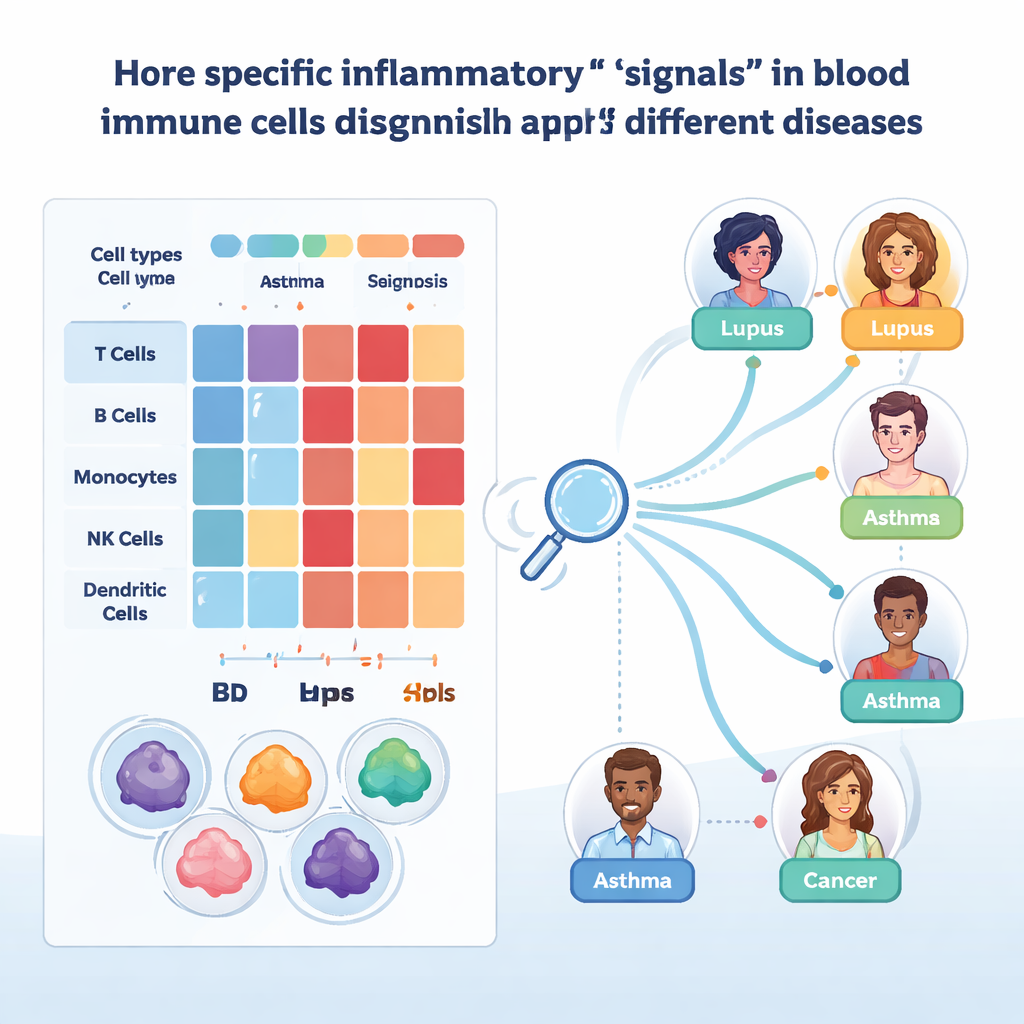
Обучение машин распознавать болезнь по клеткам крови
Чтобы превратить этот атлас в практический инструмент, команда применила интерпретируемое машинное обучение. Они обучали модели градиентного бустинга на решающих деревьях отдельно для каждого основного типа клеток, поручая алгоритмам маркировать отдельные клетки правильным диагнозом на основе их экспрессии генов. Эти модели достигали высокой точности при тестировании на отложенных образцах, особенно после коррекции технических различий. С помощью SHAP — метода, объясняющего, какие гены влияют на каждое решение — исследователи могли выделить кандидатные биомаркеры. Один пример — CYBA в моноцитах: его уровни помогали отличать кожные заболевания, такие как псориаз, от воспаления кишечника при болезни Крона и язвенном колите. Другой пример — IFITM1 в определенных Т-клетках и клетках врожденной лимфоидной линии, который разделял астму и ХОБЛ и указывал на различные модели хронической антивирусной защиты.
К компасу диагностики на основе крови
Наконец, авторы поинтересовались, можно ли классифицировать целиком пациентов — а не только отдельные клетки — по их профилям циркулирующих иммунных клеток. Они спроецировали данные каждой клетки в сжатое «встраиваемое» пространство, усреднили эти встраивания по типу клеток для каждого пациента и обучили классификаторы предсказывать заболевание. Когда новые пациенты были похожи на те, что в обучающей выборке, точность была отличной. Но когда образцы поступали из полностью независимых исследований с другими лабораторными методами, точность резко падала, что выявляет чувствительность таких инструментов к технической вариабельности. Более контролируемый «централизованный» набор данных, полученный в одном центре с одной химией секвенирования, восстановил большую часть эффективности, что указывает на необходимость стандартизированных протоколов или очень больших, разнообразных обучающих наборов.
Что это значит для будущей диагностики и лечения
Для неспециалиста главный вывод в том, что циркулирующие иммунные клетки несут богатый отпечаток того, как именно в вашем организме протекает воспаление. Читая эти отпечатки клетка за клеткой, работа показывает, что возможно различать многие заболевания, обнаруживать гены, которые могут определять конкретные симптомы, и начинать строить универсальные анализы крови для классификации воспалительных болезней. Исследование пока не является готовым клиническим тестом — технические различия между исследованиями все еще ограничивают надежность — но оно закладывает основу для будущих «жидкостных биопсий», которые могли бы помочь врачам быстрее ставить правильный диагноз и выбирать лечение, используя простой забор крови.
Цитирование: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Ключевые слова: воспаление, иммунные клетки, синговая РНК-секвенирование одной клетки, биомаркеры, машинное обучение