Clear Sky Science · ru
Репотрецитиниб при продвинутых солидных опухолях с NTRK‑фьюжнами: фаза 1/2
Новая надежда от таргетированной противораковой таблетки
Лечение рака всё чаще создают как точные инструменты, а не как грубые орудия. В этом исследовании рассматривают репотрецитиниб — таргетированный пероральный препарат для пациентов, чьи опухоли несут редкие генетические изменения, называемые NTRK‑фьюжнами. Хотя такие фьюжны встречаются менее чем в 1 из 100 солидных опухолей, они могут появляться в разных органах — от лёгких до щитовидной железы и мягких тканей — и часто дают выраженный ответ на специально разработанные лекарства. Проблема в том, что ранние препараты со временем перестают действовать. В этом исследовании ставится простой, но важный вопрос: сможет ли более продуманный препарат нового поколения удерживать контроль над раком дольше, даже после неудач других таргетных препаратов?
Редкий, но мощный онкогенный переключатель
Некоторые виды рака стимулируются фьюжнами в генах NTRK1, NTRK2 и NTRK3. Эти фьюжны действуют как заевшие включённые «переключатели» роста в опухолевых клетках. Препараты первого поколения, блокирующие получающиеся белки TRK, уже помогли многим пациентам, но со временем опухоль часто научается их обходить, приобретая новые мутации в той самой области, куда связывается лекарство. Репотрецитиниб был создан более компактным, чтобы он мог поместиться в эту область даже после таких изменений. Международное исследование TRIDENT‑1 протестировало препарат у взрослых с продвинутыми солидными опухолями, несущими NTRK‑фьюжны, включая тех, кто никогда ранее не получал ингибиторы TRK, а также пациентов, у которых опухоль уже стала резистентной к одному или двум ранним ингибиторам TRK.
Что сделал треал
В исследование было включено 144 пациента с NTRK‑фьюжн‑положительными солидными опухолями в центрах по всему миру; 120 из них составили основную группу для оценки эффективности. Опухоли охватывали как минимум 18 типов, чаще всего немелкоклеточный рак лёгкого, рак щитовидной железы, опухоли слюнных желёз и саркомы мягких тканей. У всех был локально распространённый или метастатический процесс, и многие уже прошли несколько линий терапии, включая химиотерапию, иммунотерапию или предыдущие ингибиторы TRK. Пациенты получали репотрецитиниб перорально ежедневно по схеме дозирования, отработанной в ранней фазе исследования. Исследователи отслеживали, у какого числа пациентов уменьшались опухоли, как долго сохранялись ответы, как долго пациенты жили без прогрессирования заболевания и как переносился препарат.
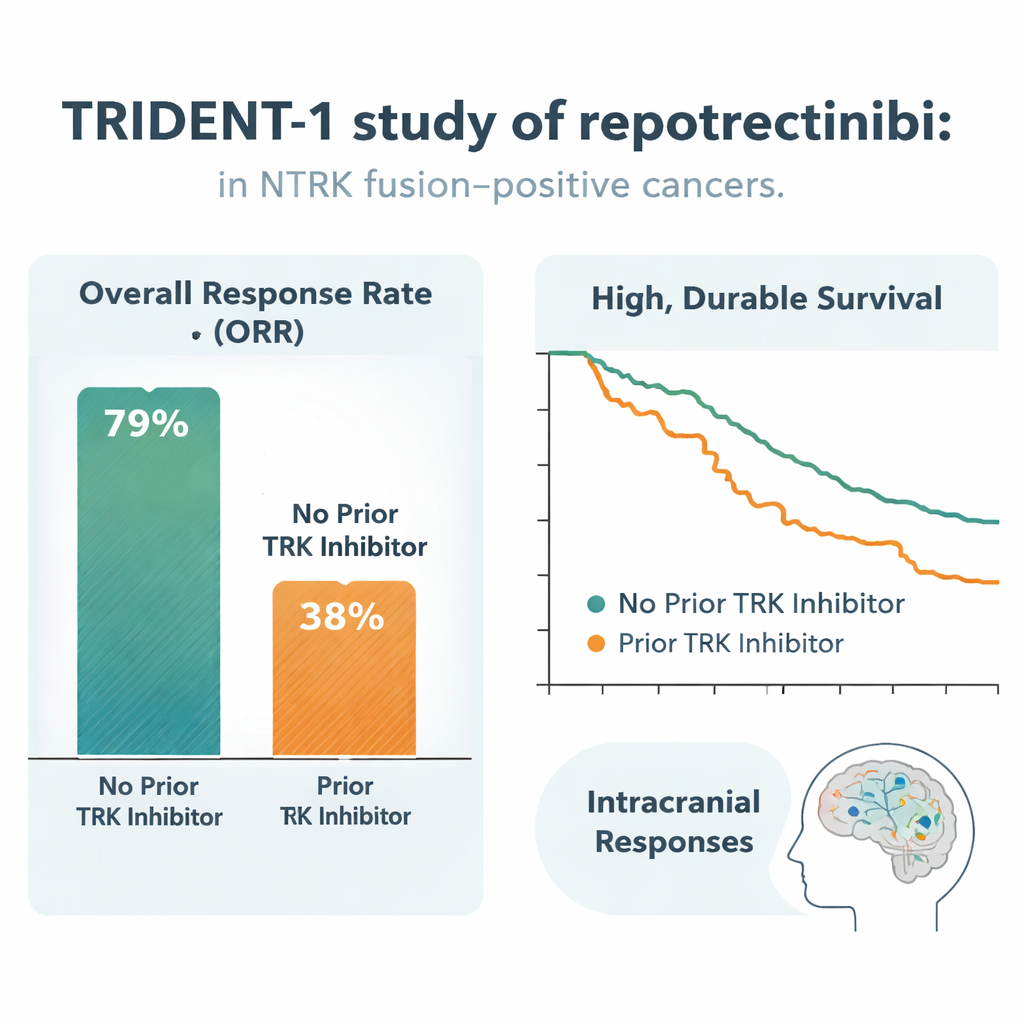
Сильные и длительные ответы
Среди 51 пациента, никогда ранее не получавшего ингибитор TRK, 59% продемонстрировали сокращение опухоли, достаточное для объективного ответа, а у 16% опухоли исчезли на снимках. Ответы, как правило, появлялись быстро — примерно в течение двух месяцев — и были впечатающе длительными: спустя два года примерно 85% отвечавших по‑прежнему получали пользу, и около 60% всей группы ещё не наблюдали прогрессирования. Даже в более ранее леченной группе из 69 пациентов, чьи опухоли уже преодолели другой TRK‑препарат, 48% ответили на репотрецитиниб, типичная продолжительность ответа составляла около 10 месяцев, и примерно четверть пациентов оставались без прогрессирования через год. Важно, что эффект наблюдался в разных типах опухолей и независимо от того, какой именно ген NTRK или партнёр фьюжна был вовлечён.
Достижение резистентных и церебральных поражений
Ключевой вызов для препаратов TRK — так называемые мутации на «солвент‑фронте», специфические изменения в кармане связывания лекарства, которые могут блокировать действие ранних препаратов. В этом исследовании почти у половины ранее леченных пациентов такие мутации были выявлены в начале. Даже в этой трудноизлечимой подгруппе 53% продемонстрировали значимое уменьшение опухоли при приёме репотрецитиниба, что подтверждает способность препарата преодолевать по крайней мере некоторые формы резистентности. Мозг, частая «прятка» для рака, был ещё одной важной областью внимания. Среди пациентов с измеримыми мозговыми метастазами на исходном уровне у двух из трёх из ранее нелеченой группы и у четырёх из шести среди ранее леченных наблюдалось уменьшение опухолей в мозге, часто на многие месяцы. У пациентов, начавших без поражений головного мозга, подавляющее большинство оставалось свободным от новых мозговых очагов в ходе наблюдения.
Побочные эффекты и значение для пациентов
У более чем 500 людей, получавших репотрецитиниб в этом и родственных исследованиях, наиболее частыми побочными эффектами были головокружение, изменение вкуса и покалывание — в большинстве случаев лёгкие или умеренные. Более серьёзные связанные с лечением явления, такие как анемия или повышение уровня мышечных ферментов, встречались реже, и лишь примерно 4% пациентов прекратили приём препарата из‑за побочных эффектов. Показатели качества жизни в целом оставались стабильными или улучшались у большинства участников в течение многих циклов терапии. В сумме результаты показывают, что репотрецитиниб может обеспечить длительный контроль над NTRK‑фьюжн‑положительными опухолями — в том числе над теми, которые уже выработали резистентность к предыдущим TRK‑препаратам, и над поражениями в мозге — при общей приемлемой переносимости. Для пациентов с этими редкими, но агрессивными опухолями исследование подтверждает репотрецитиниб как важную новую опцию в расширяющемся наборе средств прецизионной онкологии.
Цитирование: Besse, B., Lin, J.J., Bazhenova, L. et al. Repotrectinib in NTRK fusion–positive advanced solid tumors: a phase 1/2 trial. Nat Med 32, 682–689 (2026). https://doi.org/10.1038/s41591-025-04079-7
Ключевые слова: таргетная противораковая терапия, NTRK‑фьюжн, репотрецитиниб, резистентность к ингибиторам TRK, метастазы в мозг