Clear Sky Science · ru
Расширение опухолевых cDC1, индуцированное Flt3L, усиливает иммунотерапию за счёт программирования стволоподобных CD8+ T‑клеток в лимфоузлах
Помощь иммунной системе вспомнить, как бороться с раком
Почему у некоторых пациентов опухоли исчезают под действием современной иммунотерапии, тогда как у других эффекта почти нет? Это исследование заглядывает под капот иммунной системы, чтобы ответить на этот вопрос. Авторы показывают, что усиление определённой группы «часовых» в опухоли позволяет создать резерв длительно существующих стволоподобных киллерных T‑клеток в соседних лимфоузлах. Эти клетки, в свою очередь, делают стандартные препараты блокады контрольных точек, особенно анти‑CTLA‑4, более эффективными и длительными по действию.
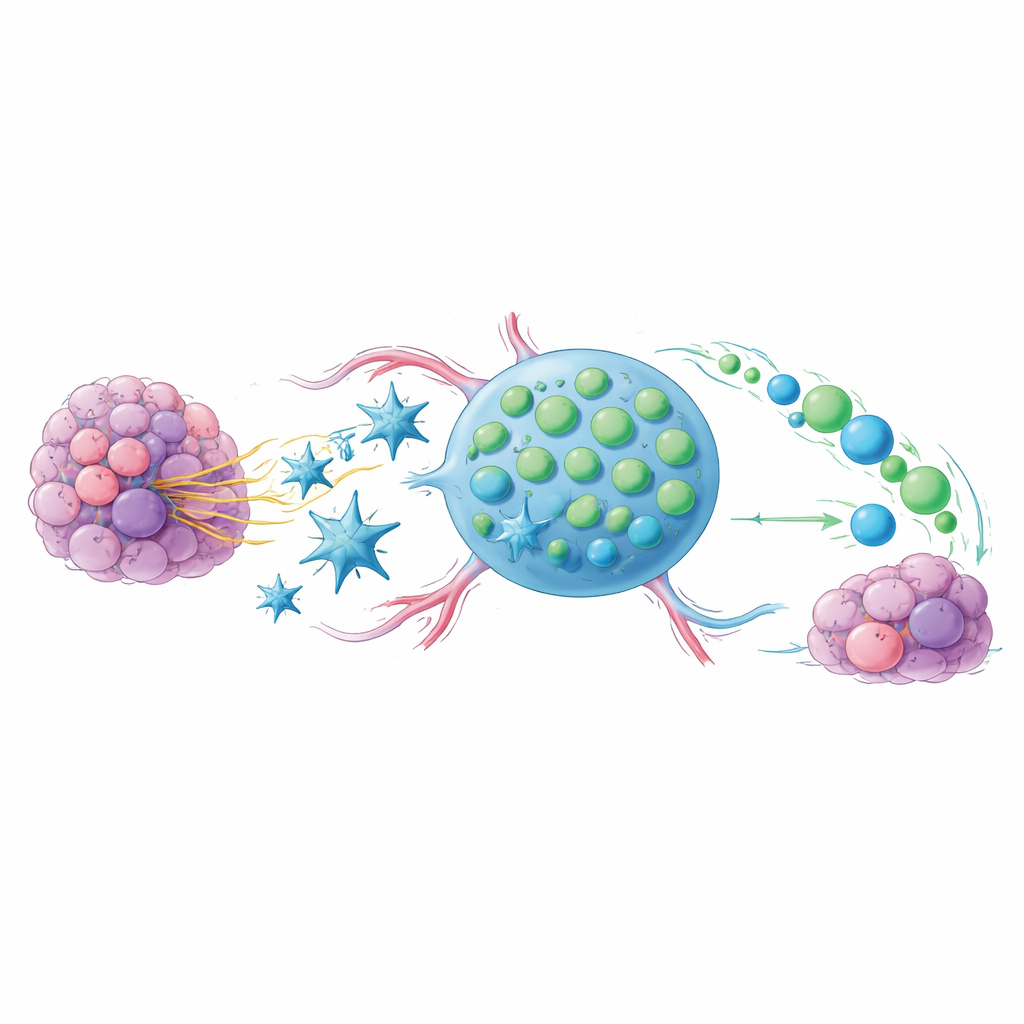
Проблема уставших клеток, сражающихся с опухолью
Препараты блокады контрольных точек, такие как анти‑PD‑1 и анти‑CTLA‑4, высвобождают иммунные клетки против рака, но эффективно работают лишь у части пациентов. Один из ключей — состояние CD8 T‑клеток, основных «убийц» инфицированных или злокачественных клеток. Когда эти Т‑клетки перегружают слишком долго, они переходят в изношенное, «истощённое» состояние и перестают эффективно делиться. Однако меньшая подкласс этих клеток сохраняет более юный, стволоподобный характер: они легко делятся, порождают новых бойцов и тесно связаны с благоприятными ответами у пациентов, получающих терапию блокадой контрольных точек. Главный вопрос этой работы — как склонить опухоль и её микроокружение в пользу этих стволоподобных клеток, а не их выгоревших собратьев.
Суперзарядка сторожевых клеток опухоли
Команда сосредоточилась на конвенциональных дендритных клетках типа 1 (cDC1) — редком, но мощном классе иммунных стражей, которые особенно хороши в представлении фрагментов опухоли T‑клеткам. Они использовали сигнальную молекулу роста, называемую лигандом Flt3 (Flt3L), чтобы расширить популяцию этих клеток внутри опухолей у мышей, либо заставляя раковые клетки секретировать его, либо вводя как препарат. Секвенирование одиночных клеток (single‑cell RNA‑seq) показало, что опухоли с богатым содержанием Flt3L содержали гораздо больше дендритных клеток и лимфоцитов и меньше опухолевых клеток. В пределах дендритного компартмента расширились три различные группы, включая одну высоко зрелую, подготовленную к миграции в лимфоузлы, где T‑клетки впервые проходят обучение. Одновременно CD8 T‑клетки внутри этих опухолей смещались от терминально истощённого профиля в сторону стволоподобного или памяти‑подобного состояния.
Создание резерва стволоподобных T‑клеток в лимфоузлах
Отслеживая опухолепецифические T‑клетки и применяя генетические методы, исследователи показали, что лечение Flt3L усиливает популяцию CD8 T‑клеток с маркерами поверхности, связанными со стволоподобным потенциалом и активным делением. Эти клетки зависели от XCR1‑положительных дендритных клеток и от CCR7‑направленной миграции дендритных клеток из опухоли в дренирующий лимфоузел. Когда дендритные клетки истощали или блокировали их миграцию, пул стволоподобных T‑клеток сокращался. Блокада выхода лимфоцитов из лимфоузлов давала схожий эффект, отрезая приток обновлённых T‑клеток в опухоль. Молекулярный профиль показал, что этот процесс опирается на фактор транскрипции Myb и предпочитает T‑клетки с относительно слабым распознаванием опухолевых мишеней — тип, который всё чаще признают важным для долгосрочного контроля рака.
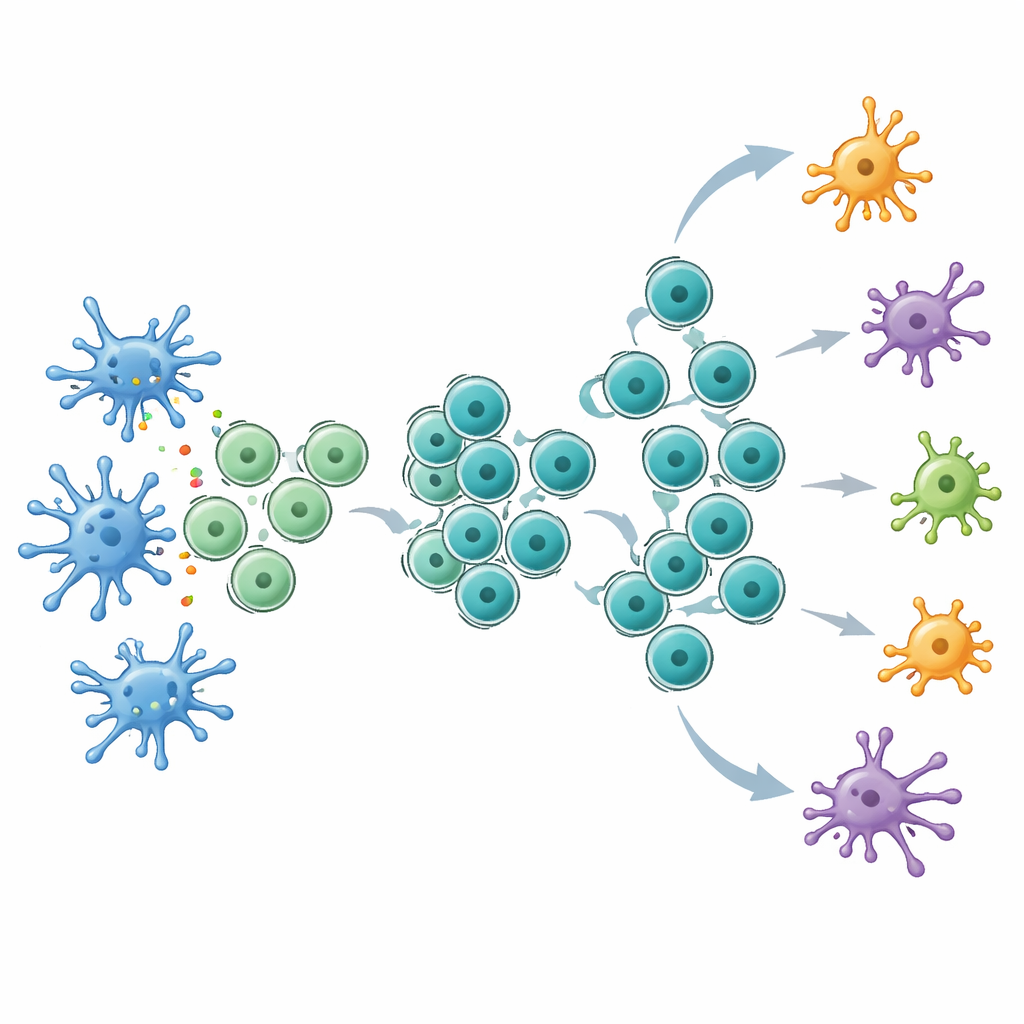
Повышение эффективности терапии блокадой контрольных точек
Вооружённые этим расширенным резервом стволоподобных T‑клеток, мыши гораздо лучше отвечали на блокаду контрольных точек, особенно на анти‑CTLA‑4. У животных, получавших Flt3L, опухоли уменьшались сильнее, выживаемость улучшалась, а в крови и лимфоузлах обнаруживалось больше опухолепецифических T‑клеток. Внутри опухолей Flt3L увеличивал количество стволоподобных CD8‑клеток, в то время как последующая блокада CTLA‑4, по‑видимому, стимулировала их созревание в мощные эффекторные клетки, производящие высокие уровни ключевых противоопухолевых молекул. Секвенирование T‑клеточных рецепторов показало, что комбинированная терапия расширяла набор клонов T‑клеток, включая многие субдоминантные, что указывает на более разнообразную атаку на опухоль. Детальный анализ одиночных клеток выявил уникальный кластер CD8 T‑клеток, отмеченный экспрессией рецептора к сигнальной молекуле IL‑21, который занимал промежуточное положение между стволоподобным и истощённым состояниями и разделял рецепторы с ранними и поздними популяциями. Блокада сигнального пути IL‑21 ослабляла преимущества сочетания Flt3L с анти‑CTLA‑4.
Что это означает для будущих методов лечения рака
Для неспециалиста главный вывод таков: успешная иммунотерапия зависит не только от того, чтобы сильнее «пнуть» иммунную систему, но и от наличия правильного типа клеток, на которые можно опереться. Эта работа показывает, что подпитка и направляющее воздействие на дендритные клетки с помощью Flt3L может заполнить соседние лимфоузлы возобновляемым пулом стволоподобных киллерных T‑клеток. Когда затем применяют препараты блокады контрольных точек, такие как анти‑CTLA‑4, они могут задействовать этот резерв для порождения волн свежих бойцов, которые более многочисленны, более разнообразны и лучше контролируют опухоли. Анализы человеческих онкологических наборов данных указывают, что генные сигнатуры, связанные с этим путём, также предсказывают лучшие исходы у пациентов. В совокупности эти результаты указывают на потенциал комбинированных подходов, которые сначала создают правильный «посевной фонд» иммунных клеток с такими агентами, как Flt3L, а затем высвобождают его с помощью препаратов блокады контрольных точек для более сильного и длительного контроля рака.
Цитирование: Lai, J., Chan, C.W., Armitage, J.D. et al. Flt3L-mediated tumor cDC1 expansion enhances immunotherapy by priming stem-like CD8+ T cells in lymph nodes. Nat Immunol 27, 530–542 (2026). https://doi.org/10.1038/s41590-026-02419-4
Ключевые слова: иммунотерапия рака, дендритные клетки, стволоподобные CD8 T клетки, блокада контрольных точек, лиганд Flt3