Clear Sky Science · ru
CD38 наделяет локальные антиген-специфические Treg-клетки стрессоустойчивостью для контроля компартментализованного воспаления ЦНС
Почему важны иммунные клетки, защищающие мозг
Многие аутоиммунные болезни мозга, такие как рассеянный склероз, ведут себя как тлеющие пожары: первоначальный всплеск воспаления стихает, но повреждения могут снова вспыхнуть спустя годы. В этом исследовании задают на первый взгляд простой, но важный вопрос: что поддерживает мир в ЦНС после атаки и что сдвигает равновесие обратно в сторону болезни? Авторы сосредотачиваются на небольшой популяции иммунных клеток — регуляторных T-клетках, которые оседают в мозге и спинном мозге после воспаления, и раскрывают, как один молекулярный маркер на поверхности позволяет им выживать в суровой среде и предотвращать рецидивы.
Иммунные миротворцы, которые остаются
Используя модель на мышах, имитирующую отдельные черты рассеянного склероза, исследователи отслеживали разные типы T-клеток по мере нарастания болезни и последующего восстановления. В то время как обычные хелперные T-клетки, вызывающие воспаление, уменьшались по мере улучшения симптомов, регуляторные T-клетки — специализированные клетки, которые подавляют иммунные ответы — сохранялись в ЦНС. Их относительная доля среди местного пула T-клеток фактически увеличивалась, и они образовывали скопления в отдельных нишах вокруг пространств с цереброспинальной жидкостью и защитных оболочек мозга. Мечение происхождения входящих T-клеток показало, что после восстановления очень мало новых регуляторных T-клеток поступало из лимфатических узлов. Вместо этого популяция в ЦНС в основном поддерживалась локально, что указывает на долгосрочные «миротворческие» резидентные силы. 
Стрессоустойчивые стражи в враждебной нише
Поствоспалительная ЦНС далеко не комфортна для этих стражей. После основной волны болезни уровни ростового сигнала интерлейкина-2 (IL-2), от которого регуляторные T-клетки сильно зависят, падают, поскольку большинство обычных T-клеток отступает. В то же время ткань богата метаболитом NAD+, который может вызывать гибель клеток или ослаблять ключевые поверхностные рецепторы при модификации специальным ферментом. Генетически маркируя и отслеживая отдельные регуляторные T-клетки, авторы разделили их на «стабильные» клетки, которые сохраняли свою идентичность, и «нестабильные», потерявшие характерную программу Foxp3. Стабильные клетки проявляли гораздо более выраженный профиль сигнальной активности IL-2 и более высокий уровень рецепторов IL-2, что предполагает, что способность чувствовать скудный IL-2 является ключевой для выживания в этой стрессовой среде.
Локальный контроль рецидивов изнутри мозга
Чтобы проверить, действительно ли эти резидентные регуляторные T-клетки важны для долгосрочного контроля болезни, исследователи избирательно удаляли их из ЦНС, вводя токсин непосредственно в мозговую жидкость, при этом большинство системных регуляторных T-клеток в теле оставалось нетронутым. В течение нескольких дней ранее выздоравливающие мыши развивали тяжелые рецидивы с возобновлением паралича. Напротив, истощение регуляторных T-клеток только в теле, при сохранении их в ЦНС, не вызывало вспышек. Рецидив сопровождался быстрой реактивацией и расширением эффекторных T-клеток, уже находившихся в ЦНС, даже когда их приток из крови был заблокирован. Это демонстрирует, что локальные регуляторные T-клетки, а не циркулирующие, необходимы для сдерживания оставшихся агрессивных клеток, которые задерживаются после острой атаки.
Как один фермент защищает регуляторные клетки
Углубившись в механизм, авторы искали молекулы, отличающие стрессоустойчивые регуляторные T-клетки ЦНС. Ключевым игроком оказался CD38 — фермент на поверхности клетки, разрушающий внеклеточный NAD+. В воспалённой ЦНС регуляторные T-клетки резко повышали экспрессию CD38, тогда как обычные T-клетки не демонстрировали такого заметного изменения. Когда команда переносила миелин-реактивные регуляторные T-клетки, лишённые CD38, в мышей, эти клетки попадали в ЦНС, но не могли контролировать болезнь, в отличие от нормальных клеток. В смешанных химерных животных, где только резидентные регуляторные T-клетки были лишены CD38, удаление фракции, содержащей CD38, было достаточно, чтобы спровоцировать рецидивы, показывая, что CD38 действует в клеточно-интринсивном (внутриклеточном) режиме, позволяя эффективно контролировать процесс.
Защита жизненно важного сигнала
Механистические эксперименты показали, как CD38 придаёт эту устойчивость. Высокие уровни NAD+ в ЦНС способствуют химической модификации поверхностных белков ферментом ARTC2.2. Одним чувствительным мишеням является высокоаффинный субъединичный компонент рецептора IL-2, который регуляторные T-клетки экспрессируют на очень высоком уровне, особенно при распознавании антигенов мозга. У CD38-дефицитных регуляторных T-клеток, подвергшихся действию NAD+, большинство рецепторов IL-2 подвергались модификации, что приводило к слабой активации вниз по каскаду белка-переносчика STAT5 и сниженной чувствительности к IL-2. Напротив, клетки, экспрессирующие CD38, локально снижали уровень NAD+ вокруг себя, ограничивая эту вредную модификацию и сохраняя сильную передачу сигналов IL-2. В живых мышах введение NAD+ в мозг избирательно убивало большинство регуляторных T-клеток через этот путь, в то время как обычные T-клетки оставались в основном невредимыми, подчёркивая, насколько хрупка эта ниша без защитного фермента. 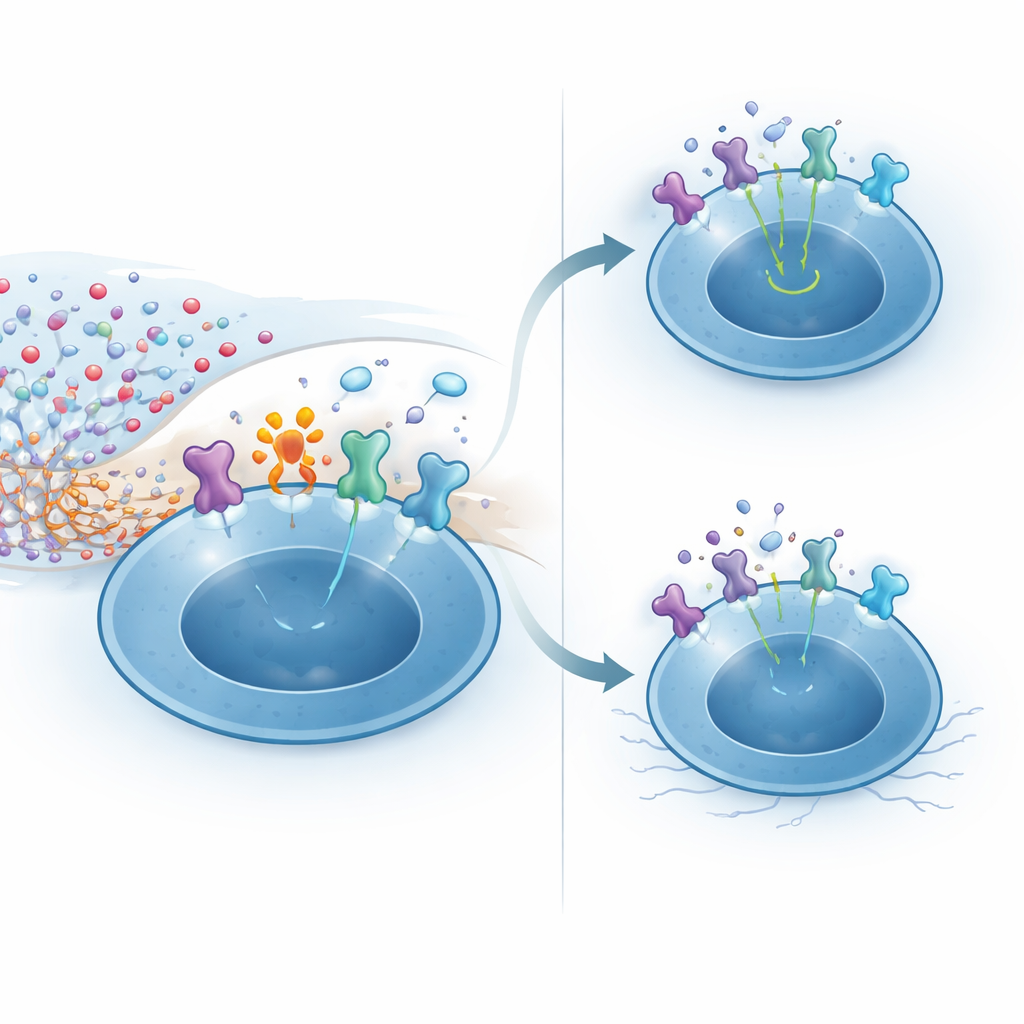
Что это значит для хронической аутоиммунности мозга
Эта работа изображает хроническую аутоиммунность ЦНС как компартментализованную битву: небольшие очаги оставшихся агрессивных T-клеток располагаются в мозге и спинном мозге и сдерживаются столь же специализированными локальными регуляторными T-клетками. Эти стражи «стрессоустойчивы», потому что CD38 позволяет им выживать при высоких уровнях NAD+ и продолжать чувствовать крошечные количества IL-2, сохраняя их идентичность и супрессивную функцию. Для широкой аудитории ключевой вывод таков: долгосрочный контроль заболеваний вроде рассеянного склероза может зависеть не столько от циркулирующей иммунной системы, сколько от поддержки и защиты этих резидентных миротворцев внутри мозга — потенциально посредством таргетирования путей, повышающих функцию CD38 или чувствительность к IL-2 в регуляторных T-клетках.
Цитирование: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
Ключевые слова: регуляторные T-клетки, рассеянный склероз, воспаление центральной нервной системы, фермент CD38, иммунная толерантность