Clear Sky Science · ru
Пространственная организация TGFβ-сигналинга фибробластов как основа устойчивости к лечению при ревматоидном артрите
Почему важна упорная боль в суставах
У многих людей с ревматоидным артритом современные препараты, подавляющие иммунную систему, уменьшают воспаление, но суставы остаются болезненными и скованными. В этом исследовании задаются вопросом, почему некоторые пациенты не выздоравливают, даже когда воспаление в суставе, по видимому, стихает. При внимательном изучении того, где и как определённые поддерживающие клетки сустава включают программы рубцевания, исследователи обнаруживают скрытую форму повреждения, которая может объяснять продолжающуюся боль и указывать на новые стратегии лечения.
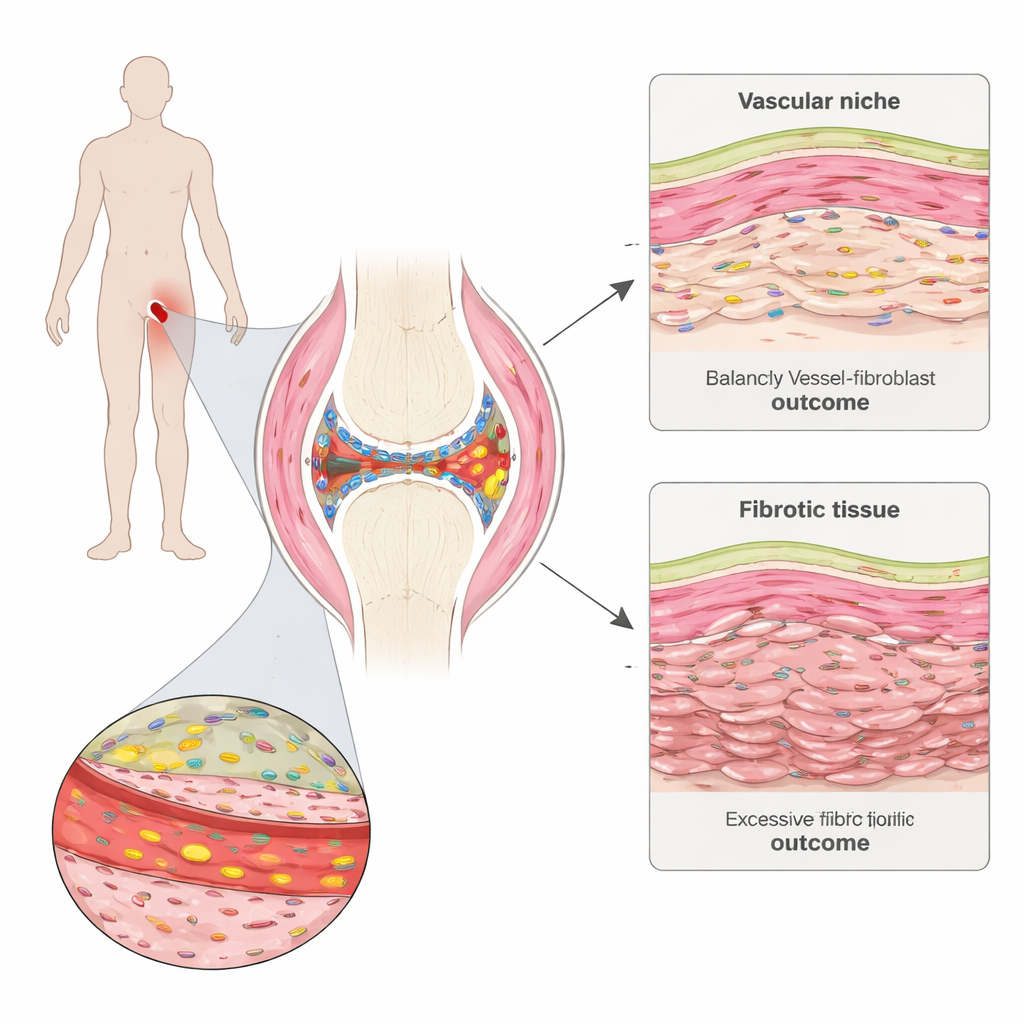
Взгляд внутрь болящего сустава
Ревматоидный артрит поражает синовию — тонкую ткань, выстилающую и смазывающую суставы. Команда взяла небольшие биопсии синовии у людей с ранней стадией болезни до начала терапии и повторно через шесть месяцев. С помощью передовой пространственной картографии экспрессии генов они могли видеть, какие гены активны в тысячах отдельных клеток, сохраняя при этом их расположение в ткани. Были выделены разные «районы» синовии, включая скопления иммунных клеток, жировые зоны, тонкую внутреннюю оболочку и области, насыщенные кровеносными сосудами и структурными клетками — фибробластами.
Клетки, формирующие рубец, и устойчивость к лечению
Сравнивая пациентов, которые впоследствии достигли ремиссии, с теми, кто не выздоровел, исследователи обнаружили поразительную закономерность: ещё до лечения у пациентов без ремиссии уже были более выраженные признаки рубцевания ткани, или фиброза. Особая программа фибробластов, характеризующаяся высокой продукцией внеклеточного матриксного белка COMP, была расширена у этих пациентов. Эти COMP-обогащённые фибробласты имели общие черты с клетками, формирующими рубцы при фиброзе лёгких и кожи, и сильнее всего коррелировали с плохим ответом на лечение. Со временем области, доминируемые этими клетками, становились плотными по соединительной ткани и относительно бедными по числу клеток, что указывает на отложение жёсткого матрикса, способного сохраняться даже после угасания воспаления.
Кровеносные сосуды как скрытые дирижёры
Фиброгенные фибробласты не были разбросаны случайно. Они образовывали скопления вокруг кровеносных сосудов, формируя слоистые периваскулярные зоны. Внутренний слой, прилегающий к стенке сосуда, экспрессировал другие гены, чем внешний слой. Команда показала, что клетки, выстилающие сосуды, посылают Notch-сигналы соседним фибробластам, которые, в свою очередь, модифицируют реакцию этих фибробластов на семейство про-рубцовых сигналов, известных как TGF‑beta. Близко к сосуду Notch-сигнал стимулирует фибробласты к продукции TGF‑beta, но одновременно уменьшает число рецепторов TGF‑beta на их поверхности, сдерживая чувствительность. Дальше от сосуда, где влияние Notch ослабевает, фибробласты несут больше рецепторов и становятся сильно отзывчивыми, превращаясь в COMP-обогащённые клетки, ведущие к фиброзу.
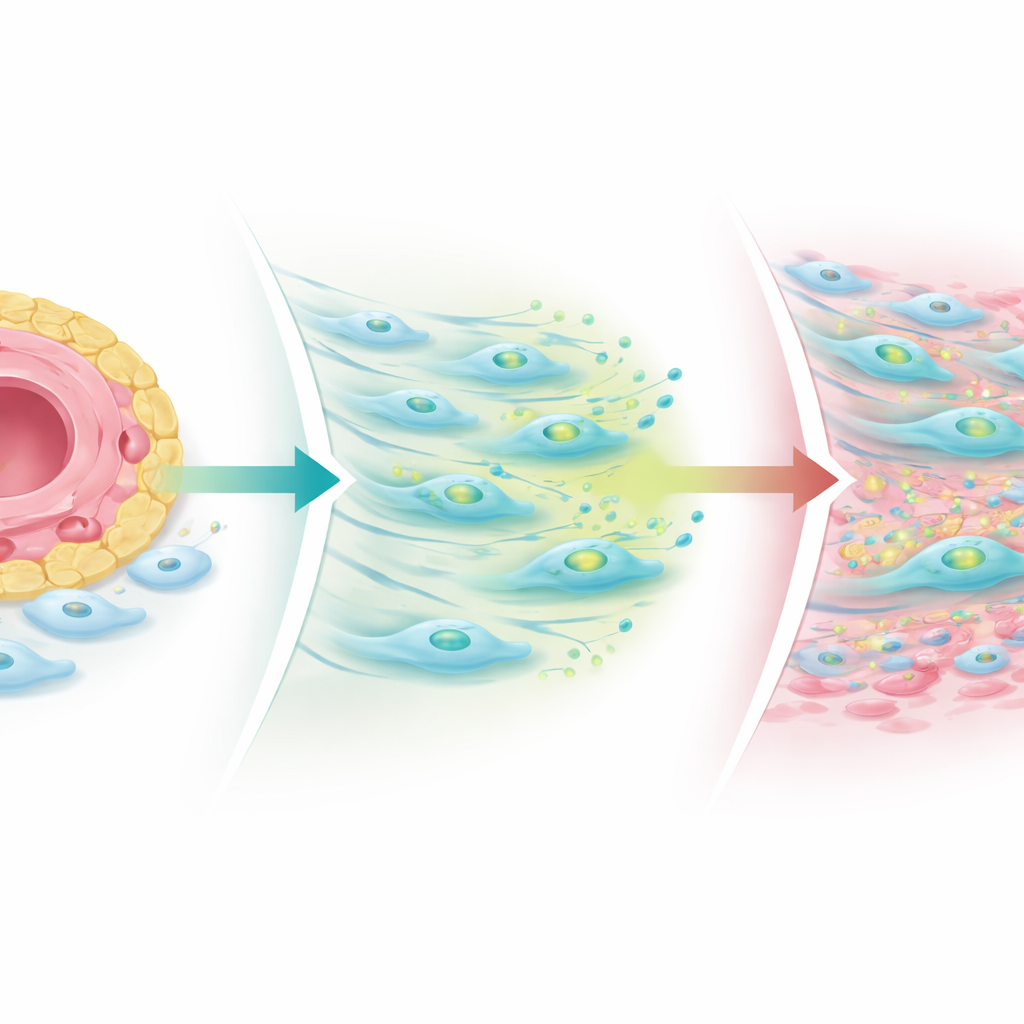
Что происходит, когда баланс нарушен
Исследователи построили упрощённые модели сустава в лабораторных чашках и трёхмерные органоиды из тканевых образцов пациентов, чтобы изучить этот механизм. При усилении Notch-сигнальных потоков от эндотелиальных клеток фибробласты увеличивали продукцию TGF‑beta, но снижали уровень рецепторов, ограничивая рубцевание. Когда Notch блокировали или нарушали его устойчивую картину, фибробласты восстанавливали рецепторы TGF‑beta — особенно со-рецептор TGF‑beta рецептор III — и COMP‑положительные фиброгенные клетки расширялись вглубь от сосудов. В биопсиях пациентов, взятых после лечения, иммунные кластеры уменьшались почти у всех, тогда как фиброгенные ниши, особенно COMP-обогащённые участки, часто увеличивались, особенно у тех, у кого сохранялась боль в суставах. Это указывает на то, что стандартные противовоспалительные препараты могут погасить иммунный «огонь», оставляя или даже обнажая процесс рубцевания, который поддерживает скованность и боль в суставах.
Новые подходы к успокоению упорных суставов
Наконец, команда проверила, может ли прерывание этого фиброгенного контура иметь терапевтический эффект. В органоидах, полученных от пациентов, препараты, ингибирующие Notch или блокирующие сигналинг TGF‑beta, снижали продукцию COMP, других белков, связанных с рубцеванием, и ключевых коллагенов, а также перестраивали активность генов в периваскулярных зонах. Для непрофессионала послание таково: не всё повреждение при ревматоидном артрите объясняется видимым воспалением — часть его «жёстко запрограммирована» в поддерживающих клетках сустава и кровеносных сосудах. Нацеливание на диалог Notch–TGF‑beta, который контролирует, как фибробласты откладывают рубцовую ткань, может в будущем предотвратить или обратить упорную фибротическую форму болезни, устойчивую к современным иммунно-ориентированным препаратам.
Цитирование: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Ключевые слова: ревматоидный артрит, фиброз, фибробласты, сигналинг TGF-бета, путь Notch