Clear Sky Science · ru
Инжиниринг ксилозилтрансфераз для манипуляции протеогликанами в клетках млекопитающих
Почему клеточные «плащи» важны
Каждая клетка в нашем организме носит молекулярный «плащ», который помогает ей общаться с соседями и ощущать окружение. Существенная часть этого покрова состоит из протеогликанов — белков, украшенных длинными сахарными цепями, действующими как мини‑антенны для факторов роста, иммунных сигналов и структурных указаний. Когда такая сахарная модификация нарушается, развитие может давать сбой, а ткани, например кости и мышцы, страдать значительно. Тем не менее учёным долгое время было трудно точно сказать, какие белки несут эти цепи и как отдельные компоненты «плаща» влияют на поведение клетки. В этой работе предложена точная химическая стратегия для пометки и восстановления этих сахарных цепей в живых клетках млекопитающих, что открывает путь к чтению и переписыванию информации на их поверхности. 
Перенастройка первого шага присоединения сахара
Сборка протеогликанов начинается, когда специализированное семейство ферментов — ксилозилтрансферазы XT1 и XT2 — добавляет первый сахар к белку, отмечая место, где разрастётся длинная цепь. Поскольку оба фермента способны выполнять этот первый шаг, было трудно выяснить, к каким именно белкам каждый из них обращается в клетках. Авторы использовали подход «впадина‑и‑шишка» — распространённый в современной химической биологии — чтобы решить эту проблему. Они слегка изменили форму активного центра XT1, создав дополнительное пространство («впадина»), и ввели соответствующий, немного более объёмный сахарный строительный блок, 6AzGlc («шишка»). Получившийся инженерный XT1 теперь способен использовать этот модифицированный сахар, тогда как натуральный фермент — нет, что позволяет помечать только те белки, к которым прикасался перенастроенный фермент.
Проникновение дизайнерского сахара в клетки
Чтобы этот подход заработал в живых клетках, команде пришлось доставить «шишковый» сахар в форме, распознаваемой клеточным метаболизмом. Вместо опоры на обычные пути поглощения сахаров — которые плохо справляются с аналогами ксилозы — они создали защищённую (caged) версию 6AzGlc с спрятанной фосфатной группой. Попав в цитозоль, клеточные ферменты снимают защиту и превращают молекулу в UDP‑6AzGlc, активированную форму, необходимую для работы инженерных ксилозилтрансфераз. Тщательная хроматография подтвердила, что клетки, обработанные корректно сконструированным защищённым соединением, продуцировали значительные количества активированного дизайнерского сахара, тогда как зеркальный контроль давал почти нулевой результат. 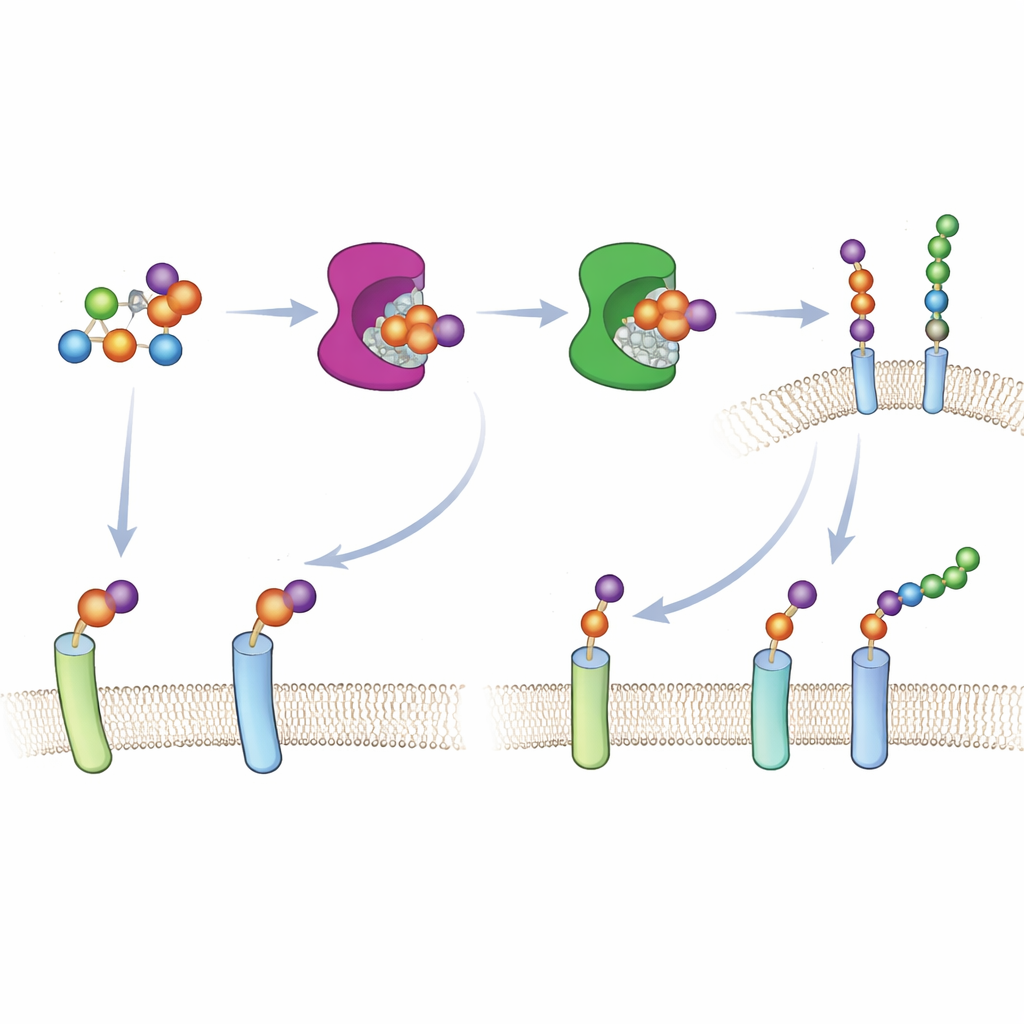
Пометка и идентификация скрытых участников
Имея и модифицированный фермент, и активированный сахар, исследователи показали, что только клетки, экспрессирующие инженерный XT1 или XT2, включали метку 6AzGlc в свои поверхностные протеогликаны. Азидная группа в 6AzGlc служит маленькой химической ручкой, которую можно «кликать» с помощью флуоресцентных красителей или биотина, что позволяет визуализировать и обогащать помеченные белки. Масс‑спектрометрия обогащённых образцов выявила богатый набор известных протеогликанов — включая декорин, несколько глипиканов, синдекан‑4, CD44 и версикан — подтверждая, что система отмечает подлинные сахар‑несущие белки. Важно, что инженерные ферменты сохранили те же предпочтения по последовательностям, что и их натуральные аналоги, то есть химическая метка устанавливается в аутентичных местах присоединения, а не в новых искусственных позициях.
Создание дизайнерских протеогликанов
Неожиданным преимуществом метки 6AzGlc стало то, что, в отличие от естественного начального сахара, она не может быть удлинена до полноразмерной цепи последующими ферментами. Это фактически «запирает» цепь и упрощает молекулярную структуру для анализа масс‑спектрометрией. Авторы превратили это свойство в инструмент: после того как XT1 устанавливает 6AzGlc в естественной точке присоединения, они с помощью клик‑химии прикрепляют синтетические фрагменты гепарина, создавая «дизайнерские протеогликаны» с точно заданными сахарными цепями. В раке молочной железы, в клетках, лишённых собственного синдекана‑1, возвращение таких дизайнерских версий восстановило нормальное распластывание на белково‑покрытой поверхности, показав, что химически пересобранный протеогликан способен функционально замещать натуральный.
Значение для биологии и медицины
Эта работа даёт мощный набор инструментов для селективной маркировки и манипуляции сахарными цепями, контролирующими клеточную коммуникацию. Разделяя роли XT1 и XT2 и помечая только их прямые мишени, исследователи теперь могут картировать, какие протеогликаны действуют в конкретных тканях и в состояниях заболеваний. Возможность останавливать естественный рост цепи и заменять её на созданные по заказу сахара также позволяет учёным выяснить, насколько функция протеогликана определяется белковым скелетом против его сахарного покрытия. В долгосрочной перспективе такая точная инженерия может помочь расшифровать сложную сигнализацию на поверхности клетки и вдохновить разработки терапий, восстанавливающих или перепрограммирующих дефектные клеточные «плащи» при нарушениях развития, раке и других заболеваниях.
Цитирование: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Ключевые слова: протеогликаны, гликозаминогликаны, ксилозилтрансфераза, химическая биология, сигнализация на поверхности клетки