Clear Sky Science · ru
Геномные исследования ассоциаций аутоиммунного гипотиреоза выявляют вклад иммунитета и специфические для щитовидной железы факторы и обратную связь с риском рака
Почему это важно для повседневного здоровья
Многие люди ощущают усталость, мерзнут или испытывают умственную затуманенность, не догадываясь, что виновата щитовидная железа. Аутоиммунный гипотиреоз, при котором собственная иммунная система постепенно атакует щитовидную железу, поражает более одного из двадцати человек. В этом исследовании использованы генетические данные сотен тысяч добровольцев для ответа на два крупных вопроса: какие наследуемые изменения в ДНК повышают вероятность этого состояния и как те же изменения связаны с риском развития рака? Ответы показывают неожиданную компромиссную ситуацию: иммунитет, который иногда повреждает щитовидную железу, может одновременно обеспечивать дополнительную защиту от опухолей.
Обзор по всему геному
Исследователи объединили медицинские записи и генетическую информацию из двух крупных популяционных проектов — FinnGen в Финляндии и UK Biobank в Великобритании. Они сосредоточились на людях, которым требовалась длительная заместительная терапия гормонами щитовидной железы, и тщательно исключили тех, чьи проблемы с щитовидной железой были следствием операций, рака или других неаутоиммунных причин. В результате получилось более 81 000 случаев аутоиммунного гипотиреоза и более 700 000 контрольных лиц, что делает это исследование крупнейшим по данному состоянию на сегодняшний день. Просканировав миллионы маркеров ДНК по всему геному, авторы обнаружили 418 независимых генетических сигналов вне основного кластера иммунных генов, распределённых по крайней мере в 280 областях генома. Многие из этих сигналов связаны с редкими или низкочастотными вариантами ДНК, изменяющими структуру белков, что даёт прямые подсказки к биологическим механизмам.
Отделение общих иммунных эффектов от специфичных для щитовидной железы
Аутоиммунный гипотиреоз лежит на пересечении общей аутоиммунности и уникальной биологии щитовидной железы. Чтобы разделить эти компоненты, команда сопоставила свои результаты с генетическими исследованиями других аутоиммунных заболеваний и с уровнями тиреотропного гормона в крови — ключевого клинического маркёра, используемого для выявления пониженной функции щитовидной железы. Применив байесовский метод классификации, они сгруппировали генетические сигналы на те, что общие для широкого круга аутоиммунных заболеваний, и те, что более специфичны для регуляции гормонов щитовидной железы. По оценкам, примерно 38% сигналов действуют через общие иммунные пути, влияющие на многие аутоиммунные состояния, тогда как около 20% влияют главным образом через функцию щитовидной железы. Варианты, направленные на щитовидную железу, чаще влияли на уровни гормонов и на гены, активные в ткани щитовидной железы, тогда как общие иммунные варианты проявляли активность в T-клетках — лейкоцитах, управляющих иммунными ответами.
Приближение к ключевому иммунному переключателю
Особенно заметным оказалось редкое изменение ДНК в гене ZAP70, кодирующем важный сигнальный белок в T-клетках. Тяжёлые дефекты этого белка известны как причина глубокой иммунной недостаточности, но вариант, обнаруженный в этом исследовании, вызывает лишь частичную потерю функции. Лабораторные эксперименты в модифицированных T-клетках показали, что изменённый ZAP70 ослабляет, но не полностью блокирует каскад сигналов, который обычно запускается после распознавания мишени. Клетки, несящие этот вариант, хуже включали маркёры активации и последующие сигнальные этапы. Такое притупление ответа, по-видимому, нарушает тонкий баланс, который обычно устраняет самореактивные T-клетки, предрасполагая носителей к аутоиммунным заболеваниям и одновременно умеренно увеличивая их риск некоторых иммунных дефицитов.
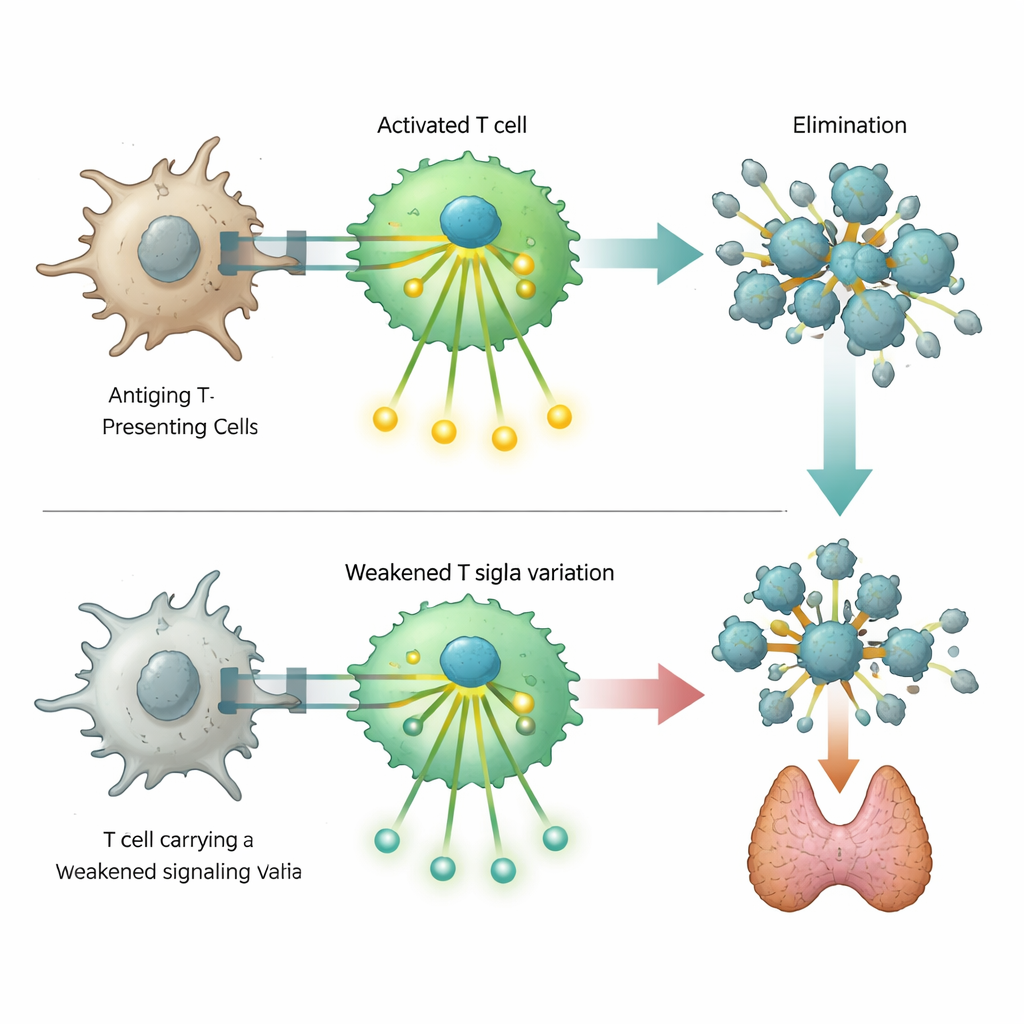
Неожиданная связь с защитой от рака
Поскольку те же иммунные пути, которые приводят к аутоиммунитету, могут также атаковать опухоли, авторы далее изучили, как генетика аутоиммунного гипотиреоза соотносится с риском рака. Они рассчитали полигенный риск‑скор, суммирующий наследственную предрасположенность к гипотиреозу, и проверили его связь с множеством заболеваний в финских данных. Как и ожидалось, более высокий скор коррелировал с повышенным риском различных аутоиммунных состояний. Более удивительным оказался устойчивый паттерн пониженного риска для ряда видов рака, особенно базально-клеточного карциномы и других кожных опухолей, а также рака молочной и предстательной железы и в общей категории «все виды рака». При непосредственном сравнении с результатами геномных исследований рака примерно 10% локусов, связанных с гипотиреозом, также влияли на риск кожного рака, причём один и тот же генетический вариант обычно увеличивал аутоиммунную направленность к щитовидной железе и одновременно снижал риск кожного рака. Эти общие варианты концентрировались в иммунных генах, включая известные мишени для препаратов чекпойнт‑иммунотерапии.
Что это значит для пациентов и медицины
С точки зрения широкого читателя, работа показывает, что некоторые люди рождаются с чуть более «заряженной» иммунной системой: это делает их более склонными к медленному, часто незаметному повреждению щитовидной железы, но одновременно лучше подготовленными к распознаванию и уничтожению зарождающихся опухолей. Исследование разделяет генетические изменения, действующие через общую иммунную гиперактивность, и те, что специфично влияют на продукцию гормонов щитовидной железы, что объясняет, почему такие состояния, как болезнь Хашимото и болезнь Грейвса, могут иметь общие риски, но по-разному смещать функцию щитовидной железы. Работа также помогает понять, почему пациенты, у которых развиваются проблемы с щитовидной железой на фоне иммунно-стимулирующей терапии от рака, нередко лучше реагируют на эти препараты. В целом результаты указывают, что обычные естественные варианты в генах иммунных контрольных точек и сигнальных путях формируют и аутоиммунные болезни щитовидной железы, и пожизненный риск рака, открывая новые перспективы для профилактики и более персонализированного применения иммунотерапии.
Цитирование: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Ключевые слова: аутоиммунный гипотиреоз, заболевание щитовидной железы, генетический риск, иммунная система, защита от рака