Clear Sky Science · ru
Расширения повторов GGC в новых открытых рамках считывания транслируются в токсичные полиглициновые белки при окулофарингодистальной миопатии
Скрытые послания в нашей ДНК
Большинству из нас в школе объясняли, что лишь небольшая часть нашей ДНК кодирует белки, а остальное когда‑то списывали как «мусор». Это исследование переворачивает эту идею. Оно показывает, что небольшие, легко пропускаемые фрагменты повторяющейся ДНК могут тайно порождать новые белки, которые повреждают мышцы и мозг, тем самым помогая объяснить группу редких, но разрушительных неврологических заболеваний — и указывая на возможный путь их лечения.
Повторяющаяся ДНК и загадочные мышечные болезни
Наш геном полон крошечных повторяющихся последовательностей, похожих на трибуквенные слоги, скопированные снова и снова. Когда некоторые из этих повторов становятся слишком длинными, они могут вызывать более 60 известных заболеваний человека. При окулофарингодистальной миопатии (OPDM) и родственном заболевании с поражением мозга — OPML — у пациентов развиваются опущенные веки, затрудненное глотание, слабость в руках и ногах и иногда более широкие поражения нервов и мозга. Под микроскопом врачи видят характерные скопления белка внутри мышечных и нервных клеток, но до сих пор было неясно, как повторы, расположенные в якобы «некодирующих» областях ДНК, могут порождать токсичные белки.
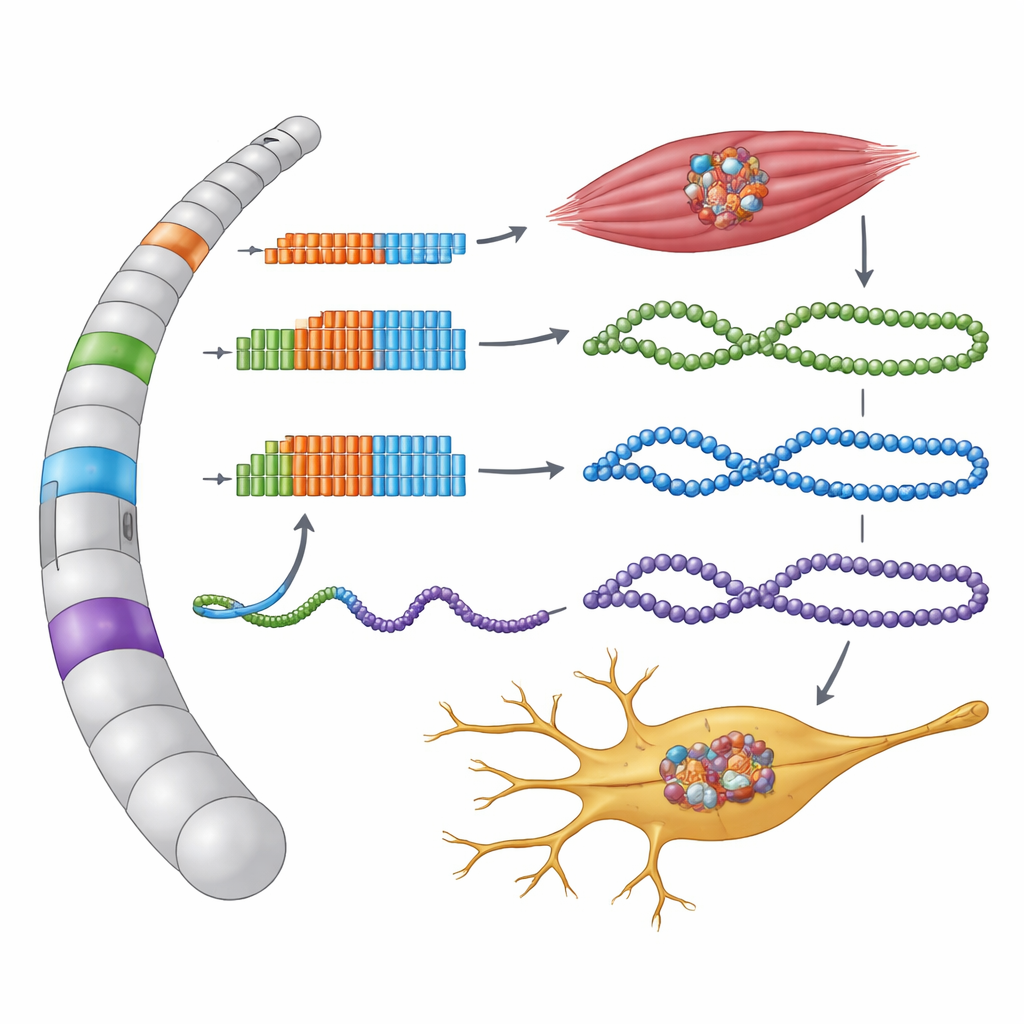
Некодирующие регионы, которые тайно синтезируют белок
Исследователи сосредоточились на участках ДНК, где трехбуквенная последовательность GGC повторяется многократно в нескольких генах, связанных с OPDM и OPML. Эти повторы расположены в областях, обозначенных как некодирующие — в нематерилизованных хвостах генов или в длинных РНК, считавшихся не переводимыми в белок. Воссоздав эти человеческие последовательности в клетках и отслеживая, как их считывают, команда обнаружила, что каждая последовательность GGC фактически находится внутри крошечной, ранее не замеченной белок-кодирующей единицы — небольшой открытой рамки считывания. Когда клетки читают эти скрытые инструкции, каждый GGC‑повтор транслируется в аминокислоту глицин, образуя необычно длинные «полиглициновые» хвосты на новых микро‑белках.
Новые токсичные белки, которые слипаются и убивают клетки
С помощью специально созданных антител учёные показали, что эти микро‑белки с полиглициновыми участками присутствуют в мышечных образцах пациентов и концентрируются именно там, где обнаруживаются странные p62‑позитивные белковые включения. Затем они заставили человеческие мышечные клетки, плодовых мух и мышей синтезировать те же типы полиглициновых белков. Во всех трёх системах белки конденсировались в округлые плотные включения в цитоплазме и ядре, похожие на те, что видны в тканях пациентов. Клетки, производившие эти белки, с большей вероятностью погибали, а у мышей поражённые мышцы демонстрировали уменьшение волокон, внутриядерное расположение ядер и признаки воспаления. Когда белки накапливались в мозге и сердце, животные проявляли нарушения движения, нейродегенерацию, кардиомиопатию и сниженную продолжительность жизни, что соответствует многим симптомам, описанным у пациентов.

Одна основная токсическая черта — множество местных вариантов
Хотя эти микро‑белки имеют общую центральную черту — длинную цепочку остатков глицина — они не идентичны. Каждый возникает из разной крошечной рамки считывания в разных генах и потому содержит уникальные аминокислотные участки, окружающие полиглициновый фрагмент. Команда выяснила, что эти прилегающие сегменты существенно влияют на поведение белков: где в клетке они накапливаются, насколько склонны образовывать агрегаты, с какими клеточными партнёрами взаимодействуют и насколько токсичны для мышечных и нервных клеток. Некоторые варианты оказывались особенно вредными, быстро вызывая формирование включений и гибель клеток, тогда как другие были относительно более мягкими. Это указывает на общий токсический механизм в основе заболевания, который уточняется локальным контекстом последовательности.
Первый шаг к общей стратегии лечения
Обнадеживает, что исследователи также выявили малую молекулу — катионный порфирин TMPyP4, — которая может снизить как накопление, так и токсичность этих полиглициновых белков в клетках и в модели на дрозофиле. По-видимому, TMPyP4 действует в основном, препятствуя трансляции GC‑богатых повторов, уменьшая продукцию вредных белков без широкого подавления синтеза белка. Хотя это далеко от готового лекарства, вещество служит доказательством принципа, что единый терапевтический подход однажды мог бы помочь пациентам с несколькими родственными состояниями, вызванными похожими расширениями повторов.
Что это значит для нашего понимания болезней
Для неспециалиста основной вывод впечатляющ: участки ДНК, долгое время считавшиеся некодирующими, могут скрывать крошечные рецепты белков, которые становятся опасными при расширении определённых повторов. При OPDM, OPML, заболевании с внутриядерными включениями нейронов и родственных расстройствах расширенные GGC‑повторы транслируются в липкие полиглициновые белки, которые скапливаются внутри клеток и постепенно нарушают функции мышц, нервов и мозга. Обнаружив этот общий механизм и первый кандидат на соединение, способное его ослаблять, исследование расширяет наше представление о том, что считается геном, и открывает новые пути для лечения растущего семейства нейродегенеративных заболеваний, вызванных расширениями повторов.
Цитирование: Boivin, M., Yu, J., Eura, N. et al. GGC repeat expansions within new open reading frames are translated into toxic polyglycine proteins in oculopharyngodistal myopathy. Nat Genet 58, 517–529 (2026). https://doi.org/10.1038/s41588-026-02507-z
Ключевые слова: окулофарингодистальная миопатия, микросателлитное расширение повтора, полиглициновые белки, трансляция некодирующей ДНК, нейродегенеративное мышечное заболевание